��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (8��)?��������ԭ��Ӧ�У�������______���ӣ������ķ�Ӧ��_________��Ӧ����ԭ��________���ӣ������ķ�Ӧ��____________��Ӧ������������Ӧ�ķ���ʽΪ��2Fe+3Cl2====2FeCl3������������_______�ۣ���������ķ�ӦʽΪ________��������������________�ۣ���ʵ֤���������������Ա������������(�ǿ��������)____________��
�ο��𰸣���8�֣���
�����������
�����Ѷȣ���
2��ѡ���� ��Ũ����ͬ��Al2��SO4��3����NH4��2Fe��SO4��2��MgSO4��Һ�У�����������Ũ�ȵ�BaCl2��Һʱ��ǡ��ʹ����������Һ��SO42-ȫ����������Al2��SO4��3����NH4��2Fe��SO4��2��MgSO4��������Һ�����֮��Ϊ��������
A��1��2��3
B��3��2��1
C��2��3��6
D��6��3��2
�ο��𰸣�����������Ũ�ȵ�BaCl2��Һ��ǡ��ʹ����������Һ��SO42-ȫ��������˵��Ũ����ͬ��Al2��SO4��3����NH4��2Fe��SO4��2��MgSO4��Һ�к��е�SO42-���ʵ�����ͬ��
��BaSO4�����ʵ���Ϊ1mol����
n[Al2��SO4��3]=13n��BaSO4��=13��1mol=13mol��
n[��NH4��2Fe��SO4��2]=12n��BaSO4��=12mol��
n��MgSO4��=n��BaSO4��=1mol��
��Ũ����ͬ�����n=cV��֪Ũ����ͬ�����£���Һ���֮�ȵ����������ʵ���֮�ȣ�����Ҫ���������ε����֮��Ϊ13mol��12mol��1mol=2��3��6��
��ѡC��
���������
�����Ѷȣ�һ��
3������� �ҹ����Ṥҵ��SO2�ŷ���Լ10��֣����Ṥҵ��β��������д�����
��1��ij�������ð�-�������������������ͬʱ���ս�¯���еİ����乤������ͼ��ͼ1��
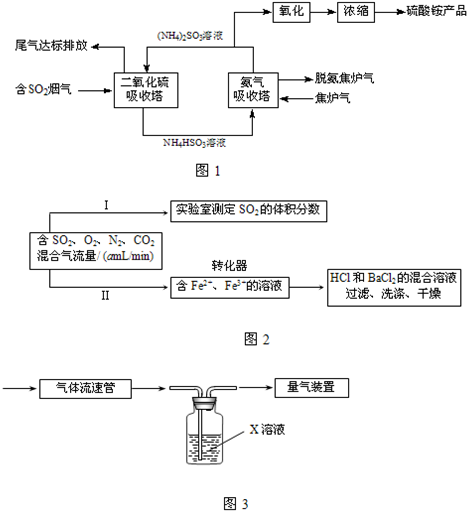
�ٴӻ��������ĽǶȿ��������������տɷ�ֹ______�����һ����ʵ�鷽��������β�����Ƿ��а�����______��
�ڰ����������з�����Ӧ�����ӷ���ʽΪ______��
��2����ѧ���������Fe3+�������ԣ���SO2������SO42-��ʵ��SO2�Ļ������ã�
��ͼ2ʵ���ɲ���ͼ3װ��ģ��ⶨ������SO2�����������X��Һ����ѡ��______��
��ͼ2ʵ��ɲ������з����ⶨSO2�����������ȡ280mL����״����������Ʒ������Fe2��SO4��3��Һ��ȫ��Ӧ����Ũ��Ϊ0.020mol/L��K2Cr2O7��Һ�ζ���Ӧ���ɵ�Fe2+�����յ�����K2Cr2O7��Һ25.00mL��β����SO2���������Ϊ______��
��֪��Cr2O72-+Fe2++H+��Cr3++Fe3++H2O��δ��ƽ��
�ۼ���ʵ����ڱ�״���½��У�����֪�������������Ϊ�ⶨת������SO2������SO42-��ת���ʣ���ʵ���л���ⶨ��������______��______��
�ο��𰸣���1���ٺ�����������������IJ�������������ˮ�嵪��Ӫ������������ʹʪ��ĺ�ɫʯ����ֽ��죬
�ʴ�Ϊ������IJ�����ˮ�嵪��Ӫ��������ʪ��ĺ�ɫʯ����ֽ����β����Ʒ�У��۲���ֽ�Ƿ������
��NH4HSO3�����ԣ�����������ʷ�Ӧ��NH4HSO3-+NH3?H2O�T��NH4��2SO3+H2O��
�ʴ�Ϊ��HSO3-+NH3?H2O�TSO32-+NH4++H2O��
��2���ٶ������������л�ԭ�ԣ�����������Ե����Ը�����ػ��ˮ��Ӧ���ʴ�Ϊ����ĵ�����Һ��������KMnO4��Һ����
������Ʒ��SO2�����������x����
? 6SO2 ��12Fe2+��2Cr2O2-7
? 6mol? 2mol
?0.280xL22.4L/mol? ?0.025L��0.020mol/L
���x=12.00%��
�ʴ�Ϊ��12.00%��
�����ⶨת������SO2������SO42-��ת���ʣ�����Ҫ�ⶨʱ������ɳ������������ʴ�Ϊ��ʵ��ʱ�䣻BaSO4��������
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪NH4CuSO3��������10 mol/L�������ȣ��������������к�ɫ��������
�ڲ����̼�����ζ������ ����Һ������ɫ������ݴ��ж�����˵����ȷ����
A����Ӧ��������������
B��NH4CuSO3����Ԫ�ر�����
C���̼�����ζ�������ǰ���
D��1 mol NH4CuSO3��ȫ��Ӧת��0.5 mol����