微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以下实验现象的描述错误的是
[? ]
A.紫色石蕊试液中滴加氯水,溶液先变红后褪色
B.品红试液中通入SO2后溶液由红色褪为无色,加热后又变红色
C.FeCl2溶液中滴入KSCN溶液,溶液呈血红色
D.蓝色的胆矾晶体中加入浓硫酸,晶体会转化为白色固体
参考答案:C
本题解析:
本题难度:简单
2、简答题 在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液变为黄色.
(1)甲同学认为这不是发生化学反应所致,则使溶液变黄色的物质是(填粒子的化学式,下同)______;乙同学认为这是发生化学反应所致,使溶液变黄色的物质是______.
(2)现提供以下试剂:A.酸性高锰酸钾溶液?B.氢氧化钠溶液?C.四氯化碳?D.硫氰化钾溶液?
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象.
| ______同学正确 | 选用试剂 | 实验现象
第一种方法
______
______
第二种方法
______
______
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是______.
(4)若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,你认为是否可行?______;理由是______.
参考答案:(1)因溴水的颜色为黄色,则溶液呈黄色是因为含有Br2所致;氧化性:Br2>Fe3+,则发生2Fe2++Br2=2Fe3++2Br-,生成Fe3+且Fe3+在水中为黄色,溶液呈黄色是因为含有Fe3+所致,
故答案为:Br2,Fe3+;?
(2)溴易溶于四氯化碳中而不易溶于水中,且四氯化碳与水不溶,根据四氯化碳层颜色判断,如果有机层无色,则说明使溶液呈黄色的物质不是溴;
Fe3+遇KSCN溶液变为红色,向溶液中滴加硫氰化钾溶液后,溶液呈红色,则说明使溶液呈黄色的物质是铁离子,
所以乙同学正确,
故答案为:乙
方法选用试剂实验现象第一种方法C有机层无色第二种方法D溶液变红(3)因还原性Fe2+>Br-,通入氯气时还原性强的离子先被氧化,即Fe2+先被氧化,故答案为:Fe2+;
(4)溴和铁离子都具有氧化性,都能把碘离子氧化生成碘单质,碘遇淀粉试液变蓝色,所以不能用碘化钾判断,故答案为:不可以,因为Br2和Fe3+都能把I-氧化成I2,遇淀粉均蓝色.
本题解析:
本题难度:一般
3、选择题 下列有关化学实验操作的叙述正确的是( )
A.在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液
B.向SO2溶液中分别滴加Ba(NO3)2、BaCl2、Ba(OH)2溶液,均产生BaSO3白色沉淀
C.向2.0mL浓度均为0.1mol/L的KCl和Kl混合溶液中滴加1~2滴0.01mol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大
D.分别电解熔融氯化镁和熔融氯化铝可以制取金属镁和金属铝
参考答案:C
本题解析:
本题难度:一般
4、简答题 硫酸亚铁是比较重要的亚铁盐,在农业上用作农药,主治小麦黑穗病,在工业上用于染色、制造蓝黑墨水和木材防腐、除草剂等.
(1)实验室条件下用铁粉和稀硫酸制取少量硫酸亚铁溶液,为防止其变质,应在该溶液中应加入适量______.
(2)新制的绿矾晶体(FeSO4?7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:______.
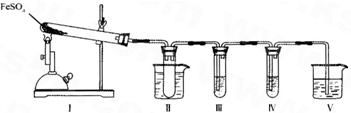
(3)已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2.某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物.已知SO3的熔点是16.8°C,沸点是44.8°C.
①装置II的试管中不装任何试剂,其作用是______,试管浸泡在50℃的热水浴中,目的是______.
②装置III和装置IV的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.
限选试剂:3mol.L-1.H2S04、6mol.L-l?NaOH、0.5mol.L?-1?BaCl2、O.5mol.L-1Ba(NO3)2、0.01mol.L-1?酸性?KMnO4?溶液、0.0l?mol.L-1?溴水.
检验试剂
预期现象与结论
装置III的试管中加入足量______.
产生大量白色沉淀,证明气体产物中含有SO3.
装置IV的试管中加入足量______.
______
______.