微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框图进行反应;又知单质A是当今世界产量最大的金属,E的溶液是无色的.请回答:
(1)A是______,B是______,C是______(请填写化学式);
(2)反应①的化学方程式______;
(3)反应③的离子方程式______;
(4)反应④的离子方程式______.
参考答案:B为黄绿色气体,应为Cl2,单质A是当今世界产量最大的金属,应为Fe,则D为FeCl3,F能与Cl2反应生成FeCl3,则F应为FeCl2,则E为HCl的水溶液,C为H2,则
(1)由以上分析可知,A为Fe,B为Cl2,C为H2,故答案为:Fe,Cl2,H2;
(2)反应①为Fe和Cl2的反应,反应的化学方程式为2Fe+3Cl2?点燃?.?2FeCl3,故答案为:2Fe+3Cl2?点燃?.?2FeCl3;
(3)反应③为Fe和HCl的反应,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(4)反应④为FeCl2和Cl2的反应,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
本题解析:
本题难度:一般
2、推断题 A.J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极;?F常温下是气体,各物质有以下的转化关系(部分产物及条件略去)。?

请回答以下问题:? ?
(1)写出原电池的负极反应方程式________________
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为_____________(写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者___________?后者(用“>”、“<”或“=”表示)。 ?
(3)写出②的化学方程式_____________?
(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过蓝色的钴玻璃观察火焰呈紫色。
①X的水溶液与NaHCO3溶液混合,反应的离子方程式为_________
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图:?
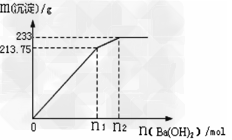
请回答:X晶体的俗名为___________;其溶液的物质的量浓度为__________?mol/L。
参考答案:(1)Al+4OH--3e- = AlO2-+2H2O?
(2)10-2-10-12 mol/L或c(OH-)-c(H+)?;<?
(3)4NH3+5O2 4NO+6H2O?
4NO+6H2O?
(4)①Al3++3HCO3- = Al(OH)3↓+3CO2↑? ;? ②明矾 ;1mol/L
本题解析:
本题难度:一般
3、填空题 下列物质A~F是我们熟悉的单质或化合物,其中A、B是常见的金属,E在常温下是黄绿色气体;在适当的条件下,他们之间可以发生如图所示的转化.
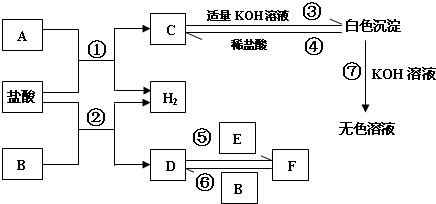
试回答下列问题:
(1)A的化学式是______;
(2)在①-⑦反应中,属于氧化还原反应的有______,其中属于置换反应的有______;
(3)写出上图中白色沉淀与NaOH溶液反应的离子方程式:______;
(4)请写出在D的溶液中滴加NaOH溶液的过程中发生反应的化学方程式______、______.
(5)检验上图无色溶液中金属阳离子的方法是(填写实验名称):______,现象是______.
参考答案:A是常见的金属,由A+盐酸→C+H2,C为金属氯化物,C与KOH反应生成白色沉淀,可以溶于KOH、盐酸,故该白色沉淀为Al(OH)3,则C为AlCl3,A为Al.E在常温下是黄绿色气体,E为Cl2,由B+盐酸→D+H2可知,D为金属氯化物,D能与氯气反应生成F,F能与金属B反应得到D,则B为变价金属Fe,则D为FeCl2,F为FeCl3,FeCl3溶液可以与Fe反应生成FeCl2,
(1)由上述分析可知,A的化学式是Al,故答案为:Al;
(2)在①-⑦反应中,反应①②⑤⑥属于氧化还原反应,其中①②属于置换反应,
故答案为:①②⑤⑥;①②;
(3)图中白色沉淀为氢氧化铝,与NaOH溶液反应生成偏铝酸钠与水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)FeCl2溶液中滴加NaOH溶液的过程中发生反应的化学方程式:FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)上图无色溶液中金属阳离子为K+,利用焰色反应进行检验,透过蓝色钴玻璃观察火焰颜色为紫色说明含有K+,
故答案为:焰色反应;透过蓝色钴玻璃观察火焰颜色为紫色.
本题解析:
本题难度:一般
4、填空题
(10分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按下面框图进行反应。又知D溶液为黄色,E溶液是无色的,请回答:
(1)D的化学式是是________,画出B元素原子结构示意图__________。
(2)反应④的化学方程式为____________________。
(3)现有12mol/L的E溶液, 要稀释为0.15mol/L的稀溶液480mL,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管、还需要_________________。量取浓溶液的体积是______mL。在配置过程中如果定容时俯视刻度线,会造成所配溶液浓度________(填“偏高”、“偏低”或“无影响”,下同),如果实验完毕忘记洗涤量筒会造成所配溶液浓度_______。
要稀释为0.15mol/L的稀溶液480mL,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管、还需要_________________。量取浓溶液的体积是______mL。在配置过程中如果定容时俯视刻度线,会造成所配溶液浓度________(填“偏高”、“偏低”或“无影响”,下同),如果实验完毕忘记洗涤量筒会造成所配溶液浓度_______。
参考答案:

本题解析:略
本题难度:一般
5、填空题 根据如图推断填空:
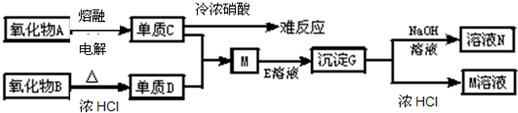
(1)C是______,D是______,G是______(填化学式).?
(2)写出下列反应的离子方程式:B+浓盐酸:______;G+NaOH溶液:______
(3)单质C难以跟冷浓HNO3反应的原因是______.
参考答案:单质C由氧化物A电解生成,且与冷浓硝酸难以反应,应为Al,则A为Al2O3,氧化物B可与浓盐酸在加热条件下反应生成单质,应为实验室制备氯气的反应,则B为MnO2,D为Cl2,
M为AlCl3,由转化关系可知G为Al(OH)3,N为NaAlO2,
(1)由以上分析可知C为Al,D为Cl2,G为Al(OH)3,故答案为:Al;Cl2;Al(OH)3;
(2)MnO2与浓盐酸在加热条件下生成氯气,反应的方程式为MnO2+2Cl-+4H+△.Mn2++Cl2↑+2H2O,Al(OH)3具有两性,可与NaOH反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:MnO2+2Cl-+4H+△.Mn2++Cl2↑+2H2O;Al(OH)3+OH-=AlO2-+2H2O;?
(3)铝与浓硝酸发生钝化反应,在表面生成一层致密的氧化铝膜,可阻止反应进一步进行,故答案为:铝遇冷浓硝酸表面形成致密氧化膜阻止进一步反应而钝化.?
本题解析:
本题难度:一般