��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����100 mL 3 mol��L��1 NaOH��Һ��100 mL 1 mol��L��1��AlCl3��Һ���ٽ�NaOH��Һ�ֶ�μӵ�AlCl3��Һ�С��ڽ�AlCl3��Һ�ֶ�μӵ�NaOH��Һ �У��Ƚ����ֲ�����
�У��Ƚ����ֲ�����
A��������ͬ��������������
B��������ͬ����������Ҳ���
C������ͬ��������������
D������ͬ�������������
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2������� ����������Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO�����ʣ�����ȡ���ֹ��յ��������£�

��ش��������⣺
��1�����̼������������Al3+�ķ���ʽΪ____________________________.
��2�������Ҽ����ռ������SiO32�������ӷ���ʽΪ______________________.
��3����֤��ҺB��Fe3+����ȡ������Һ������________�����Լ����ƣ���
��4����ҺE��K�����ʵ���Ҫ�ɷ���____________(�ѧʽ)��д������Һ��һ����;____________
��5����֪298Kʱ��Mg(OH)2���ܶȻ�����KSP=5.6��10��12��ȡ��������ҺB������һ�������ռ�ﵽ������Һƽ�⣬���PH=13.00������¶��²�������Һ�е�c(Mg2+)=__________________.
�ο��𰸣���1��Al2O3 + 6H+ = 2Al3+ + 3H2O��3�֣�
��2��SiO2 +2OH�� = SiO32�� + H2O��3�֣�
��3�����軯�أ���������ء�������Һ�Ⱥ����𰸣���2�֣�
��4��NaHCO3��1�֣����ƴ���������ͷ۵Ⱥ����𰸣�2�֣�
��5��5.6��10-10mol?L-1��3�֣�
������������������м�������ʱ������Al3+�ķ���ʽΪAl2O3 + 6H+ = 2Al3+ + 3H2O�������ռ�ʱ����SiO32�������ӷ���ʽΪSiO2 +2OH�� = SiO32�� + H2O��Fe3+�ļ�����������軯�ػ���Һ������ҺY��D��ͨ�����������̼ʱ����NaHCO3���������ͷۻ��ƴ����5��298Kʱ����Һ��pH=13.00ʱ��c��OH-��="0.1mol/L," c(Mg2+)=Ksp/c2(OH)= 5.6��10��12/0.01=5.6��10-10mol?L-1.
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ʾ��ʵ������в������������Ӧ��ͼ�β�����ϵ���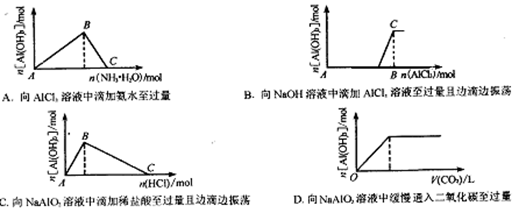
�ο��𰸣�A
���������
A��������������������������������ڰ�ˮ�У�Al3����3NH3��H2O=Al(OH)3��3NH4��������ѡ��A����ȷ���������ȷ�ģ���ѡA��B���ȷ���4OH�D��Al3��=AlO2�D��2H2O��������Al3����3AlO2�D��6H2O="4Al" (OH)3����?C���ȷ�����AlO2�D����H����H2O="Al" (OH)3����������Al(OH)3��3H��=Al3����3H2O��D�����շ�����AlO2�D��CO2��H2O=Al(OH)3����NaHCO3
�����Ѷȣ�һ��
4��ѡ���� �������������彡����ɽϴ�Σ������
[? ]
A����С�մ�(NaHCO3)��������������ͷ
B����ʳ����ϴ��ˮƿ���ڱڸ��ŵ�ˮ��
C����Al(OH)3��������
D����SO2�ӹ�ʳƷʹʳƷ����
�ο��𰸣�D
���������
�����Ѷȣ���
5�������� ��12�֣���ʽ̼����þ[MgaAlb(OH)c(CO3)d��x?H2O]������������ȼ����
��1����ʽ̼����þ������ȼ���ã������������ȷֽ������մ���������?��
��2��MgaAlb(OH)c(CO3)d��x?H2O��a��b��c��d�Ĵ�����ϵʽΪ?��
��3��Ϊȷ����ʽ̼����þ����ɣ���������ʵ�飺
��ȷ��ȡ3.390g��Ʒ������ϡ�����ַ�Ӧ������CO20.560L���ѻ���ɱ�״���£�������ȡһ������Ʒ�ڿ����м��ȣ���Ʒ�Ĺ�������ʣ�������Ʒ��ʣ������/������Ʒ����ʼ������100%�����¶ȵı仯����ͼ��ʾ����Ʒ��2700Cʱ����ȫʧȥ�ᾧˮ��6000C���ϲ�������Ϊ����������Ļ�����
��������ʵ�����ݼ����ʽ̼����þ��Ʒ�е�n(OH��): n(CO32��)��д��������̣���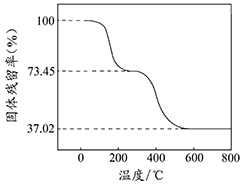
�ο��𰸣�
��ֹȼ��
2a+3b=c+2d
��3��

���������(1�����ȷֽ�Ϊ���۵������þ�������������ڿ�ȼ����棬��ֹȼ�գ���2�������и�Ԫ�صĺϼ۴�����Ϊ0��2a+3b=c+2d����3�����ݷֽ�ͼ�����֪��Ϣ���ó���һ����ʧȥ�ᾧˮ���ڶ����Ƿֽ�Ϊ�����Ӧ���ݺ�һ�μ���OH-��CO32-�Ĺ�ϵ������ʱǰ������ˮ���������ɶ�����̼�����ߵĺͿ��Ը���ͼ�е����ݻ��㣬�ٸ��ݶ�����̼�����������ˮ�������������õ�OH-��CO32-�����ʵ�����
�����Ѷȣ�һ��