��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� п��Һ�������һ�����͵绯ѧ����װ�ã�����ͼ��ʾ�������ҺΪ�廯пˮ��Һ�����Һ�ڵ���ʴ��͵�ؼ䲻��ѭ��������˵������ȷ����
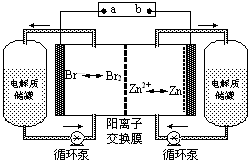
A�����ʱ�缫a���ӵ�Դ�ĸ���
B���ŵ�ʱ�����ĵ缫��ӦʽΪZn��2e��=Zn2+
C���ŵ�ʱ������ʴ����е�������Ũ������
D�������ӽ���Ĥ����ֹBr2��Znֱ�ӷ�����Ӧ
�ο��𰸣�A
�������������ȷ����ŵ�ʱ���ܷ�Ӧ���Է���������ԭ��Ӧ��ΪZn+Br2=ZnBr2���缫aΪ�������缫bΪ����������ʱ�缫a���Դ�������������缫b���Դ�ĸ����������ݴ˿�ȷ��A�����
�����Ѷȣ�һ��
2��ѡ���� ��������ͼʾ��˵������ȷ���ǣ�?��
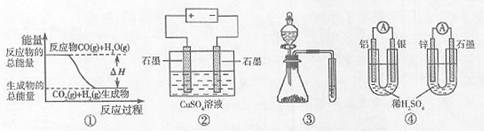
A��ͼ�ٱ�ʾ���淴Ӧ����CO(g)+H2O(g)  CO2(g)+H2(g)���еġ�H����0
CO2(g)+H2(g)���еġ�H����0
B��ͼ��Ϊ�������ͭ��Һ��װ�ã�һ��ʱ���ڣ����缫�������ʵ����ʵ���֮��һ��Ϊ1��1
C��ͼ��ʵ��װ�ÿ���ɱȽ����ᡢ̼�ᡢ��������ǿ����ʵ��
D��ͼ������װ����ͨ�����ߵĵ�������ͬʱ�����ĸ������ϵ����ʵ���Ҳ��ͬ
�ο��𰸣�C
�����������
�����Ѷȣ���
3��ѡ���� ������ȼ�ϵ�ؾ��й�����Ӧ��ǰ����ͨ�������Ͻ���������NaOH��ҺΪ�������Һ������˵����ȷ���ǣ� ? ��
A�������ĵ缫��ӦΪO2+2H2O+2e-=4OH-
B�������ĵ缫��ӦΪAl+3OH---3e-�TAI��OH��3��
C����ع��������У����Һ��pH���ֲ���
D�����ʹ��ʱ��������H2������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� (6��)��1���״�����Ϊȼ�ϵ�ص�ԭ�ϡ���CH4��H2OΪԭ��,ͨ�����з�Ӧ���Ʊ��״���
��:CH4(g)+H2O(g) CO(g)+3H2(g)��H="+206.0" kJ��mol-1
CO(g)+3H2(g)��H="+206.0" kJ��mol-1
��:CO(g)+2H2(g) CH3OH(g)��H="-129.0" kJ��mol-1
CH3OH(g)��H="-129.0" kJ��mol-1
CH4(g)��H2O(g)��Ӧ����CH3OH(g)��H2(g)���Ȼ�ѧ����ʽΪ _____________��
��2���״���ˮ�ʻ����һ������Ⱦ,��һ�ֵ绯ѧ��������������Ⱦ,��ԭ����:ͨ���,��Co2+ ������Co3+,Ȼ����Co3+ ����������ˮ�еļ״�������CO2��������ʵ��������ͼװ��ģ����������:
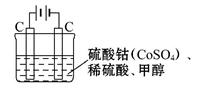
��д�������缫��Ӧʽ _______ ��
��д��Co3+��ȥ�״������ӷ���ʽ ��
�ο��𰸣�(6��) ��1�� CH4(g)+H2O(g) CH3OH(g)+H2(g) ��H="+77.0" kJ��mol-1
CH3OH(g)+H2(g) ��H="+77.0" kJ��mol-1
��2����Co2+ �� e-  Co3+ ��6Co3++CH3OH+H2O
Co3+ ��6Co3++CH3OH+H2O CO2��+6Co2++6H+
CO2��+6Co2++6H+
�����������1�����ݸ�˹���ɣ�I+II�ɵ�������Ȼ�ѧ����ʽ������CH4(g)��H2O(g)��Ӧ����CH3OH(g)��H2(g)���Ȼ�ѧ����ʽΪCH4(g)+H2O(g) CH3OH(g)+H2(g) ��H="+77.0" kJ��mol-1��
CH3OH(g)+H2(g) ��H="+77.0" kJ��mol-1��
��2������������������Ӧ����Co2+ ��������Co3+,�缫��ӦʽΪCo2+ �� e-  Co3+��
Co3+��
��Co3+ ����������ˮ�еļ״�������CO2�������������ֱ���ԭΪCo2+������Co3+��ȥ�״������ӷ���ʽ��6Co3++CH3OH+H2O CO2��+6Co2++6H+��
CO2��+6Co2++6H+��
���㣺�������ӷ���ʽ����д����˹���ɵ�Ӧ��
�����Ѷȣ�һ��
5��ѡ���� ���й��ڻ�ѧ��ת��Ϊ���ܵ�����װ�õ�˵����ȷ����
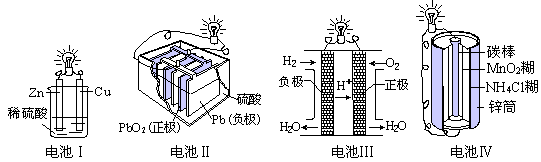
A����آ���п������
B����آ���һ���Ե��
C����آ���ʱ������������ԭ��Ӧ
D����آ�����ʱ��������пͨ����������̼��
�ο��𰸣�D
���������A��ԭ����нϻ��õĽ����������������õĽ�����������п��ͭ���ã������װ��I��п�Ǹ�����ͭ��������A����ȷ��B��Ǧ�����ǿɳ���أ����ڶ��ε�أ�B����ȷ��C��������ȼ�ϵ���������ڸ���ͨ�룬����������Ӧ������������ͨ�룬������ԭ��Ӧ��C����ȷ��D���ڸɵ����пͲ�Ǹ�����̼�������������Ե�آ�����ʱ��������пͨ����������̼����D��ȷ����ѡD��
�����Ѷȣ�һ��