微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图。 请回答下列问题

(1)电极X的材料是___________;电解质溶液Y是_____________;
(2)银电极为电池的_______极,发生的电极反应为_____________________; X电极上发生的电极反应为_________________;
(3)外电路中的电子是从____________电极流向___________电极。
参考答案:(1)Cu;AgNO3
(2)正极;Ag++e-==Ag↓;Cu-2e-==Cu2+
(3)X;Ag
本题解析:
本题难度:一般
2、选择题 (2014届江苏省南通市高三第二次调研化学试卷)
如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是
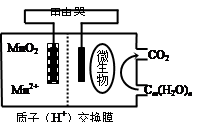
A.分子组成为Cm(H2O)n的物质一定是糖类
B.微生物所在电极区放电时发生还原反应
C.放电过程中,H+从正极区移向负极区
D.正极反应式为:MnO2+4H++2e―=Mn2++2H2O
参考答案:D
本题解析:
A、原先认为糖均为碳水化合物,符合上式,但后来发现许多糖不符合该式,如鼠李糖(C6H12O5)、脱氧核糖(C5H10O4)等,也有符合该式的不是糖,如甲醛、乙酸(C2H4O2)、乳酸(C3H6O3)等错误;B、微生物放电,糖中碳元素化合价升高失去电子,为负极发生氧化反应,错误;C、原电池中阴离子向负极移动,阳离子向正极移动,错误;D、正确。
本题难度:一般
3、选择题 一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是(?)
A.CH3OH(g)+O2(g)-2e-=H2O(l)+CO2(g)+2H+(aq)
B.O2(g)+4H+(aq)+4e-=2H2O(l)
C.CH3OH(g)+H2O(l)-6e-=CO2(g)+6H+(aq)
D.O2(g)+2H2O(l)+4e-=4OH-
参考答案:C
本题解析:首先写出该燃料电池的总反应式:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l),然后分析化合价变化,确定氧化反应、还原反应及负正极。因为负极发生氧化反应,故反应式为:2CH3OH(g)+2H2O(l)-12e-=2CO2(g)+12H+(aq);正极发生还原反应,反应式为:3O2(g)+12H+(aq)+12e-=6H2O (l)。
本题难度:一般
4、填空题 某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是________________
(2)实验室中现有Na2SO4、CuCl2、MgSO4、K2SO4等4种溶液,可与上述实验中CuSO4
溶液起相似作用的是________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有________________(答两种)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,
收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
| A
| B
| C
| D
| E
| F
|
4mol/L H2SO 4/mL
| 30
| V1
| V2
| V3
| V4
| V5
|
饱和CuSO4溶液 /mL
| 0
| 0.5
| 2.5
| 5
| V6
| 20
|
H2O /mL
| V7
| V8
| V9
| V10
| 10
| 0
|
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
② 该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
参考答案:(1) CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn微电池,加快了氢气产生的速率 (2分)
(2) CuCl2、(1分)
(3)升高反应温度、适当增大硫酸的浓度、或增加锌的比表面积等(2分)
(4)①30 10 17.5 (3分)
②当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积(2分)
本题解析:CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn微电池,加快了氢气产生的速率,因此能起到相似作用的应该是含有铜离子的,所以为氯化铜。影响化学反应速率的因素有,温度,催化剂,浓度,压强,反应物的接触面积。AB应比较的是硫酸铜溶液对该反应的影响。因此硫酸的量应与A的相同,所以V1=30 据表格可知,CDEF应该是呈两倍的关系递增,所以V6="10" 。从图表可知饱和硫酸铜的体积与水的体积之和应为20毫升。所以V9应为20减去2.5等于17.5. :当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降主要是由于当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积
考点:考查影响化学反应速率因素的相关知识。
本题难度:一般
5、选择题 (08年成都诊断,11)右图中,两电极上发生的电极反应如下:a极: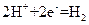 ↑,
↑,
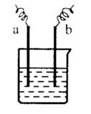
b极: -2
-2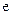 =
= 。则以下说法不正确的是(?)
。则以下说法不正确的是(?)
A.该装置可能是电解池
B.该装置中电解质溶液pH可能等于7
C.a、b可能是同种电极材料
D.该过程中能量的转换一定是化学能转化为电能
参考答案:D
本题解析:本题考查原电池和电解池,较难题。该装置为原电池时,则b为负极,材料为Zn,a为正极,材料为活动性比Zn弱的金属,电解质溶液为非氧化性酸溶液;该装置为电解池时,b极为阳极,材料为Zn,a极为阴极,材料可为活性电极或惰性电极,电解质溶液为活泼金属的盐溶液。因此该装置既可能为原电池,也可能为电解池,A对,D错;该装置为电解池时,电解质为NaCl时,pH=7,B对;该装置为电解池时,电极材料均可为Zn,C对。
本题难度:一般