微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据化学平衡知识,判断下列 说法正确的是(?)
说法正确的是(?)
A.已知NaHA溶液呈弱碱性,则该溶液中下列各种微粒浓度大小排列顺序为:
c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.在小苏打溶液中存在下列关系:c(HCO3-)=c(Na+)-c (CO32-)-c(H2CO3)
C.向AgCl悬浊液中加入足量的NaI溶液,无明显现象产生
D.常温下,稀释0.1 mol/L的氨水,溶液中所有离子浓度均下降
参考答案:B
本题解析:略
本题难度:一般
2、选择题 用物质的量均是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是(?)
A.c(CH3COOH)>c(CH3COO-)
B.c(CH3COO-)+c(CH3COOH)=0.1 mol・L-1
C.c(H+)>c(OH-)
D.c(CH3COO-)+c(OH-)=0.1 mol・L-1
参考答案:C
本题解析:c(CH3COO-)大于c(Na+),所以根据电荷守恒定律可知,溶液显酸性。这说明醋酸的电离程度大于醋酸钠的水解程度,因此C正确,A不正确,应该是c(CH3COOH)<c(CH3COO-) ;B不正确,应该是c(CH3COO-)+c(CH3COOH)=0.2 mol・L-1;D不正确,应该是c(CH3COO-)+c(OH-)>0.1 mol・L-1,所以答案选C。
本题难度:一般
3、选择题 下列水解的离子方程式正确的是
A.S2-+2H2O H2S+2OH-
H2S+2OH-
B.Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.CO32-+H2OHCO3-+OH-
D.HS-+H2O H2S↑+OH-
H2S↑+OH-
参考答案:B
本题解析:A、S2?分步水解,错误;B、Fe3+水解生成Fe(OH)3和H+,正确;C、CO32?部分水解,应该用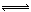 ,错误;D、HS?微弱水解,生成少量H2S,不能用↑符号,错误。
,错误;D、HS?微弱水解,生成少量H2S,不能用↑符号,错误。
本题难度:一般
4、实验题 (8分)Ⅰ.(1)饱和氯化铵溶液显酸性,原因是
________________________________________________________________________
________________________________________________________________________;
向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解;其合理的解释(用相关离子方程式表示)为
________________________________________________________________________
________________________________________________________________________。
(2)向Mg(OH)2悬浊液中加入适量CH3COONH4溶液,
Mg(OH)2能否完全溶解________(填“能”或“否”),理由是
________________________________________________________________________
________________________________________________________________________。
Ⅱ.硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4===H++HSO4-,HSO4-===H++SO42-。
请回答下列有关问题:
(1)Na2SO4溶液呈________(填“弱酸性”“中性”或“弱碱性”),其理由是________________________________________________________________________
(用离子方程式表示);
(2)H2SO4溶液与BaCl2溶液反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)在0.10 mol・L-1的Na2SO4溶液中,下列离子浓度关系正确的是________(填写编号);
A.c(Na+)=c(SO42-)+c(HSO4-)+c(H2SO4)
B.c(OH-)=c(HSO4-)+c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-)
D.c(Na+)=2c(SO42-)+2c(HSO4-)