微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)下表是元素周期表的一部分,完成以下有关问题。
周期
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0
|
2
| ?
| ?
| ?
| ①
| ②
| ③
| ④
| ?
|
3
| ⑤
| ?
| ⑥
| ⑦
| ?
| ⑧
| ⑨
| ⑩
|
(1)在①~⑩元素中,最不活泼的元素是_____(写元素符号,下同);最高价氧化物对应的水化物的酸性最强的元素是?,最高价氧化物对应的水化物的碱性最强的元素是?。
(2)②、③、④的氢化物中最稳定是?(填该氢化物化学式)。
( 3)④⑤⑥的原子半径从大到小的顺序是?>?>?(写元素符号) 。
(4)①的一种氢化物的产量是衡量一个国家石油化学工业发展水平的标志,该氢化物与⑨的氢化物反应的化学方程式为?。
参考答案:(1)Ar? Cl? Na? (2)HF (3) Na>Al>F
 ?
?
(4)CH2=CH2+HCl? CH3CH2Cl
本题解析:略
本题难度:简单
2、选择题 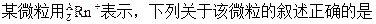
A.所含质子数=A-n
B.所含中子数=A-Z
C.所含电子数=Z+n
D.质量数=Z+A
参考答案:B
本题解析:①质量数=质子数+中子数
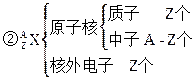
所以该微粒的质子数=Z,电子数=Z-n,质量数=A,中子数=A-Z,则B正确。
本题难度:一般
3、选择题 人类探测月球发现,月球上有大量3He存在,它可以作为未来核聚变的重要原料之一,以下关于3He的说法正确的是(?)
A.是4He的同素异形体
B.比4He多一个中子
C.是4He的同位素
D.比4He少一个质子
参考答案:C
本题解析:略
本题难度:简单
4、实验题 (12分)氢气、纳米技术制成的金属燃料、非金属固体燃料已应用到社会生活和高科技领域。
⑴已知短周期金属元素A和B,其单质单位质量的燃烧热大,可用作燃料。其原子的第一至第四电离能如下表所示:
电离能(kJ/mol)
| I1
| I2
| I3
| I4
|
A
| 899.5
| 1757.1
| 14848.7
| 21006.6
|
B
| 738
| 1451
| 7733
| 10540
|
①根据上述数据分析, B在周期表中位于?区,其最高价应为?;
②若某同学将B原子的基态外围电子排布式写成了ns1np1,违反了?原理;
③B元素的第一电离能大于Al,原因是 ;
⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由?。
②C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子相对稳定结构,则C60分子中σ键与π键的数目之比为?。
参考答案:(12分)
⑴① s +2 (各2分) ②能量最低原理 (2分)?③镁原子3s轨道全充满,能量较低(2分)
⑵①不正确? C60是分子晶体,熔化时不需破坏化学键?(2分) ②3∶1 ?(2分)
本题解析:略
本题难度:简单
5、选择题 下列关于元素周期表的说法正确的是(?)
A.能生成碱的金属元素都在ⅠA族
B.原子序数为14的元素位于元素周期表的第3周期ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.最外层电子数是次外层电子数的2倍的原子容易失去电子成为阳离子
参考答案:B
本题解析:A、因ⅡA族的金属元素也能生成碱,如氢氧化镁,故A错误;
B、原子序数为14的原子为硅,有三个电子层,每一层的电子数分别为2、8、4,所以位于元素周期表的第3周期ⅣA族,故B正确;
C、因氦原子的最外层电子数为2,故C错误;
D、最外层电子数是次外层电子数的2倍的原子,比如碳,很稳定,故D错误;
故选:B。
点评:本题考查长式元素周期表的结构,要求学生对元素周期表的组成特点要熟悉,周期表中周期与周期之间,族与族之间含有较多规律,在学习中要善于抓住这些规律会起到事半功倍的效果。
本题难度:简单