微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用石墨作电极电解2 mol・L-1的NaCl和1 mol・L-1的MgSO4混合溶液时,下列曲线合理的是 ( )
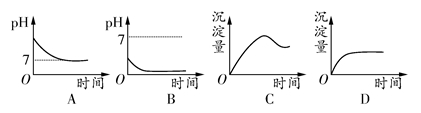
参考答案:D
本题解析:依据2NaCl+2H2O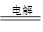 2NaOH+H2↑+Cl2↑ MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,溶液起始及最终的pH均接近于7,沉淀量从起始至最终应是先逐渐增加,后期保持不变。故D项正确。
2NaOH+H2↑+Cl2↑ MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,溶液起始及最终的pH均接近于7,沉淀量从起始至最终应是先逐渐增加,后期保持不变。故D项正确。
本题难度:一般
2、选择题 下列描述中正确的是(?)
A.电解法制镁时一般是用熔融态的氯化镁进行电解,但也可用氯化镁溶液
B.电解法生产铝时,可用钢网代替碳棒作阳极增大接触面积
C.我国第五套人民币中的一元硬币材料为钢芯镀镍,在硬币制作时,钢芯应做阴极
D.用电解法制备高纯度的镍,粗镍做阴极,精镍作阳极,阳极质量的减少与阴极质量的增加相等
参考答案:C
本题解析:略
本题难度:简单
3、填空题 请分析下列有关铝盐溶液电解时的变化情况。
(1)用石墨作电极,用如图装置电解AlCl3溶液,两极均产生气泡,阴极区有沉淀生成。持续电解,在阴极附近的溶液中还可观察到的现象是 ,解释此现象的离子方程式是 。
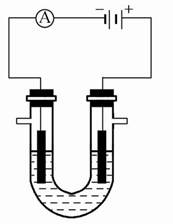
(2)若用石墨作电极电解NaCl和Al2(SO4)3的混合溶液,混合溶液中二者的物质的量浓度分别为3 mol・L-1、0.5 mol・L-1,则下列表示电解过程的曲线正确的是 。

参考答案:(1)白色沉淀逐渐溶解至消失 Al(OH)3+OH-=AlO2-+2H2O
(2)A、D
本题解析:(1)用惰性电极电解AlCl3溶液,起始时总反应方程式可表示为2AlCl3+6H2O  2Al(OH)3↓+3Cl2↑+3H2↑,阴极区产物为Al(OH)3和H2,故阴极区有白色沉淀Al(OH) 3生成,随着电解的进行,AlCl3消耗完,这时相当于电解水,阴极上H+放电,导致阴极区碱性增强,之前生成的Al(OH)3又慢慢溶解,离子方程式可表示为Al(OH)3+OH-=AlO2-+2H2O。
2Al(OH)3↓+3Cl2↑+3H2↑,阴极区产物为Al(OH)3和H2,故阴极区有白色沉淀Al(OH) 3生成,随着电解的进行,AlCl3消耗完,这时相当于电解水,阴极上H+放电,导致阴极区碱性增强,之前生成的Al(OH)3又慢慢溶解,离子方程式可表示为Al(OH)3+OH-=AlO2-+2H2O。
(2)本题是对混合溶液的电解,可对4种离子进行重新组合,由题知,电解NaCl和Al2(SO4)3的混合溶液相当于电解1 mol・L-1 AlCl3溶液,电解过程中总反应式可表示为2AlCl3+6H2O 2Al(OH)3↓+3H2↑+3Cl2↑,由此可知选项A、D正确。
2Al(OH)3↓+3H2↑+3Cl2↑,由此可知选项A、D正确。
本题难度:一般
4、选择题 用铂作电极电解某金属氯化物MCln的水溶液,当阳极产生a mol气体时,阴极析出m g金属,则金属的相对原子质量是:
A.
B.
C.
D.
参考答案:C
本题解析:用铂作电极电解氯化物水溶液,阳极反应为2Cl--2e-=Cl2↑,阴极反应为Mn++ne-=M,由阴阳两极转移电子数相等得:nCl2~2M,n:2=a:(m/M),M= 。
。
点评:电解池中阴阳两极转移电子数相等。
本题难度:一般
5、选择题 碘被称为“智力元素”,科学合理地补碘可防止碘缺乏症.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.以碘为原料,通过电解可以制备碘酸钾.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却(实验装置如右图所示).以下有关该实验的说法错误的是( )
A.碘是紫黑色固体物质,实验室常用升华法来分离提纯含有少量杂质的固体碘
B.电解时,阳极上发生反应的电极反应式为I-+6OH--6e-=IO3-+3H2O
C.通过离子交换膜的K+离子的运动方向是从右向左
D.当有3mol电子发生转移时,其中被还原生成的KIO3的物质的量为0.5mol