微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。由于该反应是吸热反应,所以在情况下有利于该反应自发进行
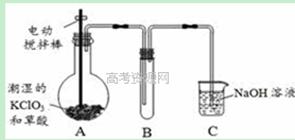
(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式: 。
(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、 ;B装置必须放在冰水浴中,其原因是 。
(3)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2・3H2O,在温度高于38℃时析出晶体是NaClO2。请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:① ;② ;③洗涤;④干燥。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知2 Na2S2O3 + I2=Na2S4O6 + 2NaI)
①配制100 mL c mol/LNa2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有: 。
②写出步骤2中发生反应的离子方程式 。
③原ClO2溶液的浓度为 g / L(用步骤中的字母代数式表示)。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 。
若滴定开始仰视读数,滴定终点时正确读数,则测定结果 。
(填“偏高”“偏低”或“不变” )
参考答案:(1)2KClO3+H2C2O4 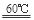 K2CO3+CO2↑+2ClO2↑+H2O;
K2CO3+CO2↑+2ClO2↑+H2O;
(2)温度计; 使ClO2充分冷凝,减少挥发;
(3)①蒸发结晶(,写蒸发、浓缩、结晶均给分);②趁热过滤;
(4) ① 100ml 容量瓶、胶头滴管;②2ClO2 + 10I- + 8H+ = 2Cl- + 5I2 + 4H2O;
③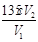 ;④偏高;偏低。
;④偏高;偏低。
本题解析:(1)根据已知信息可得方程式为:2KClO3+H2C2O4 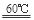 K2CO3+CO2↑+2ClO2↑+H2O;(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯和温度计;B装置必须放在冰水浴中,是为了使ClO2充分冷凝,减少挥发;(3)由于NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2・3H2O,在温度高于38℃时析出晶体是NaClO2,所以从NaClO2溶液中制得NaClO2晶体的操作步骤是①蒸发结晶,然后②趁热过滤;③洗涤;④干燥。从而得到NaClO2晶体。(4)①配制100 mL c mol/LNa2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有100ml 容量瓶、胶头滴管;②ClO2有氧化性,而I-有还原性,二者在酸性条件下发生氧化还原反应。根据电子守恒、原子守恒可知:步骤2中发生反应的离子方程式为2ClO2 + 10I- + 8H+ = 2Cl- + 5I2 + 4H2O;③由方程式得关系式为2ClO2~5I2~10Na2S2O3。n(Na2S2O3)=" c" mol/L×V2×10-3L,所以稀释后的V1 mL溶液中含有的ClO2的物质的量为2 cV2×10-4mol.则原溶液10ml即稀释后的100m的溶液中含有的ClO2的物质的量为(2 cV2÷ V1)×10-2mol.故原溶液的浓度为:c(ClO2)= (2 cV2÷V1)×10-2mol÷0.01L=(2 cV2÷V1)mol/L=
K2CO3+CO2↑+2ClO2↑+H2O;(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯和温度计;B装置必须放在冰水浴中,是为了使ClO2充分冷凝,减少挥发;(3)由于NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2・3H2O,在温度高于38℃时析出晶体是NaClO2,所以从NaClO2溶液中制得NaClO2晶体的操作步骤是①蒸发结晶,然后②趁热过滤;③洗涤;④干燥。从而得到NaClO2晶体。(4)①配制100 mL c mol/LNa2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有100ml 容量瓶、胶头滴管;②ClO2有氧化性,而I-有还原性,二者在酸性条件下发生氧化还原反应。根据电子守恒、原子守恒可知:步骤2中发生反应的离子方程式为2ClO2 + 10I- + 8H+ = 2Cl- + 5I2 + 4H2O;③由方程式得关系式为2ClO2~5I2~10Na2S2O3。n(Na2S2O3)=" c" mol/L×V2×10-3L,所以稀释后的V1 mL溶液中含有的ClO2的物质的量为2 cV2×10-4mol.则原溶液10ml即稀释后的100m的溶液中含有的ClO2的物质的量为(2 cV2÷ V1)×10-2mol.故原溶液的浓度为:c(ClO2)= (2 cV2÷V1)×10-2mol÷0.01L=(2 cV2÷V1)mol/L=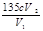 g/L. ④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则消耗的Na2S2O3体积偏大,使得测定结果偏高;若滴定开始仰视读数,开始读数偏大,滴定终点时正确读数,则消耗的Na2S2O3体积偏小,测定结果偏低。
g/L. ④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则消耗的Na2S2O3体积偏大,使得测定结果偏高;若滴定开始仰视读数,开始读数偏大,滴定终点时正确读数,则消耗的Na2S2O3体积偏小,测定结果偏低。
考点:考查化学反应原理、仪器的使用、物质的制取、误差分析、化学方程式和离子方程式的书写、浓度的计算的知识。
本题难度:一般
2、填空题 向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式: 。
(2)下列三种情况下,离子方程式与 (1)相同的是 (填序号)。
A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
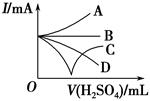
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的 (填序号)曲线表示。
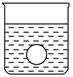
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示。向该烧杯中缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。
参考答案:(1)Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O (2)A (3)C (4)下沉
本题解析:(1)向Ba(OH)2溶液中逐滴加入稀硫酸,反应的离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O。(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性,反应的离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,离子方程式为:Ba2++OH-+SO42-+H+=BaSO4↓+H2O;向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量,反应的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O。(3)向Ba(OH)2溶液中缓缓加入稀硫酸,当Ba(OH)2与H2SO4恰好完全反应时,溶液导电能力接近为零,再加过量稀硫酸,溶液导电能力又增强,故曲线C正确。(4)Ba(OH)2与H2SO4反应过程中,随反应的进行,溶液密度变小,塑料小球下沉。
本题难度:一般
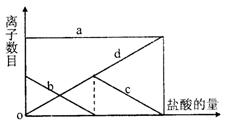
3、选择题 向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
| a
| b
| c
| d
|
A
| Cl―
| K+
| CO32―
| HCO3―
|
B
| K+
| CO32―
| Cl―
| HCO3―
|
C
| K+
| CO32―
| HCO3―
| Cl―
|
D
| K+
| HCO3―
| Cl―
| CO32―
|
参考答案:C
本题解析:因向一定量的K2CO3溶液中缓慢地滴加稀盐酸,先后发生如下反应:K2CO3+HCl
本题难度:一般
4、填空题 (8分)已知: 2Fe2+ + Br2=2Fe3++2Br-;Cl2+2Br-= Br2+2Cl-
在含n mol FeBr2的溶液中,通入Cl2,有x mol Cl2发生反应。
(1)当 时,反应的离子方程式为_________________________
时,反应的离子方程式为_________________________
(2)当反应的离子方程式为:3Cl2+2Fe2+ +4Br-=2Br2+2Fe3+ +6Cl-时,x与n的关系为_____
(3)当Fe2+和Br-同时被氧化时,x与n的关系是_______________
(4)当x=n时,反应后氧化产物的物质的量为________________
参考答案:2Fe2+ + Cl2 = 2Fe3+ + 2Cl-;(2) ;(3)
;(3)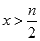 (4)
(4)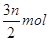 或
或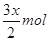
本题解析:(1)2Fe2+ + Br2=2Fe3++2Br-,说明亚铁离子的还原性大于溴离子的还原性,向FeBr2溶液中通入氯气,氯气先和亚铁离子先发生置换反应2Fe2+ + Cl2 = 2Fe3+ + 2Cl-,然后再和溴铁离子发生反应,答案为2Fe2+ + Cl2 = 2Fe3+ + 2Cl-;(2)所以在含有n molFeBr2的溶液中通入Cl2,有x molCl2发生反应,当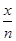 ≥
≥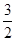 时,溴离子离子、二价铁离子全部被氧化;(3)
时,溴离子离子、二价铁离子全部被氧化;(3)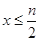 时只氧化亚铁离子,当
时只氧化亚铁离子,当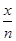 >
>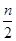 时,不但能氧化亚铁离子还氧化溴离子,故答案为
时,不但能氧化亚铁离子还氧化溴离子,故答案为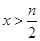 ;(4)x=n时,反应中先氧化全部亚铁离子,n molFeBr2的溶液中含有nmol的亚铁离子,消耗
;(4)x=n时,反应中先氧化全部亚铁离子,n molFeBr2的溶液中含有nmol的亚铁离子,消耗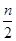 氯气,剩余
氯气,剩余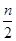 氯气又与溴离子发生Cl2+2Br-= Br2+2Cl-,生成
氯气又与溴离子发生Cl2+2Br-= Br2+2Cl-,生成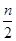 molBr2,故氧化产物为Fe3+和Br2,物质的量为
molBr2,故氧化产物为Fe3+和Br2,物质的量为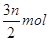 ,故答案为
,故答案为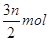 或
或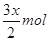
考点:氧化还原反应
本题难度:一般
5、选择题 仔细分析下列实验:
实验1: 实验2:

A、B、C试管中的现象如下表所示:
A
| B
| C
|
产生白色沉淀,溶液仍为蓝色
| 产生蓝色沉淀,溶液变为无色
| 产生蓝色沉淀,溶液为无色
|
写出A、B、C试管中发生反应的离子方程式。
(1)A: ;
(2)B: ;
(3)C: 。
参考答案:(1)Ba2++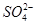 ====BaSO4↓ (2)Cu2++2OH-====Cu(OH)2↓
====BaSO4↓ (2)Cu2++2OH-====Cu(OH)2↓
(3)Ba2++Cu2++2OH-+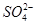 ====BaSO4↓+Cu(OH)2↓
====BaSO4↓+Cu(OH)2↓
本题解析:BaCl2溶液和CuSO4溶液混合Ba2+和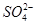 结合成BaSO4白色沉淀,Cu2+和Cl-不反应,所以溶液仍然呈现蓝色;向A试管中得到的滤液中加入NaOH溶液,Cu2+和OH-反应结合成Cu(OH)2蓝色沉淀。Ba(OH)2溶液和CuSO4溶液混合,Cu2+和OH-反应结合成Cu(OH)2蓝色沉淀,Ba2+和
结合成BaSO4白色沉淀,Cu2+和Cl-不反应,所以溶液仍然呈现蓝色;向A试管中得到的滤液中加入NaOH溶液,Cu2+和OH-反应结合成Cu(OH)2蓝色沉淀。Ba(OH)2溶液和CuSO4溶液混合,Cu2+和OH-反应结合成Cu(OH)2蓝色沉淀,Ba2+和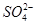 结合成BaSO4白色沉淀,发生两个离子反应,生成两种沉淀。
结合成BaSO4白色沉淀,发生两个离子反应,生成两种沉淀。
考点:离子反应
本题难度:一般