微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向明矾[KAl(SO4)2?12H2O]溶液中滴加Ba(OH)2溶液,当SO42-完全沉淀时,铝元素的存在形式是 (?)?
A.全部为Al(OH)3沉淀
B.几乎全部以[Al(OH)4]-形式存在于溶液中
C.一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中
D.一部分为Al(OH)3沉淀,一部分以[Al(OH)4]-形式存在于溶液中
参考答案:B
本题解析:4)2?12H2O,设明矾为1mol,则溶液中含有1molAl3+,2molSO42-,由反应SO42-+Ba2+=BaSO4↓可知,使SO42-全部转化成BaSO4沉淀,需要2molBa(OH)2,则加入4molOH-,则发生Al3++4OH-=[Al(OH)4]-,所以最后溶液中存在[Al(OH)4]-,所以向明矾[KAl(SO4)2?12H2O]溶液中滴加Ba(OH)2溶液,当SO42-完全沉淀时,铝元素的存在形式是几乎全部以[Al(OH)4]-形式存在于溶液中,故本题的答案选择B。
点评:本题考查了铝及其化合物,该考点是高考考查的重点和难点,本题难度中等。
本题难度:一般
2、选择题 欲将混合液中Al3+、Cu2+、Ba2+、Ag+逐一沉淀出来加以分离,加入试剂?①Cl-?②SO42-?③OH-?④CO2?⑤CO32-的正确顺序是
[? ]
A.①②③④?
B.③⑤①②?
C.②①③⑤?
D.①⑤③②
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是?(?)?
选项
| 离子组
| 加入试剂
| 加入试剂后发生反应的离子方程式
|
A
| Fe2+、NO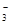 、K+ 、K+
| 稀硫酸
| 3Fe2++NO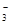 +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O
|
B
| Fe3+、I-、ClO-
| 氢氧化钠溶液
| Fe3++3OH-=Fe(OH)3↓
|
C
| Ba2+、HCO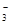 、Cl- 、Cl-
| 氢氧化钠溶液
| HCO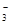 + OH-=CO + OH-=CO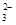 +H2O +H2O
|
D
| Al3+、Cl-、NO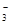
| 过量氢氧化钠溶液
| Al3++3 OH-=Al(OH)3↓
参考答案:A
本题解析:A、Fe2+、NO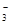 、K+可以大量共存,加入稀硫酸后,溶液中相当于存在稀硝酸,与Fe2+发生氧化还原反应生成Fe3+、NO,离子方程式符合书写原则,正确;B、Fe3+、ClO-与I-因发生氧化还原反应不能大量共存,错误;C、Ba2+、HCO 、K+可以大量共存,加入稀硫酸后,溶液中相当于存在稀硝酸,与Fe2+发生氧化还原反应生成Fe3+、NO,离子方程式符合书写原则,正确;B、Fe3+、ClO-与I-因发生氧化还原反应不能大量共存,错误;C、Ba2+、HCO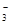 、Cl-可以大量共存,加入氢氧化钠溶液后,OH-与Ba2+、HCO 、Cl-可以大量共存,加入氢氧化钠溶液后,OH-与Ba2+、HCO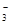 反应生成碳酸钡沉淀,离子方程式书写错误;D、Al3+、Cl-、NO 反应生成碳酸钡沉淀,离子方程式书写错误;D、Al3+、Cl-、NO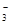 可以大量共存,加入过量氢氧化钠溶液,Al3+与3OH-反应生成AlO2-而不是Al(OH)3沉淀,错误,答案选A。 可以大量共存,加入过量氢氧化钠溶液,Al3+与3OH-反应生成AlO2-而不是Al(OH)3沉淀,错误,答案选A。
本题难度:一般
4、选择题 把过氧化钠投入含有HCO3?-、Cl-、Mg2+、Na+的水溶液中,离子数目不变的是
A.HCO3?-
B.Cl-
C.Mg2+
D.Na+
参考答案:B
本题解析:试题分析:过氧化钠与水反应生成了氢氧化钠,所以过氧化钠投入含有HCO3?-、Cl-、Mg2+、Na+的水溶液,得高的是强碱性的溶液,而HCO3?-、Mg2+不能在强碱性溶液中存在,所以其离子的数目减少,发生了变化,过氧化钠与水反应生成了氢氧化钠,使得钠离子的数目变多,而Cl-的数目不变故本题的答案选择B。
考点:离子共存
点评:本题考查了离子共存的知识,该知识高考考查的重点和难度,本题要注意的是题干中的要求--离子数目不变的是,若离子减少或者是增多都不可以选。
本题难度:简单
5、选择题 已知某溶液中存在较多的H+和SO42-,则该溶液中还可以大量共存的离子组是
A.Al3+、CO32-、Cl-
B.Mg2+、Ba2+、Cl-
C.Mg2+、Fe2+、NO3-
D.Na+、NH4+、Cl-
参考答案:D
本题解析:分析:溶液中存在较多的H+和SO42-,再利用离子之间不能结合生成沉淀、水、气体,不能发生氧化还原反应,不能发生相互促进水解的反应来分析.
解答:A、因H+和CO32-结合生成水和气体,且Al3+、CO32-相互促进水解,则该组离子不能大量共存,故A错误;
B、因Ba2+、SO42-,能结合生成硫酸钡沉淀,则该组离子不能大量共存,故B错误;
C、因H+和Fe2+、NO3-能发生氧化还原反应,则该组离子不能大量共存,故C错误;
D、因该组离子之间不反应,则能够大量共存,故D正确;
故选D.
点评:本题考查离子的共存问题,熟悉复分解反应发生的条件、氧化还原反应、水解等知识可解答,难度不大.
本题难度:一般
|