��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 25�桢101kPa�£�̼�������ͼ����ȼ����������393.5 kJ��mol��1��285.8 kJ��mol��1
��890.3kJ��mol��1������ѡ������ȷ����
A��2H2(g)��O2(g)��2H2O(l)��H����285.8kJ��mol��1
B��CH4(g)��2O2(g)��CO2(g)��2H2O(l)��H��+890.3kJ��mol��1
C��H2(g)��1/2O2(g)��H2O(g)��H����285.8kJ��mol��1
D��C(s)��2H2(g)��CH4(g)��H����74.8 kJ��mol��1
�ο��𰸣�D
���������ȼ������ָ1mol��������ȫȼ�������ȶ���������ų�����������ʾȼ���ȵ��Ȼ�ѧ����ʽ�п�ȼ��Ϊ1mol������Ϊ�ȶ������̼���ʡ�������������Ȼ�ѧ����ʽ�ֱ�Ϊ����C��S��+O2��g���TCO2��g����H=��393.5kJ��mol��1����H2��g��+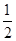 O2��g���TH2O��l����H=��285.8kJ��mol��1����CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=��890.3kJ��mol��1�����ݸ�˹���ɽ��2H2(g)��O2(g)��2H2O(l)?��H����571.6kJ��mol��1��Aѡ�������ȼ���Ƿ��ȣ�Ӧ���ǡ�H����890.3kJ��mol��1��Bѡ�����Һ̬ˮ��Ϊ��̬ˮ��Ҫ����һ�������������ԡ�H>��285.8kJ��mol��1��Cѡ������ݸ�˹���ɢ�-����+�ڡ�2����CH4��g��=C��S��+2H2��g�����ʡ�H=��-890.3KJ��mol��1��-[��-393.5KJ��mol��1��+��-285.8kJ��mol��1����2]=+74.8KJ��mol��1��Dѡ����ȷ��
O2��g���TH2O��l����H=��285.8kJ��mol��1����CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=��890.3kJ��mol��1�����ݸ�˹���ɽ��2H2(g)��O2(g)��2H2O(l)?��H����571.6kJ��mol��1��Aѡ�������ȼ���Ƿ��ȣ�Ӧ���ǡ�H����890.3kJ��mol��1��Bѡ�����Һ̬ˮ��Ϊ��̬ˮ��Ҫ����һ�������������ԡ�H>��285.8kJ��mol��1��Cѡ������ݸ�˹���ɢ�-����+�ڡ�2����CH4��g��=C��S��+2H2��g�����ʡ�H=��-890.3KJ��mol��1��-[��-393.5KJ��mol��1��+��-285.8kJ��mol��1����2]=+74.8KJ��mol��1��Dѡ����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ����
A����Һ��pHֵԽС����Һ�к��е�����������Խ��
B�����ʵ�ˮ��ҺŨ��Խ�ߣ�����Һ���ܶ�Խ��
C�����ʵĻ�ѧ���Խǿ��������ҲԽǿ
D����ͬ����ʱ������Խ�����ᣬ���Ӧ�����ε�ˮ��Һ����Խǿ
�ο��𰸣�A
�����������Һ��pHֵԽС����Һ�������ӵ�Ũ�Ⱦ�Խ������������һ��Խ��ѡ��A����ȷ��B����ȷ�����簱ˮ��Ũ��Խ����Һ���ܶ���ԽС�ģ�C����ȷ�����ʵĻ�ѧ���Խǿ���ǿ����ǻ�ԭ��Խǿ����Խ������Ӧ�����ξ�Խ����ˮ�⣬��Һ�ļ��Ծ�Խǿ��ѡ��D��ȷ����ѡD��
�����Ѷȣ�һ��
3��ѡ���� �����и���������ָ����Һ�У�һ���ܴ����������
A�������£�pH=1����Һ�У� Na����Fe3����NO3����I��
B��ˮ�����H��Ũ��Ϊ1��10��13mol��L��1����Һ�У�K����Al3����Cl����SO42��
C��AlO2?Ũ��Ϊ0.1 mol��L-1����Һ�У� Na����K����HCO3����Cl��
D������KSCN��Һ�Ժ�ɫ����Һ��K+��NH4+��Cl����NO3��
�ο��𰸣�D
������������Ӽ����������ѧ��Ӧ�����ܴ������棬��֮�ǿ��Եġ�A����Һ�����ԣ�Fe3����NO3����������I�������ܴ������棻B��ˮ�ĵ���ƽ�ⱻ���ƣ������Һ���������ԣ�Ҳ�����Լ��ԡ�����Լ��ԣ���Al3�����ܴ������档C��AlO2����HCO3����Ӧ��������������CO32�������ܴ������档D����Һ���������ӣ����Դ������棬��ѡD��
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬���ض�ѧ������֪ʶ��ѵ���ͼ��顣����������ѧ�������������������ѧ��������û���֪ʶ���ʵ�������������������Ҫ��ȷ���Ӳ��ܴ��������һ�����������1���ܷ������ֽⷴӦ������֮�䣻��2�������������������֮�䣻��3���ܷ���������ԭ��Ӧ������֮�䣻��4���ܷ�����Ϸ�Ӧ������֮�䣨�� Fe3+�� SCN-����������ӹ�������ʱ��Ӧ��ע����Ŀ����������������Ŀ������������һ���У���1����Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����2����Һ����ɫ������ɫʱ���ų� Cu2+�� Fe2+��Fe3+��MnO4-����ɫ���ӵĴ��ڣ���3����Һ�ľ��巴Ӧ�������硰������ԭ��Ӧ�������������۲�������������4���ǡ����ܡ����棬���ǡ�һ��������ȡ�
�����Ѷȣ���
4��ѡ���� ��֪����ȼ�����ɶ�����̼��Һ̬ˮ�ų�������Ϊ55.625kJ��g��1�������Ȼ�ѧ����ʽ�в���ȷ���ǣ�����
A��CH4(g)��2O2(g)��CO2(g)��2H2O(l)����H ����890kJ/mol
B�� CH4(g)+O2(g)=
CH4(g)+O2(g)= CO2(g)+H2O(l)����H����445kJ/mol
CO2(g)+H2O(l)����H����445kJ/mol
C��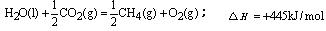
D��CH4(g)��2O2(g)��CO2(g)��2H2O(l)����H����55.625kJ/mol
�ο��𰸣�D
�����������Ŀ�и��������������ǣ�ȼ��1g�ļ���ų�55.625kJ��������Ӧ�û����ȼ��1mol����ų�������Ϊ890kJ���Ȼ�ѧ����ʽΪ��CH4(g)��2O2(g)��CO2(g)��2H2O(l)����H����890kJ��mol��1����ϵ�����������Ӧ�ķ���ʽ����ȷ��
�����Ѷȣ���
5������� ֱ���ŷź�SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2��
��1���û�ѧ����ʽ��ʾSO2�γ�����������ķ�Ӧ:?��
��2�����Ƽ�ѭ�����У�Na2SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ��?
��3������Һ����SO2�Ĺ����У�pH��n(SO3?��):n(HSO3��)�仯��ϵ���±�:
n(SO3?��):n(HSO3��)
| 91��9
| 1��1
| 1��91
|
pH
| ��.��
| 7.2
| 6.2
|
���ϱ��ж�NaHSO3��Һ���������������ԣ��û�ѧƽ��ԭ������:��������������������������
�ڵ�����Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ):������������������������
a��c��Na����=2c��SO32-����c��HSO3������
b��c��Na����> c��HSO3����> c��SO32-��>c��H����=c��OH����
c��c��Na����+c��H����= c��SO32-��+ c��HSO3����+c��OH����
(4)������Һ��pH����ԼΪ6ʱ����������������������ʾ��ͼ����:
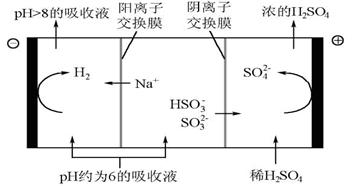
��HSO3-�������ŵ�ĵ缫��Ӧʽ����������������������������������
�ڵ�����������Һp������8����ʱ������Һ������ѭ�����á���������ԭ��:��������������������
�ο��𰸣���1��SO2+H2O H2SO3��2 H2SO3+O2
H2SO3��2 H2SO3+O2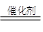 2H2SO4����2��SO2+2OH- =SO32-+H2O����3��� HSO3�����ڣ�HSO3��
2H2SO4����2��SO2+2OH- =SO32-+H2O����3��� HSO3�����ڣ�HSO3�� SO32-+H����HSO3��+H2O=H2SO3+OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�ab����4��HSO3-+H2O-2e- =3H++SO42-��H+�������õ�������H2����Һ�е�c��H�������ͣ���ʹHSO3-��������SO32-����Na+���������ң�����Һ����������
SO32-+H����HSO3��+H2O=H2SO3+OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�ab����4��HSO3-+H2O-2e- =3H++SO42-��H+�������õ�������H2����Һ�е�c��H�������ͣ���ʹHSO3-��������SO32-����Na+���������ң�����Һ����������
�����������1��SO2�γ�����������ʱ����������Ϳ����е�ˮ��������Ӧ�õ����SO2+H2O H2SO3��2 H2SO3+O2
H2SO3��2 H2SO3+O2 2H2SO4����2��������������������Һ�����Ʊ�����������Һʱ��SO2+2OH- =SO32-+H2O����3�����ݱ������ݣ���֪��n(SO3?��):n(HSO3��)=1:91ʱ����Һ��pHֵΪ���ԣ���NaHSO3��Һ�����ԣ���������������Һ��HSO3�����ڣ�HSO3��
2H2SO4����2��������������������Һ�����Ʊ�����������Һʱ��SO2+2OH- =SO32-+H2O����3�����ݱ������ݣ���֪��n(SO3?��):n(HSO3��)=1:91ʱ����Һ��pHֵΪ���ԣ���NaHSO3��Һ�����ԣ���������������Һ��HSO3�����ڣ�HSO3�� SO32-+H����HSO3��+H2O=H2SO3+OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԡ�������Һ������ʱ����Һ�е�c��H����=c��OH������������Һ�д����ŵ���غ㣬��c��Na����+c��H����=2c��SO32-��+ c��HSO3����+c��OH���������Ƴ���c��Na����=2c��SO32-����c��HSO3������a�ԣ�����n(SO?��):n(HSO?��)=1��1ʱ����Һ��pHֵΪ7.2��������ʱһ����c��HSO3����> c��SO32-�������Ƴ���c��Na����> c��HSO3����> c��SO32-��>c��H����=c��OH������b�ԣ���4�����ݵ�����ʾ�ı仯����֪HSO3-�������ŵ�ĵ缫��Ӧʽ�ǣ�HSO3-+H2O-2e- =3H++SO42-��H+�������õ�������H2����Һ�е�c��H�������ͣ���ʹHSO3-��������SO32-����Na+���������ң�����Һ����������
SO32-+H����HSO3��+H2O=H2SO3+OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԡ�������Һ������ʱ����Һ�е�c��H����=c��OH������������Һ�д����ŵ���غ㣬��c��Na����+c��H����=2c��SO32-��+ c��HSO3����+c��OH���������Ƴ���c��Na����=2c��SO32-����c��HSO3������a�ԣ�����n(SO?��):n(HSO?��)=1��1ʱ����Һ��pHֵΪ7.2��������ʱһ����c��HSO3����> c��SO32-�������Ƴ���c��Na����> c��HSO3����> c��SO32-��>c��H����=c��OH������b�ԣ���4�����ݵ�����ʾ�ı仯����֪HSO3-�������ŵ�ĵ缫��Ӧʽ�ǣ�HSO3-+H2O-2e- =3H++SO42-��H+�������õ�������H2����Һ�е�c��H�������ͣ���ʹHSO3-��������SO32-����Na+���������ң�����Һ����������
�����㶨λ�������Զ��������γ�����Ϊ�������ۺϿ����˻�ѧ��Ӧ����ʽ��д�����ӷ���ʽ��д��ˮ��Һ�е�����ƽ�⡢��Һ�е�����Ũ�ȴ�С�Ƚϡ����ԭ����֪ʶ��
�����Ѷȣ�һ��