微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ・mol-1,下列说法错误的是
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量
参考答案:D
本题解析:A、根据题给热化学方程式知,2mol(g)和1mol O2(g)完全反应生成2mol H2O(g),放热270kJ,则逆反应吸热270kJ,2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量,正确;B、2mol(g)和1mol O2(g)完全反应生成2mol H2O(g),放热270kJ,气态水变化为液体放热,2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ,正确;C、反应是放热反应,反应物能量总和大于生成物能量总和,故2mol氢气与1mol氧气的能量总和大于2mol气态水的能量,正确;D、热化学方程式中化学方程式计量数只表示物质的量不表示微粒个数,错误。
本题难度:一般
2、实验题 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为: 。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)  CH3OH(g) ΔH=-90.8kJ・mol-1
CH3OH(g) ΔH=-90.8kJ・mol-1
②2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-23.5kJ・mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ・mol-1
③CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-41.3kJ・mol-1
CO2(g)+H2(g) ΔH=-41.3kJ・mol-1
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式 ?。
(3)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 。
a.高温高压? b.低温低压
c.减少CO2的浓度? d.增加CO的浓度
e.分离出二甲醚 f.加入催化剂
(4)已知反应②2CH3OH(g)  CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质
| CH3OH
| CH3OCH3
| H2O
|
浓度/(mol・L-1)
| 0.44
| 0.6
| 0.6
|
比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”),若上述情况达到平衡,此时c(CH3OH)= 。
参考答案:(1)C+H2OCO+H2
(2)3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) ΔH=-246.4kJ・mol-1
CH3OCH3(g)+CO2(g) ΔH=-246.4kJ・mol-1
(3)ce
(4)> 0.04mol・L-1
本题解析:略
本题难度:一般
3、填空题 (4分)(1)下列反应中,属于放热反应的是?,属于吸热反应的是?。
①燃烧反应②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳
⑤食物因氧化而腐败⑥Ba(OH)2・8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(2)写出(1)中⑥的化学方程式?。
参考答案:(1)①②③⑤⑦?④⑥?(2)Ba(OH)2・8H2O +2NH4Cl ==BaCl2 +2NH3 +10H2O
本题解析:略
本题难度:简单
4、选择题 关于某一化学反应的熵变,下列说法正确的是(?)
A.△S为反应产物总熵与反应物总熵之差
B.△S与S一样随温度变化不大
C.凡是熵增加的反应一定能自发进行
D.在温度、压强一定的条件下,焓变和熵变共同决定化学反应进行的方向
参考答案:AD
本题解析:熵是与物质混乱度有关系的物理量,选项A正确。熵值以及熵变都是和温度有关系的,B不正确;熵增加的反应不一定能自发进行,选项C不正确;反应的自发性由焓变和熵变共同决定,即满足△G=△H-T・△S,选项D正确,因此正确的答案选AD。
点评:该题是基础性试题的考查,侧重对教材基础知识的巩固和训练,意在提高学生灵活运用基础知识解决实际问题的能力,难度不大,记住即可!
本题难度:简单
5、填空题 二氧化碳是一种宝贵的碳氧资源。以CO2和NH3为原料合成尿素是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)?△H1="a" kJ・mol-1
NH2CO2NH4(s)?△H1="a" kJ・mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)?△H2=+72.49kJ・mol-1
CO(NH2)2(s)+H2O(g)?△H2=+72.49kJ・mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)?△H3=-86.98kJ・mol-1
CO(NH2)2(s)+H2O(g)?△H3=-86.98kJ・mol-1
请回答下列问题:
(1)反应Ⅰ的△H1=__________kJ・mol-1(用具体数据表示)。
(2)反应Ⅱ的△S______(填>或<)0,一般在__________情况下有利于该反应的进行。
(3)反应Ⅲ中影响CO2平衡转化率的因素很多,下图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是________(填提高或降低)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如图1所示的变化趋势,其原因是__________。

(4)反应Ⅰ的平衡常数表达式K1=____________________;如果起始温度相同,反应Ⅰ由在恒温容器进行改为在绝热(与外界没有热量交换)容器中进行,平衡常数K1将__________(填增大、减少、不变)。
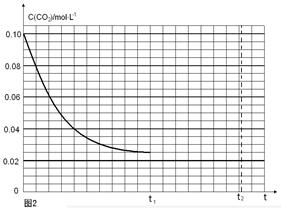
(5)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如上图2所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
(6)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3。下列物质中与尿素有类似性质的是______。
(NH4)2CO3。下列物质中与尿素有类似性质的是______。
A.NH2COONH4
B.H2NOCCH2CH2CONH2
C.HOCH2CH2OH
D.HOCH2CH2NH2
参考答案:(14分)(1)-159.47(2分)?(2)>(1分)?高温(1分)
(3)①降低(1分)②温度高于190℃时,因为反应Ⅲ是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低,(2分,给出合理解释即可给分)。
(4)K?1=1/[c2(NH3)・c(CO2)] (2分),减少(1分)
(5)
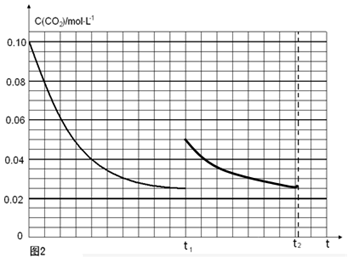 (注意:曲线的起点、平衡点和变化趋势共2分)
(注意:曲线的起点、平衡点和变化趋势共2分)
(6)A、B(2分)
本题解析:解:(1)反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)△H1="a" kJ・mol-1
NH2CO2NH4(s)△H1="a" kJ・mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)△H2=+72.49kJ・mol-1
CO(NH2)2(s)+H2O(g)△H2=+72.49kJ・mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ・mol-1
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ・mol-1
由盖斯定律总反应Ⅲ-反应Ⅱ,得到2NH3(g)+CO2(g) NH2CO2NH4(s)△H1=a=-159.47kJ・mol-1,
NH2CO2NH4(s)△H1=a=-159.47kJ・mol-1,
故答案为:-159.47;
(2)反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)△H2=+72.49kJ?mol-1,反应前后气体体积增大,△S>0,焓变分析可知是吸热反应,△H>0,所以依据反应自发进行的判断依据△H-T△S<0,需要在高温下反应自发进行,故答案为:>;高温;
CO(NH2)2(s)+H2O(g)△H2=+72.49kJ?mol-1,反应前后气体体积增大,△S>0,焓变分析可知是吸热反应,△H>0,所以依据反应自发进行的判断依据△H-T△S<0,需要在高温下反应自发进行,故答案为:>;高温;
(3)①反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ・mol-1,其他条件相同时,为提高CO2的平衡转化率,平衡正向进行,依据图象中的水碳比数据分析判断,生产中可以采取的措施是降低水碳比,二氧化碳转化率增大,故答案为:降低;
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ・mol-1,其他条件相同时,为提高CO2的平衡转化率,平衡正向进行,依据图象中的水碳比数据分析判断,生产中可以采取的措施是降低水碳比,二氧化碳转化率增大,故答案为:降低;
②反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ?mol-1,是放热反应,升温高于190℃,依据图象分析可知,二氧化碳转化率减小,因为温度升高,平衡逆向进行,
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ?mol-1,是放热反应,升温高于190℃,依据图象分析可知,二氧化碳转化率减小,因为温度升高,平衡逆向进行,
故答案为:温度高于190℃时,因为反应Ⅲ是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
(4)反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)△H1=-159.47kJ?mol-1,平衡常数K=
NH2CO2NH4(s)△H1=-159.47kJ?mol-1,平衡常数K=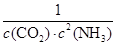 ?;
?;
起始温度相同,反应Ⅰ由在恒温容器进行改为在绝热(与外界没有热量交换)容器中进行,反应是放热反应,随反应进行温度升高平衡逆向进行,平衡常数减小;
(5)在恒温下将0.4mol NH3和0.2mol CO2放入容积为2L的密闭容器中,达到平衡时,
2NH3(g)+CO2(g) NH2CO2NH4(s)
NH2CO2NH4(s)
起始量(mol・L-1)? 0.2? 0.1? 0
变化量(mol・L-1) 0.15? 0.075
平衡量(mol・L-1) 0.05? 0.025
t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如图2所示.若其他条件不变,t1时将容器体积压缩到1L,二氧化碳浓度应增大到0.05mol・L-1,压强增大,平衡正向进行,由于生成物是固体,所以达到平衡状态,二氧化碳浓度保持不变,据此画出变化曲线为:
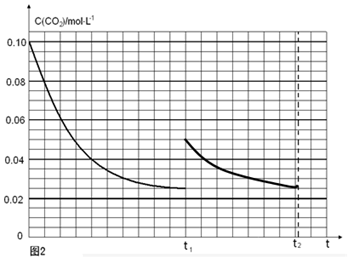 ;
;
(6)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3.分析结构特征可知,物质性质取决于官能团,尿素中氨基和羰基相连和水反应生成铵根离子,所以选项中符合此结果特征的有类似性质:
(NH4)2CO3.分析结构特征可知,物质性质取决于官能团,尿素中氨基和羰基相连和水反应生成铵根离子,所以选项中符合此结果特征的有类似性质:
A.NH2COONH4,结构中含有与羰基连接的氨基,故A符合;
B.H2NOCCH2CH2CONH2结构中含有与羰基连接的氨基,故B符合;
C.HOCH2CH2OH,结构中不含有氨基,故C不符合;?
D.HOCH2CH2NH2,分子中的氨基不是和羰基连接,不具备次性质,故D不符合;
故答案为:A、B。
本题难度:一般