微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:
①I2(g)+H2(g) 2HI(g) ΔH1=-9.48 kJ/mol
2HI(g) ΔH1=-9.48 kJ/mol
②I2(s)+H2(g) 2HI(g) ΔH2=+26.48 kJ/mol
2HI(g) ΔH2=+26.48 kJ/mol
下列判断正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.I2(g)=I2(s) ΔH=-17.00 kJ/mol
C.固态碘的稳定性比气态碘的稳定性高
D.1 mol固态碘和1 mol气态碘分别与氢气完全反应,前者断裂的I―I键更多
参考答案:C
本题解析:可逆反应不能进行完全,A项错误;根据盖斯定律,①-②得:I2(g)=I2(s) ΔH=-35.96 kJ/mol,B项错误;固态碘能量低于气态碘,故稳定性较高,C项正确;1 mol固态碘和1 mol气态碘中均含有1 mol I―I键,在反应中均全部断裂,D项错误
本题难度:一般
2、选择题 有如下反应方程式,按下列要求与所给化学方程式对应正确的是(? )(1)一种单质使一种化合物中的一种元素被还原(? )
(2)一种单质使一种化合物中的一种元素被氧化(? )
(3)同一种物质里,一种元素氧化另一种元素(? )
(4)同一种物质中,同种元素间发生氧化还原反应(? )
(5)不同物质间同种元素之间发生氧化还原反应(? )
(6)发生在不同物质间,只部分被氧化或只部分被还原的反应(? )
a.CuO+H2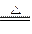 Cu+H2O
Cu+H2O
b.2KClO3MnO2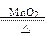 2KCl+3O2↑
2KCl+3O2↑
c.Cl2+2NaOH====NaCl+NaClO+H2O
d.KClO3+6HCl====KCl+3Cl2↑+3H2O
e.? MnO2+4HCl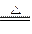 MnCl2+2H2O+Cl2↑? f.? 2NaBr+Cl2====2NaCl+Br2A、1a,2f,3b,4c,5d,6eB、1a,2f,3b,4c,5e,6dC、1f,2a,3e,4b,5c,6dD、1f,2a,3c,4b,5e,6d?
MnCl2+2H2O+Cl2↑? f.? 2NaBr+Cl2====2NaCl+Br2A、1a,2f,3b,4c,5d,6eB、1a,2f,3b,4c,5e,6dC、1f,2a,3e,4b,5c,6dD、1f,2a,3c,4b,5e,6d?
参考答案:A
本题解析:试题分析:首先标出变价元素的化合价,根据概念和要求选择。
本题难度:简单
3、选择题 2.0g?H2(g)在O2(g)中完全燃烧,生成H2O(g),放出热量Q?kJ.则下列说法正确的是( )
A.若生成H2O(l),则放出热量大于QkJ
B.若使用H2(l),则放出热量大于QkJ
C.若使用O2(s),则放出热量大于QkJ
D.电解90.0g液态水,需要吸收QkJ的热量
参考答案:A.2.0g?H2(g)在O2(g)中完全燃烧,生成H2O(g),放出热量Q?kJ,由气态变为液态,要放出热量,所以若生成
H2O(l),则放出热量大于QkJ,故A正确;
B.2.0g?H2(g)在O2(g)中完全燃烧,生成H2O(g),放出热量Q?kJ,若使用H2(l),由液态变为气态,需要吸热,则该反应放出热量小于QkJ,故B错误;
C.2.0g?H2(g)在O2(g)中完全燃烧,生成H2O(g),放出热量Q?kJ,若使用O2(s),由固体变为气体,需要吸热,则该反应放出热量小于QkJ,故C错误;
D.2.0g?H2(g)在O2(g)中完全燃烧,生成1molH2O(g),放出热量QkJ,生成5H2O(l),则放出热量大于5QkJ,则电解5mol1molH2O(l)吸收的热量大于5QkJ,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 下列关于能量转化方式的叙述错误的是
A.太阳能可转化为化学能
B.化学能可转化为热能
C.化学能可转化为电能
D.化学能可直接转化为机械能
参考答案:D
本题解析:化学能是不能直接转化成机械能的.
本题难度:一般
5、实验题 (14分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将①50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
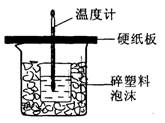
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2) 若将盐酸换成同浓度和同体积的醋酸,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用40 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上
述实验相比,所放出的热量______?__(填“比①大”、 “比①小”或“相等”),理由是__________________________?___;所求中和热的数值会________(填“相等”或“不相等”),理由是_________________________?____。
参考答案:(14分)(1)环形玻璃搅拌棒;?保温、隔热,减少实验过程中的热最损失 (2)偏小
(3) 比①小;?因为酸、碱发生中和反应放出的热量与酸、碱的用量有关;
相等?中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量,它与酸、碱的用量无关(各2分)
本题解析:略
本题难度:一般