微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在恒容密闭容器进行的可逆反应:MgSO4(s) + CO(g)  ?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
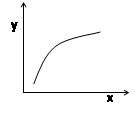
A.若平衡常数K值变大,平衡移动时v逆先减小后增大
B.容器中固体物质的质量不再改变,则反应到达平衡状态
C.若x表示温度,y可表示平衡时混合气体的密度
D.若x表示CO物质的量,y可表示平衡时CO2与CO物质的量之比
参考答案:BC
本题解析:该反应为正方向体积增加且吸热,A.若平衡常数K值变大,平衡右移,v逆增大,错误;B.容器中固体物质的质量不再改变,说明生成量和消耗量相等,则反应到达平衡状态,正确;C、升高温度,平衡正向移动,气体的质量增加,密度增大,正确;增加CO的量,平衡正向移动,但压强增大,转化的量,没有上一平衡多,故比值减小,故D错误;
本题难度:一般
2、简答题 取2g干燥铝粉和3g碘粉小心混匀,分为四堆.往各堆上分别加0.5g水,1g明矾,1g胆矾,1g无水硫酸铜.加水那堆首先冒火花,发生剧烈反应,其次发生反应的是加明矾的那一堆,再次是加胆矾的发生反应,而加无水硫酸铜的那一堆最难发生反应.
(1)铝和碘反应的方程式为______;
(2)铝和碘反应还可以看到的现象是______;
(3)四堆混合物发生反应的先后顺序说明:①______,②______.
参考答案:(1)金属铝和碘单质反应生成碘化铝,原理方程式为2Al+3I2=2AlI3,故答案为:2Al+3I2=2AlI3;
(2)金属铝和碘单质在水的作用下的反应剧烈,放热,碘单质受热易升华,所以还可以看到产生紫色蒸气,故答案为:还可以看到产生紫色蒸气;
(3)根据反应的先后顺序可以看出:水作为催化剂,可以提高铝和碘化合的反应速率,明矾中结晶水易失去,而胆矾中的结晶水相对较难失去,所以导致加水那堆首先冒火花,发生剧烈反应,其次发生反应的是加明矾的那一堆,再次是加胆矾的发生反应,而加无水硫酸铜的那一堆最难发生反应,
故答案为:水作为催化剂,提高铝和碘化合的反应速率;第一堆反应快,是直接加水的原因,第二堆比第一堆反应快是由于明矾中结晶水易失去,而胆矾中的结晶水相对较难失去.
本题解析:
本题难度:一般
3、选择题 下列各表述与示意图一致的是( )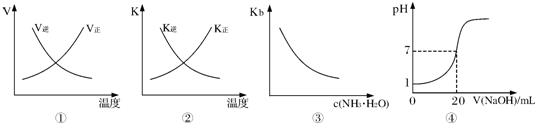
A.图①表示反应N2(g)+O2(g)?2NO(g)△H>0正、逆反应的速率随温度的变化
B.图②表示反应N2(g)+3H2(g)?2NH3(g)△H<0正、逆反应的平衡常数随温度的变化
C.图③表示氨水的电离平衡常数随氨水浓度c(NH3?H2O)的变化
D.图④表示25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,溶液的pH随加入碱体积的变化
参考答案:A、该反应为吸热反应,温度升高,正逆反应速率都增大,平衡向着正向移动,所以正反应速率大于逆反应速率,而图象中达到平衡后升高温度,逆反应速率减小是错误的,逆反应速率也应该增大,故A错误;
B、该反应为放热反应,升高温度后平衡向着逆向移动,所以逆反应的平衡常数增大,正反应的平衡常数减小,而图象中达到平衡后升高温度,逆反应的平衡常数减小、正反应的平衡常数增大与实际不相符,故B错误;
C、氨水的电离平衡常数与浓度没有关系,只受温度的影响,所以温度不变,电离平衡常数不变,而图象中平衡常数随着氨水的浓度增大而减小是错误的,故C错误;
D、25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,滴定前盐酸的pH=1,随着氢氧化钠体积不断增大,溶液的pH逐渐增大,当加入20mL氢氧化钠溶液时,二者恰好反应,溶液的pH=7,该图象符合反应实际,故D正确;
故选D.
本题解析:
本题难度:一般
4、选择题 100mL浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的量,可采用的方法是
[? ]
A.加入适量的6mol/L的盐酸
B.加入数滴氯化铜溶液
C.加入适量蒸馏水
D.加入适量的氯化钠溶液
参考答案:B
本题解析:
本题难度:一般
5、选择题 反应3Fe(s)+4H2O(g)

?Fe3O4+4H2(g)在一可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.保持体积不变,增加H2O(g)的量
B.将容器的体积缩小一半
C.保持体积不变,充入Ne使体系压强增大
D.压强不变,充入Ne使容器的体积增大
参考答案:A、因浓度越大,化学反应速率越快,所以增加H2O(g)的量,反应速率加快,故A错误;
B、将容器的体积缩小一半,反应体系中物质的浓度增大,则化学反应速率增大,故B错误;
C、保持体积不变,充入Ne,Ne不参与反应,反应体系中的各物质的浓度不变,则反应速率不变,故C正确;
D、保持压强不变,充入Ne,使容器的体积变大,反应体系中各物质的浓度减小,则反应速率减小,故D错误;
故选:C.
本题解析:
本题难度:一般