微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 导致下列环境问题与排放二氧化硫有关的是
A.温室效应
B.光化学烟雾
C.臭氧空洞
D.酸雨
参考答案:D
本题解析:分析:温室效应是由于燃烧过多煤炭、石油和天然气,这些燃料燃烧后放出大量的二氧化碳气体进入大气中造成的;
光化学烟雾是大气中的氮氧化物与碳氢化合物经过紫外线照射发生反应形成了光化学烟雾;
臭氧空洞是向大气排放的氯氟烃等化学物质在扩散至平流层后与臭氧发生化学反应,导致臭氧层反应区产生臭氧含量降低的现象;
酸雨是大量使用煤、石油、天然气等化石燃料,燃烧后产生的硫氧化物或氮氧化物,在大气中经过复杂的化学反应,形成硫酸或硝酸气溶胶,或为云、雨、雪、雾捕捉吸收,降到地面成为酸雨.
解答:A、温室效应是由于大量排放二氧化碳气体造成的,故A错误;
B、光化学烟雾是氮氧化物与碳氢化合物反应生成的,故B错误;
C、臭氧空洞是氯氟烃等化学物质与臭氧发生化学反应形成的,故C错误;
D、酸雨形成主要是二氧化硫气体形成的,故D正确.
故选D.
点评:本题考查了环境污染的几种效应,重点考查化学知识在环境污染中的知识应用.
本题难度:一般
2、填空题 (17分)合成氨工业上常用下列方法制备H2:
方法: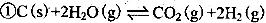
方法: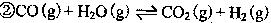
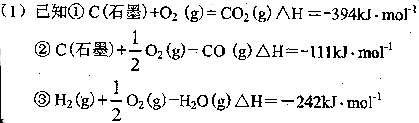
试计算25℃时由方法②制备l000g H2所放出的能量为_________ kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:
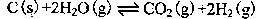 其相关数据如下表所示:
其相关数据如下表所示:
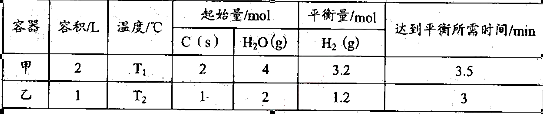
①T1_________T2(填“>”、“=”或“<”);
T1℃时,该反应的平衡常数K="_________" 。
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是_________。
③一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_________。
A.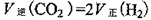
B.混合气体的密度保持不变
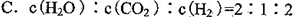
D.混合气体的平均相对分子质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
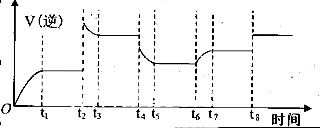
可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则从t1到t8哪个时间段H2O (g)的平衡转化率最低_________,t4时刻改变的条件是__________。
⑤在25 ℃时,c mol/L,的醋酸与0.02mol/L NaOH溶液等体积混合后溶液刚好呈中性,
用含c的代数式表示CH3COOH的电离常数Ka=_________。
参考答案:(17分)(1)20500kJ (2分)
(2)①? >?(2分)? 12.8(2分)?
② <1.4mol/L (2分)?
③BD(选全得2分,漏选得1分,有错选0分)
④t7-t8(或“t7到t8”)(2分) 降低温度(2分)
⑤ 2×10-9/(c-0.02)?(3分)
本题解析:(1)根据盖斯定律得由方法②制取氢气的热化学方程式可由已知中的反应得到,每生成1mol氢气放出的热量=①-②-③=(394-111-242)kJ=41kJ,1000g氢气的物质的量是500mol,所以制备l000g H2所放出的能量为500×41=20500kJ;
(2)①由表中数据可计算各物质的平衡浓度,所以T1的化学平衡常数K1=1.62×0.8/0.42=12.8,同理可计算T2的平衡常数K2=1.35,因为该反应是吸热反应,K1> K2,所以T1>T2
②反应进行到一半时,若按反应速率一直不变计算,1.5min时水蒸气的浓度是2mol/L-0.6mol/L=1.4mol/L,但是反应速率随反应的进行逐渐减小,前一半的反应速率大于后一半的反应速率,所以消耗水蒸气的浓度较大,则剩余水蒸气的浓度应小于1.4mol/L;
③A、平衡时氢气的正反应速率是二氧化碳逆反应速率的2倍,错误;B、该反应有固体参与,所以气体的质量一直在变,当达到平衡时气体的质量不再变化,容器的体积一直不变,所以当气体的密度不变时证明已达平衡状态,正确;C、气体的浓度之比符合化学计量数之比时 不能判断平衡是否到达,错误;D、混合气体的质量与气体的物质的量在未达平衡时一直在变,即气体的平均相对分子质量在变,平衡时混合气体的质量、物质的量均固定,混合气体的平均相对分子质量不再变化,正确,答案选BD;
④H2O (g)的平衡转化率最低,证明平衡一直逆向移动,t2~t4逆反应速率陡然增大后减小至不变,说明改变的一个条件是增大压强,平衡逆向移动;t4~t6逆反应速率陡然减小至不变,说明改变的条件是降低温度,平衡逆向移动;t6~t7逆反应速率先不变再逐渐增大至不变,说明改变的条件是又充入了水蒸气,虽然平衡正向移动,但水蒸气的转化率降低了,所以水蒸气的转化率最低的是t7-t8;t4时刻改变的条件是降低温度;
⑤混合溶液呈中性证明c(OH-)= c(H+)=1×10-7mol/L,根据电荷守恒得c(Na+)=c(CH3COO-)=0.01mol/L,因为醋酸钠溶液呈碱性,现在溶液呈中性,说明醋酸过量,所以剩余醋酸的物质的量浓度是(c-0.02)/2mol/L,则产生的电离平衡常数K= c(H+) c(CH3COO-)/ c(CH3COOH)= 2×10-9/(c-0.02)。
本题难度:一般
3、选择题 右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是
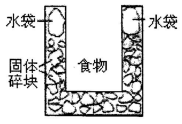
A.硝酸铵
B.生石灰
C.氯化镁
D.石灰石
参考答案:B
本题解析:水与固体碎块混和,杯内食物温度逐渐上升,这说明和水的混合过程是放热的。则选项B正确,A中是吸热的,C中热量不明显,D中不溶于水,答案选B。
点评:该题是基础性试题的考查,试题贴近生活实际,有利于调到学生的学习兴趣和学习积极性。该题基础性强,旨在考查学生灵活运用基础知识解决实际问题的能力,难度不大,记住常见的热量变化即可。
本题难度:一般
4、选择题 下列说法不正确的是
A.NH3・H2O NH4++OH-达到平衡后,升高温度平衡正向移动
NH4++OH-达到平衡后,升高温度平衡正向移动
B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率
C.明矾水解生成Al(OH)3胶体,可用作净水剂
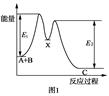
D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0
参考答案:D
本题解析:A.电解质的电离过程是吸热过程。当达到平衡后,升高温度,平衡吸热方向即向正向移动。正确。B.在海轮的外壳上镶入锌块,由于活动性Zn>Fe,Zn作原电池的负极,就可以对轮船起到保护作用,因此可减缓船体的腐蚀速率。正确。C.明矾KAl(SO4)2是强酸弱碱盐。Al3+水解生成Al(OH)3胶体,表面积大,吸附力强,可以吸附水中悬浮的固体颗粒,当重力大于浮力时就从水中沉淀出去,从而达到净化水的目的。因此可用作净水剂。正确。D.由图可以看出反应过程中A+B→X中的反应物的能量不如生成物的X的能量高,所以该反应的△H>0,而反应X→C由于反应物X的能量高,生成物C的能量低,所以该反应的△H<0。错误。
本题难度:一般
5、选择题 下列说法错误的是
[? ]
A.化学反应中的能量变化通常表现为热量的变化
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.需要加热才能发生的反应一定是吸热反应
D.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
参考答案:C
本题解析:
本题难度:简单