��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �±��г���A-R9��Ԫ�������ڱ��е�λ�ã�
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0
2
E
F
3
A
C
D
G
R
4
B
H
|
��1������9��Ԫ���У���ѧ��������õ���______������õ���______��
��2����DԪ������������Ӧ��ˮ�������������Ʒ�Ӧ�����ӷ���ʽ��______��
��3����A��B��C����Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳������Ϊ______��
��4����FԪ���⻯��Ļ�ѧʽ��______��������Һ��PHֵ______��
��5����GԪ�غ�HԪ�����ߺ˵����֮����______��
�ο��𰸣�����Ԫ�������ڱ��еķֲ�֪ʶ������֪��A��Na��B��K��C��Mg��D��Al��E��C��F��O��G��Cl��H��Br��R��Ar��
��1��Ԫ�����ڱ���Ԫ�ػ�����������ϡ������Ԫ�صĵ��ʣ����ϵ��½����Ļ����������ߣ����ҵ�������Ļ����������ߣ�����õĽ�����K���ʴ�Ϊ��Ar��K��
��2����Ԫ������������Ӧ��ˮ������������������������������������Ʒ�Ӧ�����ӷ���ʽ��
Al��OH��3+OH-=AlO2-+2H2O���ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��3�����Ӳ�Խ��뾶Խ������K�İ뾶����Ӳ���ͬ��ͬ����Ԫ�ص�ԭ�Ӵ����Ұ뾶��С������Na��Mg���ʴ�Ϊ��K��Na��Mg��
��4��OԪ���⻯��Ļ�ѧʽ��H2O����ˮ��Һ��������Һ��PHֵΪ7���ʴ�Ϊ��7��
��5��ClԪ�غ�BrԪ�����ߺ˵����֮���ǵ�������Ԫ�ص���������Ϊ18���ʴ�Ϊ��18��
���������
�����Ѷȣ�һ��
2���ƶ��� ��A��B��C��D��E?����Ԫ�أ����ǵĺ˵�������������Ҷ�С��20������C��E�ǽ���Ԫ�أ�A��E��ͬһ�壬����ԭ�ӵ����������Ų�Ϊns1��B��DҲ��ͬһ�壬����ԭ��������p�ܼ���������s�ܼ���������������Cԭ��������ϵ���������Dԭ��������ϵ�������һ�롣��ش��������⣺
��1������������Ԫ���У�����s������____________����Ԫ�ط��ţ���
��2����������Ԫ����ɵ�һ�ֻ�������__________________��д��ѧʽ����
��3��д��DԪ�ػ�̬ԭ�ӵ����������Ų�ͼ___________________��
��4��Ԫ�ص縺��ΪB_______D��Ԫ�ص�һ������ΪC______E�����������������������
�ο��𰸣���1 ��H��K?
��2 ��KAl(SO4)2��12H2O?
��3 ��
��4����?����
���������
�����Ѷȣ�һ��
3������� �±��г���A-R9��Ԫ�������ڱ��е�λ�ã���Ԫ�ط��Ż�ѧʽ��գ�
��
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0
2
E
F
3
A
C
D
G
R
4
B
H
|
��1�������Ԫ���У���ѧ��������õ���______����������ǿ���ǣ�______����������ˮ���������ǿ�ļ�ĵ���ʽ��______����������ˮ����������ǿ������______��
��2��DԪ�ص�����������Ӧ��ˮ������AԪ�ص�����������Ӧ��ˮ���ﷴӦ�����ӷ���ʽ��______��
��3��A��B��C����Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳�����е�Ϊ______��
��4��F���⻯��ĵ���ʽ______��G��H�⻯����ȶ��Եݼ���˳���ǣ�______��
��5��HԪ�ظ�AԪ���γɵĻ�����ĵ���ʽ��______��
��6��C��G����Ԫ���γɵĻ���������______������ӻ�������ۻ�����������õ���ʽ��ʾ���γɹ���______��
�ο��𰸣���Ԫ�������ڱ��е�λ�ÿ�֪��AΪNa��BΪK��CΪMg��DΪAl��EΪC��FΪO��GΪCl��RΪAr��HΪBr��
��1��ϡ������Ar������ã�ͬ�������϶��½�������ǿ���ǽ����Լ�����ͬ������ԭ��������������Լ������ǽ�������ǿ����K�Ľ�������ǿ��Cl�ķǽ�������ǿ����KOH������ǿ������ʽΪ ��HClO4��������ǿ��
��HClO4��������ǿ��
�ʴ�Ϊ��Ar��K�� ��HClO4��
��HClO4��
��2�������������������Ʒ�Ӧ����ƫ��������ˮ����Ӧ���ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��3��ͬ�������϶���ԭ�Ӱ뾶����ͬ������ԭ����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶K��Na��Mg��
�ʴ�Ϊ��K��Na��Mg��
��4��O���⻯��ΪH2O��H2O2��H2O������Oԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ ��H2O2��Oԭ��֮���γ�1�Թ��õ��Ӷԡ�Oԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ
��H2O2��Oԭ��֮���γ�1�Թ��õ��Ӷԡ�Oԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ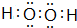 ��
��
ͬ�������϶��·ǽ����Լ������ǽ�����Խǿ�⻯��Խ�ȶ������⻯���ȶ���HCl��HBr��
�ʴ�Ϊ�� ��
��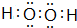 ��HCl��HBr��
��HCl��HBr��
��5��NaBr�������ӻ�������������������ӹ��ɣ�����ʽΪ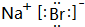 ���ʴ�Ϊ��
���ʴ�Ϊ��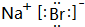 ��
��
��6��C��G����Ԫ���γɵĻ�����ΪMgCl2���������ӻ�����õ���ʽ��ʾ���γɹ���Ϊ�� ��
��
�ʴ�Ϊ�����ӻ���� ��
��
���������
�����Ѷȣ���
4��ѡ���� ��֪������Ȼ������3��ͬλ�� ��Ľ������ԭ������Ϊ28.1�����й���
��Ľ������ԭ������Ϊ28.1�����й��� ԭ�Ӻ�����
ԭ�Ӻ�����
˵������ȷ����
[? ]
A������90%
B����90%
C������90%
D�����ж�
�ο��𰸣�A
���������
�����Ѷȣ���
5������� A��B��C��Ԫ��ԭ�ӵĺ�������������ԭ���٣�A��C����ͬ���壬�����һ���ڣ�AԪ�غ�BԪ�ص�ԭ�����ߺ˵����֮��Ϊ5��Bԭ�Ӻ����3���Ӳ�ȵ�2���Ӳ����������ӡ�
��1����B��ԭ�ӽṹʾ��ͼΪ___________��A���ӵĽṹʾ��ͼΪ___________��
��2��B��C�γɻ�����Ļ�ѧʽ��___________�����ĵ���ʽ��___________������___________���������ӡ����ۡ�����A��B�γɻ�����Ļ�ѧʽ��____________�����ĵ���ʽ��_____________��������__________�����
�ο��𰸣���1��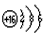 ��
��
��2��H2S�� �����ۣ�Na2S��
�����ۣ�Na2S��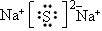 ������
������
���������
�����Ѷȣ�һ��