微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 利用下图装置,写出除去下列气体中的杂质的方法,并写出化学方程式(括号内的气体为杂质)。
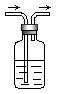
(1)CO2(SO2)?___________,化学方程式?_____________。
(2)SO2(SO3,假设SO3为气体)____________,化学方程式?_______________。
(3)NO(NO2)____________,化学方程式_________________。
参考答案:(1)将混和气体通入到盛有饱和NaHCO3溶液的该装置中,化学方程式是:
SO2+2NaHCO3=2CO2↑+Na2SO3+H2O
(2)将混和气体通入到盛有饱和NaHSO3溶液的该装置中,化学方程式是:
SO3+2NaHSO3=2SO2↑+Na2SO4+H2O
(3)将混和气体通入到盛有水的该装置中,化学方程式是:
3NO2+H2O=NO+2HNO3
本题解析:
本题难度:一般
2、选择题 NA表示阿伏加德罗常数的值,则下列叙述正确的是
A.6.8g熔融的KHSO4中含有0.05NA个阳离子
B.22.4?L?O2气体中,含有电子数为16NA
C.2L?0.5mol?L-1的醋酸溶液中含有CH3COO-NA个
D.常温常压下,1?mol?NO2气体与水反应生成NA个NO3-离子
参考答案:A
本题解析:分析:A、依据n= 计算物质的量,结合熔融KHSO4中电离出钾离子和硫酸氢根离子计算;
计算物质的量,结合熔融KHSO4中电离出钾离子和硫酸氢根离子计算;
B、依据气体摩尔体积的应用条件分析判断,标准状况下22,4L为1mol;
C、醋酸是弱电解质存在电离平衡;
D、二氧化氮和水反应生成硝酸和一氧化氮.
解答:A、6.8g熔融的KHSO4中物质的量=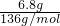 =0.05mol,熔融KHSO4中电离出钾离子和硫酸氢根离子,含有0.05NA个阳离子,故A正确;
=0.05mol,熔融KHSO4中电离出钾离子和硫酸氢根离子,含有0.05NA个阳离子,故A正确;
B、不在标准状况,22.4 L O2气体不是1mol,故B错误;
C、醋酸是弱电解质存在电离平衡,2L 0.5mol?L-1的醋酸溶液中含有CH3COO-小于NA个,故C错误;
D、常温常压下,3NO2+H2O=2HNO3+NO,1 mol NO2气体与水反应生成 NA个NO3-离子,故D错误;
NA个NO3-离子,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的应用,主要是物质构成的判断,气体摩尔体积的应用条件,弱电解质分析理解,化学方程式的简单计算,题目难度中等.
本题难度:简单
3、选择题 下列涉及有机化合物的分离提纯的说法正确的是
A.除去乙烷中混有的乙烯,可将混合气体通过酸性高锰酸钾溶液
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.除去溴苯中混有的Br2,可用NaOH溶液洗涤分液
D.乙酸乙酯中的少量乙酸和乙醇可用氢氧化钠溶液除去
参考答案:C
本题解析:A不正确,因为酸性高锰酸钾溶液能把乙烯氧化生成CO2,应该用溴水;石油分馏得不到甲烷、乙烯和苯,B不正确;苯和氢氧化钠溶液不反应,但溴可以溶解在氢氧化钠溶液中,C正确;氢氧化钠能使乙酸乙酯水解,D不正确,应该用饱和碳酸钠溶液,答案选C。
点评:把物质中混有的杂质除去而获得纯净物叫提纯,将相互混在一起的不同物质彼此分开而得到相应组分的各纯净物叫分离。在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。
本题难度:一般
4、填空题 (10分)按下列要求回答
(1)除去下列不纯物质中的少量杂质(括号内为杂质),请填入适当的试剂
①Fe(Al)??②NH3(H2O)?
③NO(NO2)??④NaCl溶液(Na2SO4)?
(2)实验室配制100mL0.5mol・L?1的Na2CO3溶液,回答下列问题:
①应用托盘天平称取碳酸钠粉末?g。
②配制时应选用的仪器有500mL溶量瓶,托盘天平、烧杯、药匙、?。
③若实验时遇到下列情况,所配溶液的浓度偏大的是?。
A.加水定容时超过刻度线,又吸出少量至刻度线
B.没有将洗涤液转入容量瓶
C.容量瓶洗涤后内壁有水珠而未作干燥 处理
处理
D.定容时府视刻度线
参考答案:(1) NaOH?碱石灰? H2O? BaCl2(适量)?各1分
(2) 5.3g?玻璃棒、胶头滴管? D?各2分
本题解析:略
本题难度:简单
5、选择题 物质的量浓度相同的NaCl、MgCl2、AlCl3三种物质的溶液,当溶液的体积比为3∶2∶1时,它们与同一浓度的AgNO3溶液恰好反应,则消耗的AgNO3溶液的体积比是
A.3∶4∶3
B.1∶1∶1
C.1∶2∶3
D.3∶2∶1
参考答案:A
本题解析:NaCl、MgCl2、AlCl3三种溶液中所含Cl-的物质的量之比为1×3∶2×2∶3×1=3∶4∶3.
本题难度:简单