��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������װ�õ�˵������ȷ���ǣ�������
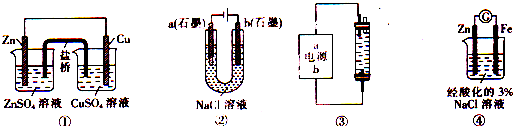
A��װ�â������е�K+����ZnSO4��Һ
B��װ�âڹ���һ��ʱ���a��������Һ��pH��С
C����װ�â�����һ����������Һ������������bΪ�����������Ϊ�����Ȼ�����Һ
D��װ�â��е�����Zn����Fe��װ������Fe2+����
�ο��𰸣�A��װ�â������е�K+����CuSO4��Һ����A����
B������Ȼ�����Һʱ��a���ǵ���������a��������������ͬʱa����������������Ũ�ȴ���������Ũ�ȣ�������Һ�ʼ��ԣ�����pH����B����
C���ô�������������Һ�����Ե�ⱥ���Ȼ�����Һ��ȡ����������Һ�������������������������������������ƣ�Ϊʹ�������ƺ�������Ӧ��֣���b��Ӧ��ԭ�����������C��ȷ��
D����װ���У�п�Ǹ������������������Ӵ�п�ص����������������������ӵõ���������������D����
��ѡC��
���������
�����Ѷȣ���
2������� ��������������Ӧ����A��NaOH+HCl=NaCl+H2O?��B��2FeCl3+Cu=2FeCl2+CuCl2
��1����������Ӧ���ʣ��ж��ܷ���Ƴ�ԭ��أ���ܡ����ܡ���
��A��______��B��______
��2�������A��B�����ܣ�˵����ԭ��______
��3�������A��B�����ԣ���װװ��ͼ��д�����������ĵ缫��Ӧʽ
������______
������______��
�ο��𰸣���1��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�ֻ��������ԭ��Ӧ���е��ӵ�ת�ƣ�����A��Ϊ��������ԭ��Ӧ��������Ƴ�ԭ��أ���B��Ϊ������ԭ��Ӧ��������Ƴ�ԭ��أ�
�ʴ�Ϊ����A�����ܣ�B�����ԣ�
��2��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�����������ԭ��Ӧ����������������Ӧ��A��Ϊ��������ԭ��Ӧ��û�з������ӵ�ת�ƣ��ʲ�����Ƴ�ԭ��أ�
�ʴ�Ϊ����A������������ԭ��Ӧ��û�з������ӵ�ת�ƣ�
��3����2FeCl3+Cu=2FeCl2+CuCl2��Ӧ�У�FeCl3����ԭ��Ϊ������Ӧ������̼�����������缫��ӦΪ2Fe3++2e-=2Fe2+
Cu��������Ϊԭ��ظ�����Ӧ���缫��ӦΪ Cu-2e-=Cu2+��ѡȡ�μӻ�ԭ��Ӧ�ĵ������ҺΪԭ��صĵ������Һ��
�ʴ�Ϊ��Cu-2e-=Cu2+��2Fe3++2e-=2Fe2+����װ��ͼΪ

���������
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ʾ��Zn��Cu�γɵ�ԭ��أ�ijʵ����ȤС������ʵ����ڶ��鿨�ϵļ�¼���£���Ƭ�ϵ�������������?��?��

�� ʵ���ļ�¼��
��Cu������Zn����
��Cu���������ݲ�����������ԭ��Ӧ
��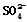 ��Cu���ƶ� ��Cu���ƶ�
������0.5mol�����������ߣ���ɲ���0.25mol����
�ݵ��ӵ������ǣ�Cu�D��Zn
��������Ӧʽ��Cu��2e��===Cu2��������������Ӧ
|
A���٢ڢ�? B���ڢۢ�? C���ڢ�? D���ۢܢ�
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ�������Zn��Cuԭ����У�Zn��������������ط�ӦZn+2H+��Zn2++H2���������ɸ��������������������������ƶ���
ZnΪ������CuΪ�������ʢٴ���H+�������ƶ�����ͭ�缫�ϵõ����ӣ��ų��������ʢ���ȷ��SO42����п�缫�ƶ�������ѡ��۴���Cu�缫�Ϸ���2H++2e����H2�����ʢ���ȷ������0.5mol���������ߣ����������0.25mol���ʢ���ȷ��������Zn�缫����Cu�缫���ʢݲ���ȷ����ѡC��
�����������Ǹ߿��ֵij������ͺ���Ҫ�Ŀ��㣬��Ҫ�ǿ���ѧ����ԭ���ԭ�����缫���ơ��缫��Ӧʽ���˽����������ּ������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷԭ��صĹ���ԭ�����缫���жϡ������ĵ缫��Ӧ�����ӡ����ӵ��ƶ�����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
4������� ��.��������һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�
3SiO2��6C��2N2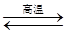 Si3N4��6CO��DH ��0��
Si3N4��6CO��DH ��0��
��1�����ݻ��̶����ܱ������У��ֱ������ֲ�ͬ��ʵ�������½��������Ʊ���Ӧ�����N2�����ʵ���Ũ����ʱ��ı仯��ͼ��ʾ��
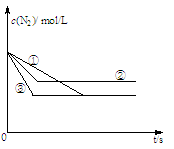
�ں͢۷ֱ���ı�һ�ַ�Ӧ���������ı�������ֱ��ǣ��� ���� ��
��2��1 000��ʱ����2 L�ܱ������н���������Ӧ������ʼʱN2Ũ��Ϊ4.0 mol/L����1Сʱ��Ӧ�ﵽƽ��״̬����ʱ������������Ũ��Ϊ10.0 mol/L������CO��ʾ�ķ�Ӧ����Ϊ ��
��.ͼΪMg��NaClOȼ�ϵ�ؽṹʾ��ͼ��
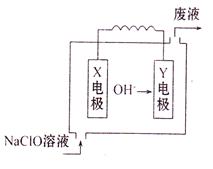
��֪�������ҺΪNaOH��Һ,�����缫����һ�缫Ϊʯī�缫��
��1��Y�缫����Ϊ ��
��2��X�缫�����ĵ缫��ӦʽΪ ��
��3�����õ�ؿ�ʼʱ����1L 0.2mol/L��NaOH��Һ��Ȼ����¿ڳ���1L 0.1mol/L��NaClO��Һ�������������̵�����仯������NaClO��ȫ�ŵ�ʱ��Һ��pH= ��
�ο��𰸣�(��2�� ��12��)�� ��1�����»�ͨCO ������� ��2��0.15 mol��L-1��min-1
��1��Mg ��2��ClO��+2e��+H2O=Cl��+2OH�� ��3�� 13
����������� ��1������ͼ���֪�����ߢڢ۴ﵽƽ���ʱ���С�����ߢٴﵽƽ���ʱ�䣬˵����Ӧ���ʿ졣�������ߢ�ƽ��ʱ������Ũ�ȴ����ߢ�ƽ��ʱ����Ũ�Ȳ��䡣��������Ӧ ���������ķ��ȷ�Ӧ����ڸı������Ӧ���������¶Ȼ�ͨCO�����۸ı������Ӧ���Ǽ��������
��2��3SiO2��6C��2N2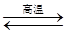 Si3N4��6CO
Si3N4��6CO
��ʼŨ�ȣ�mol/L�� 4 0
ת��Ũ�ȣ�mol/L�� x 3x
ƽ��Ũ�ȣ�mol/L�� 4��x 3x
ƽ��ʱ������������Ũ��Ϊ10.0 mol/L����4��x��3x��10�����x��3��������CO��ʾ�ķ�Ӧ����Ϊ9mol/L��60min��0.15 mol��L-1��min-1��
��1������װ��ͼ��֪�������������������Y�缫�ƶ�����Y�缫�Ǹ�����þ�ǻ��õĽ�������������Y�缫��Mg��
��2��X�缫����������������������õ����ӷ�����ԭ��Ӧ����缫��ӦʽΪClO��+2e��+H2O=Cl��+2OH�� ��
��3��1L 0.1mol/L��NaClO��Һ�д������Ƶ����ʵ�����0.1mol�����ݵ缫��ӦʽClO��+2e��+H2O=Cl��+2OH�� ��֪����0.2mol���������ӡ�1L 0.2mol/L��NaOH��Һ�����������ӵ����ʵ�����0.2mol��������ȫ��Ӧ����Һ�����������ӵ����ʵ�����0.4mol����������0.2mol�����������븺��������þ���ӽ������������þ������������Һ�����������ӵ�Ũ����0.2mol��2L��0.1mol/ 91eXAm.orgL������ҺpH��13��
���㣺���鷴Ӧ���ʡ����������ƽ��״̬��Ӱ���Լ�ԭ���ԭ����Ӧ��
�����Ѷȣ�����
5��ѡ���� һ��ԭ��ص��ܷ�Ӧ���ӷ���ʽ��Zn+Cu2+�TZn2++Cu���÷�Ӧ��ԭ��������ȷ��������
| ?A | ?B | ?C | ?D
?����
?Zn
?Ag
?Cu
?Cu
?����
?Cu
?Cu
?Zn
?Zn
?�������Һ
?CuCl2
?H2SO4
?CuSO4
?FeCl2
|
A��A
B��B
C��C
D��D
�ο��𰸣��ѵ�ط�Ӧ����ʽ����������أ�����������Ӧ�ĵ缫Ϊ����������п��������������ԭ��Ӧ�ĵ缫Ϊ�����������ò���п���õĽ�����ǽ������������������з�����ԭ��Ӧ��������ҺΪ�������Һ�������Ǻ���ͭ���ӵ���Һ��
��ѡC��
���������
�����Ѷȣ���