|
|
|
高中化学知识点总结《物质的量》答题技巧(2017年最新版)(五)
2017-03-05 13:19:40
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 纯碱在工业上非常重要。
(1)取一定量纯碱细小粉末置于烧杯中,加入一定量的水,可以得到颗粒较大的晶体A。烧杯温度升高,理由是 ;
(2)从上述烧杯中得到干燥纯净的晶体A,实验程序为: ;(填序号,可重复使用)
①蒸发结晶②放入干燥器③转移入过滤器中④用水洗涤2-3次⑤用乙醇洗涤⑥加热灼烧
(3)取纯净物13.92g晶体A,进行热重分析,直到质量不再改变,生成物质Z,具体数据如下:
物质
| 样品A
| T1oC下得到物质X
| T2oC下得到物质Y
| 600oC时得到物质Z
| 质量/g
| 13.92
| 11.75
| 7.45
| 6.36
|
通过计算确定样品A的化学式。并写出计算过程。
2、选择题 物质的量相同的N2、O2、CO2混合后,通过Na2O2颗粒一段时间,测得体积变为原混合气体体积的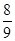 (同温同压下),此时N2、O2、CO2的物质的量之比为 (同温同压下),此时N2、O2、CO2的物质的量之比为
A.1∶1∶0
B.6∶9∶0
C.3∶4∶1
D.3∶3∶2
|
3、选择题 下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A.该硫酸试剂的物质的量浓度为18.4 mol・L-1
B.该硫酸与等体积的水混合所得溶液的质量分数小于49%
C.配制200.0 mL 4.6 mol・L-1的稀硫酸需取该硫酸50.0 mL
D.2.7 gAl与足量的该硫酸反应可得到标准状况下的H2 3.36 L
4、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是
A.2.3gNa完全与O2反应,失去的电子数为0.1NA
B.0.2mol/L的NaCl溶液中含Cl-数为0.2NA
C.7.8gNa2O2中含有的阴离子数为0.2NA
D.标准状况下,22.4LSO3中氧原子数为3NA
|
5、填空题 甲乙两位同学分别用不同的方法配制100 mL 3.6 mol/L的稀硫酸。
(1)若采用18 mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为 。?
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是?
若定容时仰视刻度线,则所配溶液浓度 (填“偏大”、“偏小”或“无影响”)。?
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是 ?。?
③定容的正确操作是 ?。?
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是 (填序号)。?
A.吸出多余液体,使凹液面与刻度线相切
B小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
(3)乙学生:用100 mL量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。你认为此法是否正确?若不正确,指出其中错误之处: ?。?