��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������˳����ȷ����
A�����ȶ���H2O>HF>H2S
B����������ϼ�F>N>C
C������H2CO3>H3PO4>H2SO4
D���ǽ�����Cl>S>Si
�ο��𰸣�D
����������ǽ�����ΪF>O>S���������ȶ���ΪHF>H2O>H2S����A����F�������ϼۣ�������������ϼ�ΪN>C>F����B��������ΪH2SO4F>H3PO4>H2CO3����C��ȷ���ǽ�����Cl>S>Si����D��ȷ��
���������⿼����Ԫ�������ɣ��ÿ����Ǹ߿�������ص���ȵ㣬�����ѶȲ���
�����Ѷȣ�һ��
2��ѡ���� ���ݱ����ṩ�IJ��ֶ�����Ԫ��ԭ�Ӱ뾶����Ҫ���ϼ۵���Ϣ���ж�������������ȷ���ǣ�
Ԫ�ش���
| L
| M
| Q
| R
| T
|
ԭ�Ӱ뾶/nm
| 0��160
| 0��143
| 0��112
| 0��104
| 0��066
|
��Ҫ���ϼ�
| ��2
| ��3
| ��2
| ��6����2
| ��2
|
?
A���⻯��ķе�ΪH2T<H2R
B��������ϡ���ᷴӦ������ΪL��Q
C��M��T�γɵĻ������������
D��L2����R2�������������
�ο��𰸣�BC
�������������Ԫ�ص�ԭ�Ӱ뾶��Ԫ�صĻ��ϼۿ���֪��L��Mg��M��Al�� Q��Be��R��S��T��O��A��O��S��ͬһ�����Ԫ�أ����ڷǽ�����O>S����Ԫ�ص��⻯��H2O��H2S�����ɷ��ӹ��ɵ����ʡ�����O�ĵ縺�Դ�ԭ�Ӱ뾶С��������ˮ����֮����˴��ڷ��Ӽ��������⣬���������������H2S�ķ��Ӽ�ֻ���ڷ��Ӽ�����������˷е�H2O>H2S������B��������Mg>Al��Ԫ�صĽ�����Խǿ�������ᷢ����Ӧʱ���ʾ�Խ�졣�����ͬŨ�ȵ����ᷴӦ����Mg>Al����ȷ��C��Al2O3�����������������ǿ�ᷴӦ�����κ�ˮ��Ҳ����ǿ�Ӧ�����κ�ˮ����ȷ��D��Mg2���ĺ�������Ų�Ϊ2��8����S2���ĺ�����ӵ����Ų�Ϊ2��8��8����˺������������ȡ�����
�����Ѷȣ�һ��
3������� ��10�֣�ÿ�ո�2�֣�ԭ�ӽṹ��Ԫ�����ڱ�������������ϵ����ش��������⣺
��1�����У�n��1��d10ns���ӹ��͵�Ԫ��λ�����ڱ���?����
��2������Ϊ��21���ͽ��������ѣ�Ti��Ԫ��ԭ�ӵļ۵����Ų�ʽΪ��?��
��3��д���ؿ��к������Ľ���Ԫ��ԭ�ӵĺ�������Ų�ʽ?��
��4��д��3p�������2��δ�ɶԵ��ӵ�Ԫ�صķ��ţ�?��
��5����֪Ti3�����γ���λ��Ϊ6����ɫ��ͬ����������ᄃ�壬һ��Ϊ��ɫ����һΪ��ɫ�����־������ɶ�ΪTiCl3��6H2O��Ϊ�ⶨ�����־���Ļ�ѧʽ�����������ʵ�飺a�ֱ�ȡ����������������ᄃ�����Ʒ��ɴ�����Һ��b�ֱ���������Һ�е���AgNO3��Һ����������ɫ������c������ȫ��ֱ���˵����ݳ�������ϴ�Ӹ�������������ԭ��ɫ�����ˮ��Һ�õ��İ�ɫ��������Ϊ��ɫ�����ˮ��Һ��Ӧ�õ�����������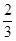 ������ɫ���������Ļ�ѧʽΪ?
������ɫ���������Ļ�ѧʽΪ?
�ο��𰸣���1��ds?��2��3d24s2?��3��1s22s22p63s23p1?��4��Si? S
��5��[TiCl��H2O��5]Cl2��H2O
�����������1���������������ڰ��չ���ԭ�������������ܼ��Ĺ�����ƣ����Ը���ɫλ��ds����
��2�����ݹ���ԭ����֪���ѣ�Ti��Ԫ��ԭ�ӵļ۵����Ų�ʽΪ3d24s2��
��3���ؿ��к������Ľ���Ԫ����Al�����Ը��ݹ���ԭ����֪����ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p1��
��4��3p�������2��δ�ɶԵ��ӵ�Ԫ��Ӧ����Si��S��
��5������ԭ��ɫ�����ˮ��Һ�õ��İ�ɫ��������Ϊ��ɫ�����ˮ��Һ��Ӧ�õ�����������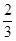 ��֪����ɫ��������2�������Ӳ������壬���Ի�ѧʽΪ[TiCl��H2O��5]Cl2��H2O��
��֪����ɫ��������2�������Ӳ������壬���Ի�ѧʽΪ[TiCl��H2O��5]Cl2��H2O��
�����Ѷȣ�һ��
4��ѡ���� ���ڶ�����Ԫ�ص���
A��K
B��Ca
C��I
D��P
�ο��𰸣�D
���������������Ԫ��ָԪ�����ڱ��е�һ�����������ڣ�ȷ��Ԫ�ص�������������Ԫ��������=���Ӳ���������������=���������ɴ��жϣ�P�ڵ�3���ڢ�A�壬����ѡD��������Ԫ�ض��ڳ����ڡ�
�����Ѷȣ���
5������� ��10�֣���֪A��B��C��D���ֶ�����Ԫ����Ԫ�����ڱ��е����λ������ͼ��ʾ�����ǵ�ԭ������֮��Ϊ46������գ�
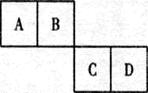
��1��BԪ�ص�����Ϊ??DԪ�ص�ԭ�ӽṹʾ�� ͼΪ?��
��2��B�ж������������֮һ��һ����ɫ���塣�������ڿ����л�Ѹ�ٱ�ɺ���ɫ����һ�������£�4L�ĸ���ɫ������3L���������ϣ���������ˮ������գ���ֻ����һ��B�ĺ����ᣬ�ú�����Ļ�ѧʽΪ ?��
��3�����Ӱ뾶��D��?C2�������������������������������ԭ�ԣ�D��?C2�����������������������������
�ο��𰸣��� ÿ��2�ֹ�10�֣���1������ ��2��HNO3��3��D����C2����D����C2��
��2��HNO3��3��D����C2����D����C2��
�����������1������A��B��C��D���ֶ�����Ԫ����Ԫ�����ڱ��е����λ�ÿ�֪�������A��ԭ��������x����B��x��1��C��x��10��D��x��11������x��x��1��x��10��x��11��46�����x��6������A��̼Ԫ�أ�B�ǵ�Ԫ�أ�C��SԪ�أ�D����Ԫ�ء�
��2���������ڿ����л�Ѹ�ٱ�ɺ���ɫ����˵����������NO������NO�����������֮����4:3�������ڷ�Ӧ�еõ�4�����ӣ����Ը��ݵ��ӵĵ�ʧ�غ��֪��NO�����������е�Ԫ�صĻ��ϼ��ǣ�5�ۣ����������ᡣ
��3����������Ų���ͬ�����������Ӱ뾶��ԭ���������������С�������Ӱ뾶��D����C2�����ǽ�����Խǿ����Ӧ�����ӵĻ�ԭ��Խ������ԭ����D����C2����
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�������������ѧ����������������Ӧ��������������Ҫ��Ԫ�ء�λ�������ԡ����߹�ϵ���ۺϿ��飬�Ƚ�ȫ�濼��ѧ���й�Ԫ���ƶ�֪ʶ���������֪ʶ�������������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬����ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������
�����Ѷȣ�һ��