微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据电子排布的特点,Cu在周期表中属于
A.s区
B.p区
C.d 区
D.ds区
参考答案:D
本题解析:略
本题难度:简单
2、选择题 下列说法正确的是
A.Na+、Fe3+、Cl 、SCN
、SCN 能大量共存于同一溶液中
能大量共存于同一溶液中
B.碳酸氢钠溶液与足量的氢氧化钡溶液混合后,其离子方程式为:HCO3 + Ba2+ + OH
+ Ba2+ + OH ="=" BaCO3↓+H2O
="=" BaCO3↓+H2O
C.若R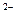 和M+的电子层结构相同,则原子序数的比较为:R>M
和M+的电子层结构相同,则原子序数的比较为:R>M
D.若X原子中的质子数为a,中子数为b,则X的质量数为: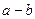
参考答案:B
本题解析:略
本题难度:一般
3、选择题 下表给出了X、Y、Z、W四种短周期元素的部分信息,请根据这些信息判断下列说法中正确的是(?)?
元素
| X
| Y
| Z
| W
|
原子半径(nm)
| 0.102
| 0.16
| 0.074
| 0.071
|
最高正价或最低价
| +6
| +2
| -2
| -1
|
A.原子序数X<Y<W<Z
B.纯净的X与纯净的Z反应生成XZ3
C.Z的最高正价为+6
D.HW是热稳定性最强的氢化物
参考答案:D
本题解析:由最高正价或最低负价,结合原子半径、短周期元素等条件可推出X是硫,Y是镁,Z是氧,W是氟。硫在氧气中燃烧只能得到SO2,O元素的非金属仅次于氟,目前还没有发现氧元素有+6价,氟是非金属性最强的元素,HF是稳定性最强的氢化物。
本题难度:简单
4、选择题 六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期。已知常温下单质A与E的状态不同,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料。则下列推断中正确的是
A.A、C两种元素可组成化学式为CA4的化合物
B.F与D形成的化合物性质很不活泼,不与任何酸反应
C.原子半径由大到小的顺序是E>F>C>D
D.元素的非金属性由强到弱的顺序是D>C>F>B
参考答案:C
本题解析:由题干信息知A是H、B是C、C是N、D是O、E是Na、F是Si。A、C两种元素可组成化学式为CA3的化合物,A错误;SiO2可以与HF反应,B错误;原子半径Na>Si>N>O,C正确;元素的非金属性O>N>C>Si,D错误。答案选C。
点评:元素的性质随着原子序数的递增而呈现出周期性的变化,称为元素周期律。元素的性质主要是指原子半径、主要化合价和金属性以及非金属性等。该题主要考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
5、选择题 X是第三周期非金属元素,该原子如果要达到8电子稳定结构,需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是
A.X最高价氧化物对应的水化物不一定是强酸
B.X元素的氢化物化学式一定为H2X
C.X的单质―定是良好的半导体材料
D.X元素的氧化物―定能与烧碱反应
参考答案:AD
本题解析:根据已知位、构、性方面的信息推断,X为Si或S。最高价氧化物对应的水化物为H2SiO3或H2SO4,前者是弱酸,后者是强酸,故A正确;气态氢化物为SiH4或H2S,故B错误;单质为Si或S,前者是半导体材料,后者是绝缘体材料,故C错误;氧化物为SiO2或SO2、SO3,都是酸性氧化物,故D正确。
本题难度:一般