微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
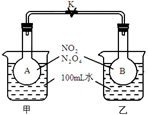
1、填空题 (10分)已知NO2转化为N2O4的反应是放热反应且是可逆反应:2NO2 (g) N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。
N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。
 ?
?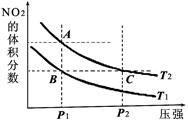
图1?图2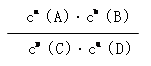
(1)图1中___________瓶中气体颜色更深?(填“A”或“B”)。请比较平衡时反应速率:A瓶__________B瓶;(填“>”“<”或“=”)
(2)在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如上图2所示。请比较图2中A、B两点混合气体的平均相对分子质量:A点_________B点。(填“>”“<”或“="”" )
(3)平衡常数定义为一定条件下,可逆反应平衡时产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积比。即aA(g)+bB(g)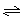 pC(g)+qD(g)中K=
pC(g)+qD(g)中K= 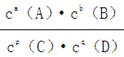
下如:N2(g)+3H2(g)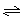 2NH3(g)的平衡常数表示式K=
2NH3(g)的平衡常数表示式K=
①2NO2 (g) N2O4(g)的平衡常数表达式K=?
N2O4(g)的平衡常数表达式K=?
②平衡常数K的具体值会随温度而改变。请比较上图2中A点和B点所对应的平衡常数数值。A点____________B点(填“>”“<”或“=”)。
参考答案:(1)B?<?(2)<?(3)①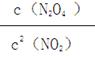 ?②<
?②<
本题解析:(1)由于反应是放热反应,所以温度低有利于平衡向正反应方向移动,即甲中颜色更深。乙中温度高,反应速率大。
(2)在压强相同是,温度为T2的NO2体积分数大,说明温度是T2大于T1,即A点气体的物质的量多,因此A点混合气的平均相对分子质量小。
(3)①根据平衡常数的概念可知,该反应的平衡常数表达式为K= 。
。
②由于温度是T2大于T1,而温度低有利于平衡向正反应方向移动,所以B点平衡常数大。
本题难度:一般
2、填空题 在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)  ?3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
?3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
(1)达到平衡时,C在反应混合气中的体积分数是?(用含字母a的代数式表示)。
(2)在相同实验条件下,若在同一容器中改为加入2molA和6 mol B,达到平衡后,C的物质的量为?mol(用含字母a的代数式表示)。此时C在反应混合气中的体积分数与原平衡相比?(选填“增大”“减小”或“不变”)。
(3)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要求平衡后C在反应混合气中体积分数仍与原平衡相同,则还应加入C?mol。
(4)在同一容器中加nmolA和3n molB,则平衡时C的物质的量为mmol,若改变实验条件,可以使C的物质的量在m~2m间变化,那么,n与m的关系是_____________。(用字母n、m关系式表示)
参考答案:(1)25a%(2)2a 不变(3)6
本题解析:(1)根据反应方程式,由生成了amolC,可知A反应了a/3mol,B反应了 2a/3mol,平衡时A为(1-a/3)mol,B为(3-2a/3)mol,C为amol,可计算出C的体积分数为25a%。(2)本题达平衡时与(1)小题达平衡时,互为等效平衡。则相同组分的体积分数相同,C的物质的量为2amol。(3)据恒温恒容下反应前后气体分子数不变的同一可逆反应的等效平衡规律,即通过反应的化学计量数比换算(极限假设转换)成反应式同一侧的反应物或生成物,其物质的量之比相同,二平衡等效,可设加入C xmol,xmolC完全换算成A、B后共有(2+x/3)molA,(8+2x/3)molB,由(2+x/3):(8+2x/3)=1:3,解得x=6。(4)n>[2/3]m
本题难度:一般
3、选择题 物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2 1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2 1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是

A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0375mol・L-1・min-1
B.保持其他条件不变,若此时再向正庚烷反应体系中加入正庚烷,平衡向生成(t-BuNO)2的方向移动
C.保持其他条件不变,升高温度,(t-BuNO)2的平衡转化率大于75%,则其能量关系可用右图表示
D.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率大于75%
参考答案:C
本题解析:A、(t-BuNO)2的转化量为1.0×75%=0.75mol,ν(t-BuNO)=2(t-BuNO)2=2×0.75÷2÷10=0.075mol・L-1・min-1,错误;B、体系中加入不反应的气体,反应物浓度不变,平衡不移动,错误;C、升高温度,反应物转化率增大平衡正向移动,反应吸热,正确;D、在正庚烷k=(1.5/2)2÷0.25/2=4.5大于在CCl4中平衡常数,平衡逆向移动,转化率减小,错误。
本题难度:一般
4、计算题 在2L的密闭容器中充入一定量的SO3,在一定温度和催化剂作用下,发生反应:2SO3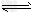 2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求:
2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。求:
(1)n(SO2);
(2)氧气的生成速率v?(O2);
(3)SO3的转化率;
参考答案:(1)1.6mol
(2)v?(O2)=0.1?mol?/(L・min)
(3)20%
本题解析:
本题难度:一般
5、选择题 在2L恒容密闭容器中发生反应:2A(g)+B(g)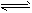 2C(g),若最初加入的A和B都是4mol,10 s后反应达到平衡,此时间段A的平均反应速率是0.12mol・L-1・s-1,则平衡后,容器中B的物质的量浓度为
2C(g),若最初加入的A和B都是4mol,10 s后反应达到平衡,此时间段A的平均反应速率是0.12mol・L-1・s-1,则平衡后,容器中B的物质的量浓度为
[? ]
A.2.8 mol・L-1
B.1.4 mol・L-1
C.3.2 mol・L-1
D.3.6 mol・L-1
参考答案:B
本题解析:
本题难度:简单