微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式不正确的是
A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH=Mg2++2CH3COO-+2H2O
B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO4-+3H2O2+6H+=2Mn2++6H2O+4O2↑
C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42―恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O
2、选择题 下列离子方程式正确的是
A.向水中通入氯气:Cl2+H2O===2H++Cl-+ClO-
B.碳酸钠溶液中通入二氧化碳:CO3来源:91考试网 www.91eXam.org2-+CO2+H2O ===2HCO3-
C.实验室制备氯气:MnO2+4HCl(浓)=== 2Mn2++2H2O+2Cl2↑
D.稀硫酸与氢氧化钡溶液反应:H++ SO42-+Ba2++OH-=BaSO4↓+H2O
3、选择题 下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效: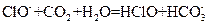
B. 溶液中加入过量的浓氨水: Al3++4NH3・H2O=AlO2-+4NH4++2H2O
溶液中加入过量的浓氨水: Al3++4NH3・H2O=AlO2-+4NH4++2H2O
C.等体积、等浓度的 稀溶
稀溶 液与
液与 稀溶液混合:
稀溶液混合:
Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3・H2O+H2O
D.向沸水中滴加FeCl3饱和溶液制取Fe(OH)3胶体:Fe3+ +3H20  Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
4、填空题 研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如下:

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。PbO2的氧化性大于MnO2。PbSO4是一种微溶物质。有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
离子
| 离子半径(pm)
| 开始沉淀
时的pH
| 完全沉淀
时的pH
|
Fe2+
| 74
| 7.6
| 9.7
|
Fe3+
| 64
| 2.7
| 3.7
|
Al3+
| 50
| 3.8
| 4.7
|
Mn2+
| 80
| 8.3
| 9.8
|
Pb2+
| 121
| 8.0
| 8.8
|
Ca2+
| 99
| -
| -
|
?

请回答下列问题:
(1)写出浸出过程中生成Mn2+反应的化学方程式?。
(2)氧化过程中主要反应的离子方程式?。
(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是?,应调节pH的范围为?。
(4)阳离子吸附剂可用于除去杂质金属离子。请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有?、?等;吸附步骤除去的主要离子为:?。
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10―6。现将c mol・L―1CaCl2溶液与2.00×10―2 mol・L―1Na2SO4溶液等体积混合(忽略体积的变化),则生成沉淀时,c的最小值是 。
5、填空题 (1)将NaHSO4溶液滴加到滴有酚酞试液的Ba(OH)2溶液中,当溶液的颜色刚好由红色变为无色时,反应的离子方程式为______.
(2)向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,写出反应的离子方程式______.
在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为______.