��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �йؼ����������±���ʾ:

�������������ȼ�յ��Ȼ�ѧ����ʽΪ
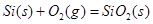 ;
;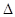 H="-989.2"
H="-989.2" 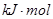
 ��x��ֵΪ����(��?��)
��x��ֵΪ����(��?��)
A��460��
B��920
C��1 165.2����
D��423.3
�ο��𰸣�A
�����������Si�����У�һ����ԭ����4����ԭ�ӳɼ���ÿ����ѧ����������ԭ�ӹ��ã����൱��ÿ����ԭ����ȫռ��������ѧ�����ʷ�Ӧ��1mol�裬��Ҫ����2mol��Si-Si������1mol��SiO2�γ�4mol��Si-O���������յ�������ȥ�ų��������û�ѧ��Ӧ�ġ�H����H=2��176KJ/mol+498.8KJ/mol-4xKJ/mol=-989.2KJ/mol��x=460KJ/mol
�����Ѷȣ�һ��
2��ѡ���� ���ʯ��ʯī��̼Ԫ�ص����ֽṹ��ͬ�ĵ��ʡ���100kPaʱ��1molʯīת��Ϊ���ʯ��Ҫ����1.895kJ���������ݴˣ����ж���100kPaѹǿ�£�����˵����ȷ���ǣ�������
A��ʯī�Ƚ��ʯ�ȶ�
B�����ʯ��ʯīʯ�ȶ�
C��1molʯī��1mol���ʯ����������
D��1molʯī�ͽ��ʯ��ȫȼ��ʱ�ͷŵ�����ʯī�Ƚ��ʯ��
�ο��𰸣�A
�����������100kPaʱ��1molʯīת��Ϊ���ʯ��Ҫ����1.895kJ������������ʯī�������ϵͣ�C����ʯī�Ƚ��ʯ�ȶ���A��ȷ��1molʯī�ͽ��ʯ��ȫȼ��ʱ�ͷŵ�����ʯī�Ƚ��ʯ�٣�D����
�����Ѷȣ�һ��
3��ѡ���� ��֪C��s��ʯī����C��s�����ʯ��-1.9KJ����֪���ʯ�ܶȸ�����?C��s��ʯī����C��s�����ʯ���ıȽϣ���ȷ���ǣ�������
A��������ʱ�������������߸��ȶ�
B��������ʱ��ǰ���ڿ�������ȫȼ�շ��ȸ���
C�����¸�ѹ������ǰ��ת��Ϊ����
D��ǰ���ۻ�ֻ���ƻ����»��������������ƻ����ۼ�
�ο��𰸣�C��s��ʯī����C��s�����ʯ����H=1.9KJ/mol��ʯī���ɽ��ʯ���ȣ�˵��ʯī�����ͣ����ʯ�����ߣ�����Խ��Խ���ã�����Խ��Խ�ȶ���
A��������ʱʯī�������ڽ��ʯ����ʯī���ȶ�����A����
B��ʯī�ͽ��ʯ����̼�ĵ��ʣ�������ʱȼ�ս��ʯ�ų������࣬��B����
C����ƽ�������ȷ�Ӧ������ƽ��������У�ʯī�Dz�״�ṹ����״֮����Ҫ����Ϊ���Ӽ���������Ҳ���Ƿ��»��������ʯ��Ҫ����Ϊԭ�Ӽ����������ṹ���ܴܺ��Ҽ����̣����Ը��¸�ѹ����ʯīת���ɽ��ʯ����C��ȷ��
D��ʯī�Dz�״�ṹ������Ƿ��»�����ÿ�����ǹ��ۼ������ʯ�ǹ��ۼ������γɵĿռ���״�ṹ���ۻ�ʱʯī�ƻ��˷��»������ۼ������ʯ�ƻ��˹��ۼ�����D����
��ѡC��
���������
�����Ѷȣ�һ��
4��ѡ���� �йؼ������������
��ѧ��
| Si��O
| O=O
| Si��Si
|
����kJ��mol-1
| X
| 498��8
| 176
|
�������������ȼ�յ��Ȼ�ѧ����ʽ��Si��s��+O2��g���TSiO2��s��?��H= ��989��2 kJ��mol-1�������X��ֵΪ(? )
A��423��3? B��460? C��920? D��1165��2
�ο��𰸣�B
���������
��ȷ�𰸣�B
��H=��Ӧ�����֮�ͼ�ȥ���������֮��
=2��176 kJ��mol-1��498.8 kJ��mol-1�D4X=��H= ��989��2 kJ��mol-1
X= 460kJ��mol-1
�����Ѷȣ�һ��
5��ѡ���� ����˵�����ʾ������ȷ����(? )
A�������ʵ������������������ֱ���ȫȼ�գ����߷ų�������
B����C��ʯī��= C�����ʯ������H =" +1.90" kJ��mol-1��֪�����ʯ��ʯī�ȶ�
C����ϡ��Һ�У�H+��aq��+ OH-��aq��= H2O��l������H =" -57.3" kJ��mol-1��������0.5 mol H2SO4��Ũ�����뺬1 mol NaOH����Һ��ϣ��ų����ȴ���57.3 kJ
D����101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+ O2��g��= 2H2O��l������H =" -285.8" kJ��mol-1
�ο��𰸣�C
�����������̬����������ڹ�̬��ģ����Ե����ʵ������������������ֱ���ȫȼ�գ�ǰ�߷ų������࣬A����ȷ��B�з�Ӧ���ȣ�������������ߣ�����ʯī�Ƚ��ʯ�ȶ���B����ȷ��Ũ��������ˮ���ȣ�����ѡ��C��ȷ��D�У���Ӧ�ȵ���ֵ���ԣ�����ȷ����ѡC��
�����Ѷȣ�һ��