微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 下表列出了A~R?9种元素在周期表中的位置
| 周期族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0
2
E
F
3
A
C
D
G
R
4
B
H
|
用元素符号填写下空:
(1)这9中元素中金属性最强的是______;
(2)化学性质最不活泼的元素是______;
(3)G的最高价含氧酸的化学式是______;
(4)E的最简单氢化物的化学式______;
(5)A在F中燃烧得到产物的化学式______;
(6)C与D的原子半径比较:R(C)______R(D)(填“>”或“<”)
2、推断题 有A、B、C、D、E六种元素,原子序数依次增大,位于不同的三个短周期,其中B与D可形成DB2、
DB3化合物,在同周期元素中,C的金属性最强,E的非金属性最强;请回答:
(1)写出A、C、E三种元素的元素符号
A__________C__________E__________
(2)A、B形成的化合物与DB2反应生成一种强酸的化学方程式为____________________
(3)已知DB2在一定条件下可转化为DB3(g),1molDB2完全反应,放出98.3kJ的热量。该反应的热化学方程式是____________________,工业上进行这一反应的设备是__________,反应的适宜条件为
_________________。
(4)用铂作电极电解由C、E形成化合物的饱和溶液时,检验阳极产物的实验方法为________________;电解一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是____________________。 若改用铁棒做阳极材料,则阳极的电极反应式为____________________。阴极反应式为____________________。
3、选择题 判断下列元素中不属于主族元素的是( )
A.磷
B.钙
C.铁
D.碘
4、选择题 下列各种性质的比较中.正确的是
A.分子的稳定性:HF>H2O>NH3
B.熔点:金刚石>汞>硫
C.离子的半径:Cl->Al3+>Na+
D.沸点:AsH3>PH3>NH3
5、推断题 (三选一)【物质结构与性质】
原子序数依次递增的A、B、C、D、E是周期表中前30号元素。已知A的最外层电子数是其内层电子数的2倍;A与C形成的常见化合物之一是主要的温室气体;D与A同主族,其单质在同周期元素所形成的单质中熔点最高;E原子M能?层为全充满状态,且核外的未成对电子只有一个。请回答下列问题:
(1)B在周期表中的位置是___________,该主族元素的气态氢化物中,沸点最低的是__________(填化学式)。
(2)根据等电子原理分析,BC2+?中B原子的轨道杂化类型是____________。
(3)五种元素中,电负性最大与最小的两种非金属元素形成的化合物在常温下是晶体,其晶体类型是____________。
(4)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测D元素的电离能突增应出现在第______电离能。
(5)A的一种相对分子质量为28的氢化物,其分子中σ键与π键的个数之比为________;A能形成多种常见单质,在熔点最低的单质中,每个分子周围紧邻的分子数目为___________;?
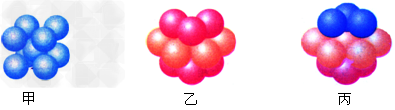
(6)E的基态原子有_____种形状不同的原子轨道;E2+?的价电子排布式为_______;下图_______(填甲、乙或丙)表示的是E晶体中微粒的堆积方式。