��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����A��B��C��D��E��������Һ���ֱ���K+��NH4+��Ag+��Ba2+��Al3+��Cl-��Br-��CO32-��SO42-��NO3-?�е������Ӻ������Ӹ�һ����ɣ��������������������Ӹ�����ͬ����֪��
��A+B����ɫ����?��A+D����ɫ����?��A+C����ɫ����
��D+B����ɫ����+��ɫ����?��A��Һ��c��H+��=c��OH-��
��B��Һ��c��H+��=1��10-12mol?L-1?��C��D��E������Һ��pH��7��
��������ʵ����ʵ�����Ƴ����÷���ʽ��ʾ��
AΪ______��BΪ______��CΪ______��DΪ______��EΪ______��
д�����Ϣ٢ڢܸۢ�����Ӧ�����ӷ���ʽ��
��______����______��
��______����______��
�ο��𰸣���1����������C��D��E������Һ��pH��7��˵��C��D��E������ҺΪǿ�������Σ�ˮ������ԣ�B��Һ�ʼ��ԣ�A��Һ��c��H+��=c��OH-����Ag+����Cl-��Br-��SO42-��CO32-���ϣ���ΪAgCl��Ag2SO4��Ag2CO3��Ϊ��ɫ������AgBrΪdz��ɫ������ֻ���γ������������Ʋ�֪AΪ������Һ��ֻ���Ȼ�����������������B��Һ�ʼ��ԣ�BΪǿ�������Σ���K+��Ba2+Ϊǿ�������ӣ�CO32-Ϊ��������ӣ����Bֻ��ΪK2CO3������B��D��Ӧ���ɰ�ɫ���������壬B�к�CO32-��������CO32-��Ӧ���ɳ�������Al3+��Ag+��Ba2+������CO32-��Al3+����˫ˮ�ⷴӦ�������ɳ��������������壬���ӷ�ӦΪ2Al3++3CO32-+3H2O�T2Al��OH��3��+CO2��������D�к�Al3+����DΪǿ��������������Һ���������ΪCl-��Br-��SO42-�е�һ�֣���Ϊ������������A�ɷֱ���C��B��D��Ӧ���ɰ�ɫ������BΪK2CO3��DΪ��������C��ֻ������������
�ʴ�Ϊ��A��BaCl2��B��K2CO3��C��AgNO3��D��Al2��SO4����E��NH4Br��
��2��
���������ӿ���ΪAg+��Ba2+�е�һ�֣�����Ϊǿ�������Σ��ʿ�ȷ�����к�Ag+��ֻ��ΪAgNO3����Ϊǿ�������Σ�����ֻ�ܺ�NH4+����Ϊ������Һ��Ϊǿ��ǿ���Σ���ȷ������ֻ�ܺ�Ba2+����Ϊ��ΪAgNO3����ס��ҡ�����Ӧ���ɰ�ɫ������
��Ag+��Ӧ���ɰ�ɫ���������������Cl-��SO42-��CO32-�����к�Ba2+�����Ա�ΪBaCl2�����к�Al3+��
���Լ�ΪAl2��SO4��3��������к�NH4+����֮��ϵ��������ΪBr-������ΪNH4Br��
�ʴ�Ϊ��Al2��SO4��3��K2CO3��BaCl2��AgNO3��NH4Br��
��2���٢ڢܸۢ�����Ӧ�����ӷ���ʽ�ֱ�Ϊ����Ba2++CO32-�TBaCO3��?��Ba2++SO42-�TBaSO4��?��Ag++Cl-�TAgCl��
��2Al3++3CO32-+3H2O�T2Al��OH��3��+3CO2����
�ʴ�Ϊ����Ba2++CO32-�TBaCO3������Ba2++SO42-�TBaSO4������Ag++Cl-�TAgCl����
��2Al3++3CO32-+3H2O�T2Al��OH��3��+3CO2����
���������
�����Ѷȣ�һ��
2��ѡ���� ��20mL?0.1mol/L�ĺ�����HXR04��Һ��15mL?0.2mol/L��ij��M��0H��a��Һǡ����ȫ��Ӧ��ȫ���������Σ���RԪ�صĻ��ϼ��ǣ�������
A��+��8-
��
B��+��8-2a��
C��+��8-��
D��+��8-3a��
�ο��𰸣�20mL?0.1mol/L�ĺ�����HXR04��Һ��n��HXR04��=0.02L��0.1mol/L=0.002mol����n��H+��=xn��HXR04��=0.002xmol��
15mL0.2mol/L��M��0H��a��Һ��n[M��0H��a]=0.015L��0.2mol/L=0.003mol����n��OH-��=an[M��0H��a]=0.003amol��
����HXR04���M��0H��aǡ����ȫ��Ӧ��ȫ���������Σ���n��H+��=n��OH-������0.002xmol=0.003amol�����x=3a2��
��HXR04��RԪ�صĻ��ϼ�Ϊm�����ݻ��ϼ۴�����Ϊ0�У�3a2+m+4����-2��=0�����m=+��8-3a2����
��ѡC��
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��ȷ����?��?��
A������CO2ͨ�����ʯ��ˮ�У�CO2 + Ca2+ + 2OH��= CaCO3�� + H2O
B��Na2O2��ˮ������Ӧ��O22��+ H2O = 2OH��+ H2��
C����AlCl3��Һ�м��������NaOH��Һ�� Al3+ + 3OH��= Al(OH)3��
D��Ca(HCO3)2��������NaOH��Һ��Ӧ�� Ca2+ + 2HCO3��+ 2OH��= CaCO3��+ CO32��+ 2H2O
�ο��𰸣�D
���������A����ȷ���ӷ���ʽΪCO2 + OH��= HCO3-;B��Ϊ2Na2O2+2H2O=4Na++4OH-+O2��;C��ΪAl3+ + 4OH��= AlO2-+2H2O��
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��ȷ����
[? ]
A��ʵ�����ô���ʯ����ᷴӦ��ȡ������̼��CaCO3+2H+ = Ca2++CO2��+H2O
B��������������������Һ����:��CH2ClCOOH+OH- ��CH2ClCOO-+H2O
C����������Һ��ͨ������������̼��2C6H5O-+CO2+H2O �� 2C6H5OH+CO
D����������Һ������ȩ�е�ȩ����CH3CHO +2[Ag(NH3)2]++2OH-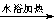 CH3COO-+ NH4++3NH3+2Ag��+H2O
CH3COO-+ NH4++3NH3+2Ag��+H2O
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5������� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A������Ͷ�뵽����NaOH��Һ�У�2Al+2OH-=2AlO2-+H2��
B��������ˮ��Ӧ��Cl2+H2O=2H++Cl-+ClO-
C��AlCl3��Һ�м��������İ�ˮ��Al3++3OH-=Al��OH��3��
D�����ۼ������Ȼ�����Һ�У�Fe+2Fe3+=3Fe2+
�ο��𰸣�A����ʧ���Ӳ���ȣ���ȷ�����ӷ���ʽΪ2Al+2OH-+2H2O=2AlO2-+3H2������A����
B��HClOΪ������ʣ���ȷ�����ӷ���ʽΪCl2+H2O=H++Cl-+HClO����B����
C����ˮΪ������ʣ�����ȷ�����ӷ���ʽΪAl3++3NH3?H2O=Al��OH��3��+3NH4+����C����
D��Fe3+���������ԣ���Fe��Ӧ����Fe2+����Ӧ�����ӷ���ʽΪFe+2Fe3+=3Fe2+����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��