| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《物质的量》考点特训(2017年冲刺版)(六)
参考答案:D 本题解析:Al(OH)3是两性氢氧化物,会溶解于NaOH溶液,所以AlCl3的溶液中加入足量NaOH溶液得到的是Na AlO2,A错;浓硫酸反应后浓度会变小,能有多少的硫酸与铜反应无法确定,B错;1mol的碳酸钾固体中缓缓滴加0.2mol的稀盐酸,碳酸钾过量,生成的是KHCO3,C错;设烧瓶的体积为VL,则HCl气体的物质的量为V/22.4mol,做喷泉实验,当水充满整个烧瓶后盐酸的浓度为:V/22.4mol÷VL=(1/22.4)mol/L,D正确。 本题难度:一般 2、选择题 实验中需0.5 mol/L的NaOH溶液230 mL,配制时应选用容量瓶的规格和称取NaOH的质量分别是 参考答案:B 本题解析: 本题难度:简单 3、选择题 在KCl、MgSO4、MgCl2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(SO42-)为 |
参考答案:B
本题解析:根据溶液中的电荷守恒,0.1×1+0.25×2=0.2×1+c(SO42-)×2,解c(SO42-)=0.20mol/L,选B。
考点:电荷守恒。
本题难度:一般
4、选择题 设NA为阿伏加德罗常数,下列说法正确的是(? )
A.常温常压下,1.6 g O2和O3混合气体中原子总数为0.1NA
B.标准状况下,过氧化钠与水反应生成1.12 L氧气时转移电子数目为0.2NA
C.0.1 mol・L的CH3COONa溶液中CH3COOH和CH3COO-总数为0.1NA
D.常温常压下,4 g He中,含有的原子数为2NA
参考答案:A
本题解析:A:混合气体中均为O原子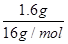 ="0.1" mol;B:2Na2O2+2H2O=4NaOH+O2↑,Na2O2发生了自身氧化还原反应,每生成1mol氧气有2mol电子的转移,故当有1.12 L氧气时转移电子数目为0.1NA;C:溶液体积未指明,无法计算出离子的量;D:氦为单原子分子,4 g He也就是1 mol,原子数也为1 mol
="0.1" mol;B:2Na2O2+2H2O=4NaOH+O2↑,Na2O2发生了自身氧化还原反应,每生成1mol氧气有2mol电子的转移,故当有1.12 L氧气时转移电子数目为0.1NA;C:溶液体积未指明,无法计算出离子的量;D:氦为单原子分子,4 g He也就是1 mol,原子数也为1 mol
本题难度:一般
5、选择题 有五瓶溶液分别是①10mL0.60mol?L
参考答案:
本题解析:
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点总结《苯和芳香烃.. | ||