��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���й���ŨHNO3��ŨH2SO4��������ȷ����
A�������¶�����п����������
B�������¶�����ͭ�Ͽ췴Ӧ
C�����ӷ�
D��¶���ڿ����У���ҺŨ�Ⱦ�����
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ʵ���� ijѧ������С��������ͼ��ʾװ�÷ֱ�������ʵ�飺
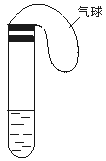
(1)���Թ���ע��ij��ɫ��Һ�������Թܣ���Һ��ɫ��dz����ȴ��ָ���ɫ����ԭ��Һ������?��Һ������ʱ��Һ�ɺ�ɫ��dz��ԭ����?��
(2)���Թ���ע��ij��ɫ��Һ�������Թܣ���Һ��Ϊ��ɫ����ȴ��ָ���ɫ�������Һ������?��Һ������ʱ��Һ����ɫ��Ϊ��ɫ��ԭ����?��
�ο��𰸣�(1)ϡ��ˮ�ͷ�̪?ϡ��ˮ�е�NH3�����ݳ���������Һ����ɫ��dz? (2)����SO2�����Ʒ��? SO2�����ݳ���Ʒ����Һ�ָ���ɫ
������������⿼��ѧ����ʵ�������ж�ʵ��ԭ����ֱ��������˼ά����������Ҫ����ʵ���װ��Ϊһ�����ϵ������ʱ�����������Һ���ݳ�������������Һ����ɫ�ı仯����ȴ���ݳ����������ܽ�����Һ�У��õ�ԭ����Һ���ָ���ԭ����Һ����ɫ������ѧ�Σ���Ϊ�����������ݳ���������Һ��ɫ������������SO2��Ʒ����Һ֮���Լ�NH3���̪��Һ֮�䣬Ȼ���������������з�������֤����ɡ�
�����Ѷȣ���
3������� ��6�֣�ֱ���ŷź�SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2.��
(1) ���Ƽ�ѭ�����У�Na2SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ��?

�����ϱ��ж�NaHSO3��Һ��?�ԣ��û�ѧƽ��ԭ�����ͣ�������������������
�ڵ�����Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ):��������������������
a��c(Na��) = 2c(SO32��)��c(HSO3��)
b��c(Na��)>c(HSO3��)>c(SO32��)>c(H��) = c(OH��)
c��c(Na��)��c(H��)=c(SO32��)��c(HSO3��)��c(OH��)
�ο��𰸣���6�֣�(1) ?SO2��2OH��= SO32����H2O ?
��2����? HSO3-���ڣ�HSO3- SO32-+H+��HSO3-+H2O
SO32-+H+��HSO3-+H2O H2SO3+OH-��HSO3-�ĵ���̶�ǿ��ˮ��̶�? ab
H2SO3+OH-��HSO3-�ĵ���̶�ǿ��ˮ��̶�? ab
�����������1������������ǿ�SO2������������ܱ�����������Һ���գ���Ӧ�Ļ�ѧ����ʽ��SO2��2OH��= SO32����H2O��
��2������NaHSO3-Һ�д��ڣ�HSO3- SO32-+H+��HSO3-+H2O
SO32-+H+��HSO3-+H2O H2SO3+OH-�����ݱ��е����ݿ�֪����SO32����HSO3�������ʵ�����1�U1�������£���Һ�������Եģ���˵��HSO3���ĵ���̶ȴ���SO32����HSO3����ˮ��̶ȣ������Һ�������Եģ�����NaHSO3��Һ�����ԡ�
H2SO3+OH-�����ݱ��е����ݿ�֪����SO32����HSO3�������ʵ�����1�U1�������£���Һ�������Եģ���˵��HSO3���ĵ���̶ȴ���SO32����HSO3����ˮ��̶ȣ������Һ�������Եģ�����NaHSO3��Һ�����ԡ�
�ڸ��ݵ���غ��֪��c(Na��)��c(H��)=2c(SO32��)��c(HSO3��)��c(OH��)�����������Һ�����ԣ���c(H��) = c(OH��)��c(Na��) = 2c(SO32��)��c(HSO3��)��a��ȷ��c����ȷ�����ڲ�����ˮ��ǵ��룬��̶ȶ��Ǻ����ģ�����bҲ����ȷ�ģ���ѡab��
���������ж�����Ũ�ȴ�Сʱ��Ӧ�����úõ���ء������غ�������غ�Ȼ������ɡ�
�����Ѷȣ�һ��
4������� ������������+4�۵������������������л�ԭ�ԡ������Լ�����ˮ��������Һ��Na2SO4��ϡH2SO4��NaOH��Һ����ˮ��
(1)Ҫ֤��Na2SO3���л�ԭ�ԣ�Ӧѡ�õ��Լ���________��������������________����Ӧ�����ӷ���ʽΪ_______________��
(2)Ҫ֤��Na2SO3����������________��Ӧѡ�õ��Լ���_________��������������_______����Ӧ�����ӷ���ʽΪ_______________��
�ο��𰸣�(1)��ˮ?��ˮ��ɫ? +Br2+H2O
+Br2+H2O
 +2Br-+2H+
+2Br-+2H+
(2)Na2S��ϡH2SO4��Һ�����2S2-+ +6H+
+6H+ 3S��+3H2O
3S��+3H2O
���������(1)��֤��Na2SO3���л�ԭ�ԣ�����һ����������֮��Ӧ����Ҫ������������(2)��֤��Na2SO3���������ԣ�����һ�ֻ�ԭ����֮��Ӧ������Ҳ������������+4����ֻ����-2��������ʱ�ű��������ԡ�
�����Ѷȣ���
5��ʵ���� Ϊ̽���������Ƶ����ȶ��ԣ�ij�о���ѧϰС�齫��ˮ�������Ƹ����������ȣ����������Ⱥ�Ĺ�����������ͼ��ʾ��ʵ��װ�ý���ʵ�顣��ش������й����⣺
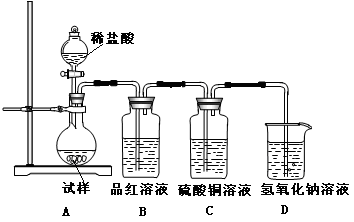
��1����ij�ֹ����������ȷ����˷ֽ⣬����˵����ȷ���ǣ�?��
A����ּ��Ⱥ�һ���й������? B������ǰ�������ɫһ���ޱ仯
C������ǰ���������һ���б仯? D��һ���������µ�����
E����ּ��Ⱥ�õ��IJ�������һ��Ϊ�����
��2���������ϣ���ˮ�������Ƹ����������ȵ�600��ſ�ʼ�ֽ⣬�ҷֽ����ֻ�����ƺ�����һ�ֹ���,��Na2SO3������ȵ�600�����Ϸֽ�Ļ�ѧ����ʽ?����������¶ȵ���600�棬�����ù��������л����μ�ϡ�������������ڵμ�ϡ���������������HSO3�������ʵ���Ũ�ȱ仯����Ϊ?��
��3����������¶ȸ���600��һ��ʱ��������ù��������л����μ�ϡ�������������۲쵽��ƿ�г��ֵ���ɫ���������д������ݲ�������������������ᷴӦ���ɵ���ɫ���������ӷ���ʽΪ?����ʱ��B��C��װ���п��ܹ۲쵽������Ϊ?��
��4���ڣ�3���еμ������������ƿ�ڳ�Cl���⣬��������һ��Ũ�Ƚϴ�������ӣ�X����Ϊ����������ӣ�X������ȡ������������ˮ�����Һ�������Ǽ��������ӣ�X��������ʵ�鷽��������Ϊ�����ķ�����?����ס����ҡ�������˵����һ������������ԭ�� ?��
�����ף�ȡ����������Һ���Թ��У��ȼ�ϡHNO3���ټ�BaCl2��Һ���а�ɫ�������ɣ�֤�������Ӵ��ڡ�
�����ң�ȡ����������Һ���Թ��У��ȼ�ϡHCl���ټ�BaCl2��Һ���а�ɫ�������ɣ�֤�������Ӵ��ڡ�
�ο��𰸣���1��D��2�֣�
��2��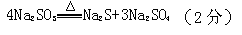 ������������С��2�֣�
������������С��2�֣�
��3��2S2-+SO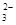 +6H+ =3S��+3H2O��2�֣���? B��Ʒ����Һ��ɫ��C�������Ա仯�����B�������Ա仯��C�в�����ɫ�������� ��B��Ʒ����Һ��ɫ��C�в�����ɫ���������÷֣� ��2�֣�
+6H+ =3S��+3H2O��2�֣���? B��Ʒ����Һ��ɫ��C�������Ա仯�����B�������Ա仯��C�в�����ɫ�������� ��B��Ʒ����Һ��ɫ��C�в�����ɫ���������÷֣� ��2�֣�
��4���ң�2�֣��������ȼ������ǿ�����Ե�ϡHNO3�����ܽ�SO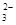 ������SO
������SO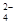 �������ж��Ƿ�����SO
�������ж��Ƿ�����SO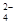 ��2�֣�
��2�֣�
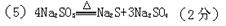 ��2�֣�
��2�֣�
�����������1��A����ּ��Ⱥ�һ���й����������̼����立ֽ⣬��A�����ϣ�?B������ǰ�������ɫ��һ���ޱ仯������������Һǰ����Ԫ�ر仯����B�����ϣ�C������ǰ�����������һ���б仯���������������ȷֽ��������ƺ������ƣ���ֽ���ﶼ�ǹ��壬��˷�Ӧǰ�����������û�з����仯����C�����ϣ�?D��һ���������µ����ʣ���ѧ��Ӧһ���������ʱ仯����D���ϣ�E����ּ��Ⱥ�õ��IJ������岻һ��Ϊ�������������ȫ�ֽ������Ȼ��غ���������E�����ϣ���ѡD��?��2�������⣬Na2SO3Ҫ���ȵ�600�����ϲŷֽ⣬������м����¶�600��������ȴ��õ��Ĺ�����ΪNa2SO3��˹����еμ�HCl��һ������Na2SO3��������ˮ���⽫������Һ��SO32-Ũ��������һ������HCl��SO32-��Ӧ���⽫����SO32-Ũ�ȼ�С�����������������Ũ��������HCl��һ���̶�ʱ��SO32-����ȫת��ΪHSO3-����ʱǰ��������ʧ����ȫ�Ǻ��������ã�HSO3-Ũ�����������С��ֱ������½����ӽ����㣬�ʴ�Ϊ������������С����3����������¶�Ϊ700�棬�����ù��������л����μ�ϡ�������������۲쵽��ƿ�г��ֵ���ɫ����Ϊ�����д������ݲ���˵��Ϊ����������������������ᷴӦ���ɵ���ɫ���������ӷ���ʽΪ��2S2-+SO32-+6H+=3S��+3H2O�����ɶ�������ķ�ӦΪSO32-+2H+=SO2��+H2O����ʱ��B��C��װ���п��ܹ۲쵽������Ϊ�����������Ư������ʹƷ����ɫ�����ɵ����岻������ͨ������ͭ������4���ڣ�3���еμ������������ƿ�ڳ�Cl-�⣬��������һ��Ũ�Ƚϴ�������ӣ�X����ͨ��ʵ������жϣ�����Ϊ��������ӣ�ȷ���ֽ����Ϊ���ƺ������ƣ�Ϊ����������ӣ�X������ȡ������������ˮ�����Һ��Ϊ�˼��ٹ����������ܽ⣬�����ò������������ȣ���������������Ǽ������ᣬ�ޱ仯���ټ����Ȼ������ɰ�ɫ����֤������������ӣ���ʵ������ᣬԭ����Һ�к��������ƣ������ᱻ����Ϊ�����ƣ�������������ӵļ��飬�ʴ�Ϊ�����裨����ȣ���?�ң������ȼ������ǿ�����Ե�ϡHNO3�����ܽ�SO32-������SO32-�������ж��Ƿ�����SO32-����5���������������жϣ��������Ƽ��ȵ�600�����Ϸֽ��������ƺ������ƣ���Ӧ�Ļ�ѧ����ʽΪ4Na2SO3=Na2S+3Na2SO4��
�����Ѷȣ�����