微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
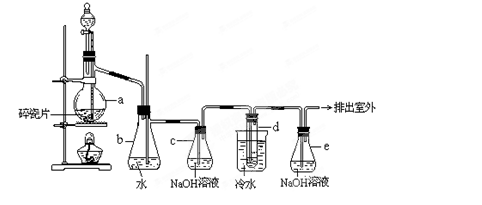
1、实验题 1,2―二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g・cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂在实验室中可以用下图所示装置制备1,2―二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
填写下列空白:
(1) 写出本题中制备1,2―二溴乙烷的两个化学反应方程式:
_________________________________;_________________________________
(2) 安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象______________________________。
(3) 容器c中NaOH溶液的作用是________________________________。
(4) 某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因:
① ___________________________________________________________;
② ___________________________________________________________
2、填空题 (14分)高纯六水氯化锶(SrCl2・6H2O)可用于制造高档磁性材料、电解金属钠的助熔剂、高档颜料和液晶玻璃等,具有很高的经济价值。高纯六水氯化锶的制备过程如下:
Ⅰ.将纯水加入烧杯内,搅拌下加入适量工业碳酸锶粉末(含少量Ba、Fe的化合物),制成浆料。
Ⅱ.缓慢加入工业盐酸进行酸化,将固体物质溶解。
Ⅲ.然后喷淋加入适量的硫酸,再加入质量分数为30%的双氧水少许。
Ⅳ.调节pH至8~10, 加热至60~70℃, ,搅拌1h,过滤,除去残渣。
Ⅴ.滤液加热至沸,继续浓缩至氯化锶质量浓度(溶质质量与溶液体积之比)为 x g/L。
请回答:
(1)用电子式表示HCl的形成过程?。
(2)已知Sr为第五周期第ⅡA族元素,则不符合Sr>Ca的是?(填序号)。
①原子半径?②最外层电子数
③金属性?④最高价氧化物对应的水化物的碱性
(3)写出步骤Ⅱ中加入盐酸时发生反应的离子方程式:?。
(4)加入硫酸后会先生成硫酸锶沉淀,进而转化为硫酸钡沉淀,试分析原理?。
(5)步骤Ⅲ中在酸性环境下加入双氧水是为将亚铁离子氧化成铁离子,写出该反应的离子方程式:?。
(6)步骤Ⅳ中调节pH至8~10,最好选用的试剂为?。
(7)已知某次实验得到浓缩后的氯化锶溶液中溶质为818g,溶剂为1000 g,经测定该溶液的密度为1.5 g/mL,则该溶液溶质的质量浓度x为??g/L(计算结果保留整数)。
3、实验题 (4分)实验室用乙醇和浓H2SO4反应制取乙烯时,常发现反应混合液变黑,同时制得的乙醇具有刺激性气味,它是浓H2SO4氧化了乙醇的缘故。试求:
现有以下盛放于洗气瓶中的药品:
A.溴水
B.浓NaOH溶液
C.澄清石灰水
D.酸性KMnO4 E.品红溶液,请设计实验方案证明所制得的乙烯中混有CO2、SO2,同时乙烯能与溴水反应。