��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ����ͪ��һ����Ҫ���л�����ԭ�ϡ�ʵ���Һϳɻ���ͪ�ķ�Ӧ���£�
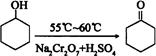
�������ͻ���ͪ�IJ����������ʼ��±���
����
| ��Է�������
| �е�(��)
| �ܶ�(g��cm��3��20 ��)
| �ܽ���
| ?
|
������
| 100
| 161.1
| 0.9624
| ������ˮ����
|
����ͪ
| 98
| 155.6
| 0.9478
| ����ˮ����������
| ?
|
?
����20mL������������Na2Cr2O7������Ļ��Һ��ַ�Ӧ���Ƶ���Ҫ������ͪ��ˮ�Ĵֲ�Ʒ��Ȼ����з����ᴿ������Ҫ������(δ����)��
A������ȥ���Ѻ��ռ�151��~156�����
B��ˮ��������(���ѷе�34.6�棬��ȼ��)��ȡ����ȡҺ�����л���
C������
D����Һ���м���NaCl���������ͣ����ã���Һ
E��������ˮMgSO4���壬��ȥ�л���������ˮ
�ش��������⣺
��1���������ᴿ�������ȷ˳����?��
��2��b��ˮ����������ȡ��Ŀ����?��
��3�����¹�����ȡ��Һ�����������У�����ȷ����?��
A��ˮ��Һ�м������ѣ�ת������Һ©�������ϲ���������ͼ������

B�����κ����Һ©���ϿڵIJ���������
C�����������������ֳַ�©������Һ��ֲ�
D����Һʱ�����Ƚ��Ͽڲ������������ϵİ��۶�©���ϵ�С�ף��ٴ��������²�Һ��ȫ������ʱ���ٴ��Ͽڵ����ϲ�Һ��
��4������������D�У�����NaCl�����������?����������ѵIJ����в��õļ��ȷ�ʽΪ?��
��5���������ʱ��һ��ʱ�����δͨ����ˮ��Ӧ��ȡ����ȷ������?��
��6���ָ�������ʱ������õ�����Ʒ���Ϊ12mL����ͪ�IJ���Լ��?��
�ο��𰸣���1��D B E C A
��2��ʹˮ�����������л����һ������ȡ����߲�Ʒ�IJ���
��3��A B C
��4�����ͻ���ͪ���ܽ�ȣ�����ˮ����ܶȣ������ڷֲ�?ˮԡ����
��5��ֹͣ���ȣ���ȴ��ͨ����ˮ
��6��60%(60.3%)
�����������1����������������ȡ�����ʻ���ͪ�к���δ��Ӧ�Ļ����������ڻ�����������ˮ���ѣ�������ͪ����ˮ���������ѣ������ᴿ�������ȷ������������Һ���м���NaCl���������ͣ����ã���Һ��Ȼ��ˮ��������(���ѷе�34.6�棬��ȼ��)��ȡ����ȡҺ�����л��㣻�ټ�����ˮMgSO4���壬��ȥ�л���������ˮ�����Ž��й��ˣ���ȥMgSO4���塣�������ȥ���Ѻ��ռ�151��~156����ּ��õ������Ļ���ͪ����2����B��ˮ����������ȡ��Ŀ����ʹˮ�����������л����һ������ȡ����߲�Ʒ�IJ�������3���������������ס��Һ©������������ѹס��Һ©���ڲ����ѷ�Һ©����ת������ʹ����Һ���ֽӴ������������©��������ų�. ��Һʱ��Ϊ��ʹҺ���ܹ�˳�����������Ƚ��Ͽڲ������������ϵİ��۶�©���ϵ�С�ף��²�Һ����¿��������ϲ��Һ����Ͽڵ�������ˣ�����IJ���ΪA B C ����4������������D�У�����NaCl����������ǽ��ͻ���ͪ���ܽ�ȣ�����ˮ����ܶȣ������ڷֲ㡣����������ѵIJ�����Ϊ�˼��ٻ���ͪ�Ļӷ���ɵ����ġ�ͨ�����õļ��ȷ�ʽΪˮԡ���ȡ���5���������ʱ��һ��ʱ���������δͨ����ˮ��Ӧ��ȡ����ȷ������ֹͣ���ȣ���ȴ��ͨ����ˮ������ᵼ��������ը�ѡ���6��ʵ�ʲ�����m(����ͪ)=" 0.9478g/ml��12mL=" 11.3736g.n(����ͪ)=m��M=11.3736g��98g/mol="0.116mol." m(������)= 0.9624g/ml��20ml=19.248g.n(��������=19.248g ��100g/mol="0.19248mol" .���Ի���ͪ�IJ���Ϊ��(0.116mol��0.19248mol����100% ="60%" ��
�����Ѷȣ�һ��
2��ѡ���� ���и��������У�������ˮ��Һ���������?��?��
A����ϩ����Ȳ��
B����ϩ�����
C������ֱ������
D������CCl4
�ο��𰸣�BD
�����������Ȳ����ϩ���ܺ���ˮ�����ӳɷ�Ӧ��A����ȷ���������ˮ����Ӧ������ѡ��B��ȷ������ֱ�����Ͷ�����ˮ����Ӧ��C����ȷ���������Ȼ�̼���ܺ���ˮ������ȡ�����б���ˮ���ϲ㣬���Ȼ�̼��ˮ���²㣬D��ȷ����ѡBD��
�����Ѷȣ�һ��
3������� ��15�֣�ij����Һ�����±������е�5�֣�������ˮ�ĵ��������ӵ�ˮ�⣩���Ҹ������ӵ����ʵ�����Ϊ1mol��
������
| K+��Ba2+��Fe2+��Al3+��Fe3+��Mg2+
|
������
| OH����HCO3����CO32����Cl����NO3����SO42��
|
����ԭ��Һ�м������������ᣬ���������ɡ�������֪����Ӧ�����Һ�е������ӵ�����û�б仯��
(1)��Һ��?���һ��������һ�������������ܡ�������HCO3����CO32����������??��
(2)ԭ��Һ����������������?����������?���������ӵķ��ţ�
(3)��ԭ��Һ�м������������ᣬ������ɫ��������ӷ�Ӧ����ʽ��?��
(4)����ԭ��Һ�м�������������������Һ����ַ�Ӧ�������ˡ�ϴ�ӡ����ﲢ���������أ���õ����������Ϊ?g��
�ο��𰸣���15�֣�
��1��һ������2�֣�
CO32����HCO3�����������ᷴӦ����CO2���壬ʹ��Һ�����������������仯��2�֣�
��2��Cl����NO3����SO42��?��3�֣�
Fe2+��Mg2+?��2�֣�
��3��3 Fe2+��? NO3����4H+��3 Fe3+��NO����2H2O?��3�֣�
��4��120?��3�֣�
�����������
�����Ѷȣ�һ��
4��ѡ���� ��Һ��ֻ��K+��Fe2+��Cl����SO42-��������.��֪K+��Fe2+��Cl���ĸ�����Ϊ3:2:1������Һ��Fe2+��SO42-�ĸ�����Ϊ
A.2:3
B.1:4
C.1:1
D.3:2
�ο��𰸣�A
��������������������K+��Fe2+��Cl�������ʵ����ֱ�Ϊ3mol��2mol��1mol�����ݵ���غ���Լ�������������Ϊ3mol��������Һ��Fe2+��SO42-�ĸ�����Ϊ2:3
���㣺����غ�
�����������ѶȲ��ߣ�ץסѡ��������⼼�ɣ����Ѽ�����̼��ԡ�
�����Ѷȣ���
5��ѡ���� ����˵���У��д������
A.Na2CO3��NaHCO3�����ܽ���ˮ
B.�������ʵ�����NaHCO3��ĩ��Na2CO3��ĩͬʱ�ֱ�����������ͬŨ�ȵ�ϡ�����У�ǰ�ߵķ�Ӧ������
C.Na2CO3���ȶ�����NaHCO3����ʱ���ֽ�
D.Na2CO3��Һ����ʯ��ˮ��Ӧ����NaHCO3��Һ������ʯ��ˮ��Ӧ
�ο��𰸣�D
���������������A����ͬ���¶��£�̼���Ƶ��ܽ�ȴ���̼�����ƣ�
B����ͬ������NaHCO3��Na2CO3��Ӧ�ų�������ң�
C��̼�����Ƽ���ʱ�ֽܷ⣬̼���Ƽ���ʱ���ֽ⣻
D��̼���ƺ�̼�����ƶ��ܺͳ���ʯ��ˮ��Ӧ����̼��Ƴ�����
���A����ͬ���¶��£�̼���Ƶ��ܽ�ȴ���̼�����Ƶģ���A��ȷ��
B��̼�����Ʒ�Ӧ��������ӷų�������̼��̼������Ҫ�Ƚ������������̼��������������ɶ�����̼����Ӧ���ӷ���ʽΪCO32-+2H+�TCO2��+H2O��HCO3-+H+�TH2O+CO2������ͬ������NaHCO3��Na2CO3��Ӧ�ų�������ң���B��ȷ��
C������ʱ��̼�������ֽܷ⣬̼���Ʋ��ֽ⣬����̼���Ƶ��ȶ��Դ���̼�����Ƶ��ȶ��ԣ���C��ȷ��
D��̼���ƺ�̼�����Ʒֱ���������Ʒ�Ӧ�ķ���ʽ���£�Na2CO3+Ca��OH��2=CaCO3��+2NaOH��NaHCO3+Ca��OH��2=CaCO3��+H2O+NaOH�����Զ��ܷ������ֽⷴӦ����D����
��ѡD��
���������⿼����Na2CO3��NaHCO3���ʵ���ͬ��ע�����Na2CO3��NaHCO3���ʵıȽϺ�Ӧ�ã�
�����Ѷȣ���