微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组原子中,彼此化学性质一定相似的是
[? ]
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有一个未成对的电子的X原子与3p 轨道上只有一个未成对的电子的Y原子
D.最外层都只有一个电子的X、Y原子
参考答案:C
本题解析:
本题难度:简单
2、填空题 A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图,

?B的最外层电子数比K层电子多1,D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
(1)指出元素A在周期表中的位置______,其气态氢化物的化学式为______.
(2)D和E两种元素相比较,非金属性较强的是(填元素符号)______,
可以验证该结论的是(填写字母序号)______;
A.比较这两种元素的常见单质的熔沸点?B.比较这两种元素的气态氢化物的熔沸点
C.比较这两种元素的气态氢化物的稳定性?D.比较这两种元素置换能力的强弱
(3)C、D、E三种元素最高价氧化物的水化物的酸性由强到弱的顺序:______.(填写化学式)
参考答案:A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,根据A的原子结构示意图可知A为Si元素,A、C同主族,则C为C元素;B的最外层电子数比K层电子多1,则B为Al元素;D元素的主族序数是周期序数的2倍,应为S元素,E的单质是黄绿色气体,应为Cl元素,
(1)由以上分析可知A为Si元素,原子有3个电子层,最外层电子数为4,处于周期表中第三周期第ⅣA族,最低负化合价为-4,氢化物的化学式为SiH4,
故答案为:第三周期第ⅣA族;SiH4;
(2)S和Cl在同一周期,同周期元素从左到右元素的非金属性逐渐增强,故非金属性Cl>S;
比较非金属性的强弱应从对应氢化物的稳定性,最高价氧化物对应水化物的酸性或单质的氧化性强弱等角度比较,不能从物理性质角度分析,故选CD,
故答案为:Cl;CD;
(3)元素的非金属性越强,则对应最高价氧化物对应水化物的酸性越强,非金属性Cl>S>C,则酸性:HClO4>H2SO4>H2CO3,
故答案为:HClO4>H2SO4>H2CO3.
本题解析:
本题难度:简单
3、填空题 有A、B、C、D、E五种微粒(原子或离子),已知:
A原子核外M电子层上有2个电子;
B原子得到2个电子后,其电子层结构与Ne相同;
C离子带有一个单位的正电荷,核电荷数为11;
D离子核外有18个电子,质子数比电子数少一个;
E微粒不带电,其质量数为1.
试回答下列问题:
(1)依次写出A、B、C、D、E各微粒的符号
A______、B______、C______、D______、E______;
(2)C、D所属元素组成的化合物是______化合物(填共价或离子),用电子式表示其形成过程______.
参考答案:A原子核外M电子层上有2个电子,则处于ⅡA,A为Mg原子;B原子得到2个电子后,其电子层结构与Ne相同,B的质子数为10-2=8,B为氧原子;C离子带有一个单位的正电荷,核电荷数为11,则C离子为Na+;D离子核外有18个电子,质子数比电子数少一个,质子数为18-1=17,D离子为Cl-;E微粒不带电,其质量数为1,不含中子,则E为H原子,
(1)由上述分析可知,A为Mg、B为O、C为Na+、D为Cl-、E为H原子,故答案为:Mg;O;Na+;Cl-;H;
(2)C、D所属元素组成的化合物是NaCl,属于离子化合物,用电子式表示其形成过程: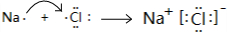 ,
,
故答案为:离子;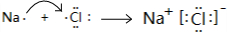 .
.
本题解析:
本题难度:一般
4、选择题 X,Y,Z,R是1~18号元素中的4种元素,它们的原子结构有以下特点:
①X元素原子的M层比L层少3个电子,
②Y元素的-2价阴离子的核外电子排布与氖原子相同,
③Z元素原子的L层比M层多5个电子,
④R元素原子的L 层比K层多3个电子,
其中金属性最强的是
[? ]
A.X
B.Y
C.Z
D.R
参考答案:C
本题解析:
本题难度:一般
5、简答题 A元素的最高价离子0.5mol被还原成中性原子时,要得到6.02×1023个电子,它的单质同盐酸充分反应时,放出0.02g?H2,用去0.4g?A.B元素的原子核外电子层数与A相同,且B元素形成的单质是红棕色液体.
(1)写出两种元素的名称:A______,B______.
(2)用电子式表示A、B形成的化合物中化学键的形成过程______.
参考答案:因A元素的最高价离子0.5mol被还原成中性原子时,要得到6.02×1023个电子即1摩尔电子,说明它的化合价为+2;单质同盐酸充分反应时,放出0.02g?H2即0.01mol,用去0.4g?A,由关系式:A~H2,可知:A的物质的也为0.01mol,A的摩尔质量为40g/mol,所以A的相对原子质量为40,故A为钙;因B元素的原子核外电子层数与A相同,且B元素形成的单质是红棕色液体,所以B是溴.
(1)A、B两元素的名称分别为:钙、溴,故答案为:钙;溴;
(2)用电子式表示溴化钙的形成过程:
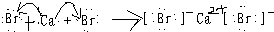
,故答案为:
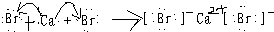
.
本题解析:
本题难度:一般