��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����д��������������������ͼ�е�װ�ý���ʵ�顣����ʾ����ʯ������ʯ�����������ƵĻ�����������ˮ�Ͷ�����̼��
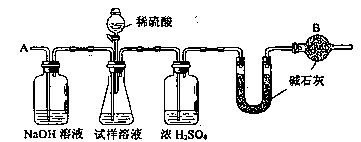
��Ҫʵ�鲽�����£��� ��ͼ��װ������������װ�õ�������
�� ��10.0 g����������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ
�� ����ʢ�м�ʯ�ҵ�U�ܵ��������õ�20.0g
�� �ӷ�Һ©������6mol��L��1�����ᣬֱ�����ٲ�������ʱΪֹ
�� �ӵ���A����������һ�����Ŀ���
�� �ٴγ���ʢ�м�ʯ�ҵ�U�ܵ��������õ�22.0g
�� �ظ�����ݺ͢IJ�����ֱ��U�ܵ������������䣬Ϊ22.2g
����պͻش����⣺
��1��װ���и����B������? _________________________�����û�����Ӹø���ܣ����ԵĽ��? (��ƫ�ߡ�ƫ�ͻ䣩��
��2���������Һ©���е����ỻ��Ũ����ͬ�����ᣬ���ԵĽ��? (��ƫ�ߡ�
ƫ�ͻ䣩��
��3������ݵ�Ŀ����? ___________________�����û�н��в���ݵIJ��������ԵĽ��________________����ƫ�ߡ�ƫ�ͻ䣩��
��4�������д������������Ϊ___________________��
�ο��𰸣���1����ֹ�����е�CO2��H2O����U���У�2�֣���ƫ�ߣ�2�֣�
��2��ƫ�ߣ�2�֣�
��3���ѷ�Ӧ�е�CO2ȫ������U���У�2�֣���ƫ�ͣ�2�֣�
��4��53.0%
�����������1��U���еļ�ʯ����Ϊ�����շ�Ӧ���ɵĶ�����̼����������Ҳ���ڶ�����̼�������B�����þ��Ƿ�ֹ�����еĶ�����̼��ˮ�ֽ���U�ܣ��Խ�������������е�ˮ�Ͷ�����̼����װ�ã�������Ϊ�Ƕ�����̼�����Զ�����̼������ƫ�������̼���Ƶ�����Ҳ��ƫ��ģ����Խ����ƫ��
��Ϊ����ֹ�����е�CO2��ˮ������U���У�ƫ�ߡ�
��2������������лӷ��ԣ�Ҳ�����Ŷ�����̼����U�ܣ�������Ϊ�Ƕ�����̼�����Զ�����̼������ƫ�������̼���Ƶ�����Ҳ��ƫ��ģ����Խ����ƫ��
��Ϊ��ƫ�ߣ�
��3�����ڷ�Ӧ������ƿ�д����ж�����̼������һ�����Ŀ������ǽ������Ķ�����̼��ȫ����U�ܣ�û�в���ݣ��в�����CO2û�з�Ӧ�����Խ��ƫ�͡�
��Ϊ���ѷ�Ӧ������CO2ȫ������U���У�ƫ�͡�
��4������Ҫ̼���Ƶ�����ΪX��
Na2CO3+H2SO4�TNa2SO4+H2O+CO2��
106? 44
X? 22.2-20.0
�б���ʽ��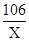 ��
��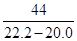
���X=5.3g��
���������д������������Ϊ
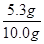 ��100%=53.0%��
��100%=53.0%��
�𰸣�53.0%
�����Ѷȣ�һ��
2��ѡ���� ��һ���¶��£����ռ���Һ�з���һ�������Ĺ������ƣ���ַ�Ӧ��ʹ֮�ָ���ԭ���¶ȡ�����˵����ȷ����?��?��
A����Һ��Na+Ũ��������O2�ų�
B����ҺpH���䣬��H2�ų�
C����Һ��Na+��Ŀ���٣���O2�ų�
D����ҺpH������O2�ų�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
3��ѡ���� ��������Ͷ�뵽�Ȼ�����Һ�У������ǣ�?��
A��OH,H2
B��Fe(OH)3,KCl,H2
C��e,KCl
D��HCl,Fe(OH)3,KCl
�ο��𰸣�B
���������������������ˮ��Ӧ���������������������أ��������������Ȼ�����Ӧ���������������������Ȼ��أ����Խ�������Ͷ�뵽�Ȼ�����Һ�У�������Fe(OH)3,KCl,H2���ʱ���Ĵ�ѡ��B��
���������⿼���˽������仯����ÿ����Ǹ߿�������ȵ㣬����Ƚ����ס�
�����Ѷȣ�һ��
4��ѡ���� ��1 L 1.00 mol/L ��Na2CO3��Һ��μ��뵽1 L 1.25 mol/L�������У������෴��������1 L 1.25 mol/L��������μ���1 L 1.00 mol/L ��Na2CO3��Һ�У����β����������������֮�ȣ�ͬ��ͬѹ�£���:��?��
A��1��1
B��2��1
C��5��2
D��2��5
�ο��𰸣�C
�����������1������̼���Ƽ��뵽������ʱ�������������˵������������ӦNa2CO3+2HCl= 2NaCl+H2O+CO2����n(HCl)="1.25" mol ���Էų�����0.625 mol ����2������������뵽̼������Һ��ʱ��.̼���������ᷴӦ�ֲ����С����ȷ�����Na2CO3+HCl= NaHCO3+NaCl��n(Na2CO3)="1.0mol" n(HCl)="1.25" mol��������1.0mol.����NaHCO31.0molʣ������0.25molȻ����NaHCO3+HCl= NaCl+H2O+CO2����̼�����ƶ���������˵��������Ӧ���������尴��������������0.25mol�����Բ���CO2����0.25mol�������β����������������֮ 91EXAM.org��Ϊ0.625 mol��0.25mol=5:2.ѡ��Ϊ ��C��
�����Ѷȣ�һ��
5��ʵ���� ijʵ��С����ͨ������ʵ����̽��Na2CO3��NaHCO3�������ʵ����ʡ�
��1����ȡ���ֹ����2 g���ֱ��������С�ձ��У��ٸ��μ�10 mL ����ˮ���������¶ȱ仯�����������ܽ⣬���ָ������º���������Һ�и�����2�η�̪��Һ��
�� ����Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬�ɴ˵õ�����?��
�� ͬѧ�������ձ��л��۲쵽�������������У�ʢ��Na2CO3���ձ��г��ֵ�������?������ĸ��ţ���
A����Һ�¶��½�? B����Һ�¶�����? C�������̪���dz��ɫ?D�������̪��ʺ�ɫ
��2����������ͼ��ʾ�ֱ����A��B���壬���ֹ���A���Ȳ�����������ʹ����ʯ��ˮ����ǣ���һ��ʱ�������ֱ���塣���û�ѧ����ʽ���ͳ���ʯ��ˮ�з���������?��
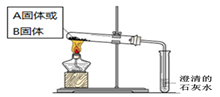
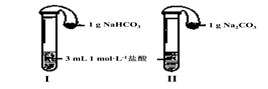
��3������ͼ��ʾ�������������õ�װ��I��II�зֱ�����Լ����������ڵĹ���ͬʱ�����Թ��С�
���Թ��о��������壬?���I����II�����ķ�Ӧ�̶ȸ�Ϊ���ҡ�
�� ��Ӧ����������������ͣ��ָ������¡�����˵����ȷ����?��
A��װ��I����������ϴ�? B��װ��II����������ϴ�
C�������������������������? D�����������������ݹ������
��4�������ֹ���ֱ����Ƴ�0.5 mol��L-1����Һ��̽����0.5 mol��L-1CaCl2��Һ��Ӧ�����
ʵ�鷽��
| Ԥ������
| Ԥ������
| ʵ�ʽ��
|
ʵ��1����2 mL Na2CO3��Һ�еμ�1 mL 0.5 mol��L-1CaCl2��Һ
| �а�ɫ
����
| Na2CO3��Һ�е�CO32-Ũ�Ƚϴ�����CaCl2������Ӧ��
| �а�ɫ����
|
ʵ��2����2 mL NaHCO3��Һ�еμ�1 mL 0.5 mol��L-1CaCl2��Һ
| �ް�ɫ
����
| NaHCO3��Һ�е�CO32-Ũ�Ⱥ�С��������CaCl2��Ӧ��
| �а�ɫ�������֣�ͬʱ����������ð����
|
?
��д������ʵ������з����ķ�Ӧ�����ӷ���ʽ��
ʵ��1��?��ʵ��2��?��
�ο��𰸣���1����ͬ�¶��£�Na2CO3��NaHCO3������ˮ��2�֣���˵���¶������Ŀ�1�֣�
��B��D��2�֣�
��2��Ca(OH)2+CO2=CaCO3��+H2O��2�֣�? CaCO3+CO2+H2O=Ca(HCO3)2��2�֣�
��3���٢�2�֣�?��2��A��C��2�֣���ѡ1����1�֣���ѡ����ѡ���÷֣�
��4��ʵ��1��Ca2++CO32-=CaCO3����2�֣�?ʵ��2��Ca2++2HCO3-=CaCO3��+CO2��+H2O��2�֣�
��������� ��1������̽����Na2CO3��NaHCO3�������ʶ���������ѧ�ηdz���֪���������Σ����������ʽ��жԱȣ��ܶ����ʿ���ֱ�ӽ��������ѧ���ݵó����˴���ȡ���������������ܽ⣬����Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬˵������ͬ�¶���Na2CO3������ܽ��Ҫ����NaHCO3���塣�����������ܽ���Ƿ��ȵģ����Ի�ʹ��ϵ�¶����ߡ�ͬʱ���Ǿ���ǿ�������Σ�ˮ��ʼ���ʹ��̪��졣��ѡBD��
��2��NaHCO3 �����ֽ����CO2��ʹ����ʯ��ˮ����ǣ�����ͨ��һ��ʱ���CO2�����ij���CaCO3���������CO2��Ӧ�����˿��ܵ�Ca(HCO3)2��������Һ�ֱ���塣�������̷����ķ�Ӧ����ʽΪ��Ca(OH)2+CO2=CaCO3��+H2O?�� CaCO3+CO2+H2O=Ca(HCO3)2?��
��3���٢�Na2CO3��NaHCO3�������ʾ�����HCl��Ӧ����CO2���壬���Ƿ�Ӧ��CO32- Ҫ����H+��Ӧ����HCO3����Ȼ������HCO3����H+��Ӧ����CO2������2�����裬����װ��I��ӦҪ����װ��IIҪ����Ϊ���ҡ�
����������������С��Ҫ����Ӧ���ɵ�CO2��������������Cԭ���غ㣬1g��Na2CO3��1g NaHCO3 �У�NaHCO3 �����ɵ�CO2���ʵ��������Բ���������࣬��A��ȷ����ʵ�����������ȫ��Ӧ��������������������������㣬��C��ȷ����ѡAC��
��4��ʵ��1�в�����ɫ���������ڸ����Ӻ�̼������ӽ��������̼��Ƴ������������ӷ���ʽΪ��
Ca2++CO32-=CaCO3������ʵ��2��������HCO3����Ca2+ ���ܷ�Ӧ��û�г������ɣ�������ʵ�ʽ���Ʋ�HCO3���������������CO32-��H+�����������CO32-��Ca2+ ���������̼��Ƴ�����ͬʱ��һ���ٽ��˵��룬ʹ�õ��������H+������Һ�е�HCO3����Ӧ����CO2���壬�������ӷ���ʽΪ��Ca2++2HCO3��=CaCO3��+CO2��+H2O��
�����Ѷȣ�һ��