微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH
溶液,其充、放电按下式进行: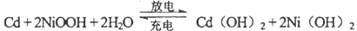
有关该电池的说法正确的是(? )。
A.充电时阳极反应: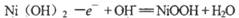
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
参考答案:A
本题解析:A、充电时相当于电解池装置,阳极发生氧化反应,所以阳极电极反应式为: ,正确;B、充电过程是把电能转化为化学能的过程,错误;C、放电时Cd作负极,失去电子,结合OH-成为Cd(OH)2,所以负极附近溶液的碱性减弱,错误;D、放电时充当原电池装置,OH-向负极移动,错误,答案选A。
,正确;B、充电过程是把电能转化为化学能的过程,错误;C、放电时Cd作负极,失去电子,结合OH-成为Cd(OH)2,所以负极附近溶液的碱性减弱,错误;D、放电时充当原电池装置,OH-向负极移动,错误,答案选A。
本题难度:一般
2、选择题 将等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加少量组成原电池的条件CuS04溶液,下列各图中产生H2的体积V(L)与时间t(min)的关系如图所示,其中正确的是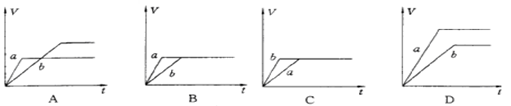
参考答案:A
本题解析:等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中放入少量的CuSO4溶液,发生:Fe+Cu2+=Fe2++Cu,形成原电池,反应速率增大,但生成的氢气少.
解答:解:等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中放入少量的CuSO4溶液,发生的反应为:
Fe+Cu2+=Fe2++Cu,铜-铁-稀硫酸形成原电池,反应速率增大,反应用时少于b,但生成的氢气少也少于b,图象应为A.
故选A.
本题难度:一般
3、选择题 以色列科学家达尼埃尔・谢赫特曼因发现“准晶体”获得2011年诺贝尔化学奖。某准晶体由一定比例的铁、铜、铝组成,取两小块该准晶体:一块投入烧杯①中,注入浓氢氧化钠溶液浸没固体;另一块投人烧杯②中,注入稀硫酸浸没固体。下列分析合理的是
A.在烧杯①中,若构成微型电池,负极反应式为2H2O十2e-=2OH-+H2↑
B.在烧杯②中,若铁、铜构成微型电池,则铜为负极
C.在烧杯①中,若构成微型电池,铝为负极
D.在烧杯②中,向溶液中滴加KSCN溶液,溶液一定变为红色
参考答案:C
本题解析:在烧杯①中,若构成微型电池,则铝作负极,铁或铜作正极,负极上铝失电子发生氧化反应,正极上得电子发生还原反应,在烧杯②中,若构成原电池,则铝或铁作负极,则铁或铜作正极,负极上活泼金属失电子发生氧化反应,正极上氢离子得电子发生还原反应.在烧杯①中,若构成微型电池,负极反应式为:2Al-6e-+8OH-=2AlO2-+4H2O,故A错误;在烧杯②中,若铁、铜构成微型电池,则铜为正极,故B错误;在烧杯①中,若构成微型电池,铝易失去电子发生氧化反应而为负极,故C正确;在烧杯②中,若铁作负极,铁失电子生成亚铁离子,向溶液中滴加KSCN溶液,溶液不变红色,故D错误;所以选C。
本题难度:一般
4、选择题 铅蓄电池在现代生活中有广泛应用,其电极材料是Pb和PbO2,电解液是硫酸溶液.现用铅蓄电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
A.蓄电池放电时,每消耗0.1molPb,共生成0.1mol?PbSO4
B.电解硫酸钠溶液时的阳极反应式为:4OH--4e-=2H2O+O2↑
C.电解后,硫酸钠溶液中有晶体析出,但c(Na2SO4)会变小
D.蓄电池放电一段时间后其电解液中H2SO4的浓度、密度都变小
参考答案:A、负极:Pb-2e-+SO42-=PbSO4,正极:PbO2+2e-+4H++SO4=PbSO4+2H2O,蓄电池放电时,每消耗0.1molPb,转移电子物质的量为0.2mol,正负极生成硫酸铅共生成0.2mol?PbSO4,故A错误;
B、电解硫酸钠溶液实质是电解水,阳极反应式为:4OH--4e-=2H2O+O2↑,故B正确;
C、电解饱和硫酸钠溶液后,饱和硫酸钠溶液中有晶体析出,但c(Na2SO4)不变,故C错误;
D、蓄电池放电一段时间后,生成硫酸铅和水,其电解液中H2SO4的浓度变小、密度都变小,故D正确;
故选BD.
本题解析:
本题难度:一般
5、选择题 用石墨电极电解足量以下溶液,阴、阳两极均产生气体且气体体积之比为2:1的是( )
A.饱和NaCl溶液
B.Na2SO4溶液
C.CuSO4溶液
D.CuCl2溶液
参考答案:A.电解氯化钠溶液时,阳极上析出Cl2,阴极上析出H2,2mol氢离子得2mol电子生成1molH2,2mol氯离子失去2mol电子生成1molCl2,所以阴、阳两极均产生气体且气体体积之比1:1,故A错误;
B.电解硫酸钠溶液时,阳极上析出O2,4mol氢氧根离子失去4mol电子生成1molO2转移4mol电子,阴极上析出H2,4mol氢离子得4mol电子生成2molH2,所以阴、阳两极均产生气体且气体体积之比为2:1,故正确;
C.电解硫酸铜溶液时,阴极上析出铜单质,没有气体生成,故C错误;
D.电解氯化铜溶液时,阴极上析出铜单质,没有气体生成,故D错误;
故选B.
本题解析:
本题难度:简单