��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij���������п��ܺ���(NH4)2SO4��AlCl3��Na2SO4��MgCl2��KNO3��Al��FeCl2�е�һ�ֻ��֣��ֶԸû����������·���������������ڱ�״���²ⶨ�������Լ�����������
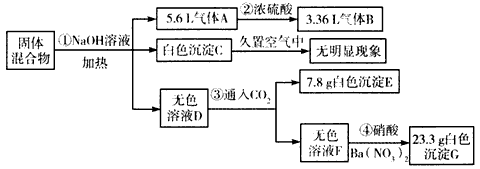
��ش��������⣺
(1)����A�ijɷ���__________���ѧʽ����ͬ������ɫ����EΪ_____________
(2)�ù���������һ����___________ ������ȷ���Ƿ���______________��ͨ��ʵ���һ��ȷ�����и����ʵķ�����________________________
(3)ͨ������˵����������Ƿ���Na2SO4�����ɣ�д��������̣��� ________________________
�ο��𰸣�(1)NH3��H2��Al(OH)3
(2)(NH4)2SO4��MgCl��Al��Na2SO4��KNO3���ýྻ�IJ�˿պȡ������ҺF���ھƾ�����������գ�����ɫ�겣���۲쵽�������ɫ����֤������KNO3
(3)n[(NH4)2SO4] ��Ϊn(BaSO4)>n[(NH4)2SO4]������ 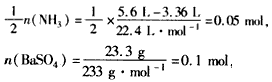 �û������һ������Na2SO4
�û������һ������Na2SO4
���������
�����Ѷȣ�һ��
2��ѡ���� Ϊ����ijFeCl2��Һ�Ƿ���ʣ�������Һ�м��루������
A��KSCN��Һ
B����Ƭ
C����ˮ
D��ʯ����Һ
�ο��𰸣�A�����FeCl2��Һ���ʣ����ʺ��������FeCl3��Fe3+�ܺ�SCN-��������ʹ��Һ����Ѫ��ɫ�������ԣ���һ��Ӧ��Fe3+��������Ӧ��������KSCN��Һ����A��ȷ��
B����Ƭ���Ȼ���������Ӧ�������飬��B����
C��������ˮ����Һ��û�������������������飬��C����
D�������Ȼ������Ƿ���ʣ�����ǿ�������Σ���Һ�������ԣ����������飬��D����
��ѡ��A��
���������
�����Ѷȣ�һ��
3��ѡ���� ���и���ϡ��Һ�����������Լ�����ֽ����������Һ������Ӧ���Ϳ��Խ����������ǣ�������
��H2SO4?MgCl2?NaCl?NaOH?��FeCl3?NaOHMgCl2NaNO3
��HCl?Na2SO4?Na2CO3NaOH?��CuSO4BaCl2Na2SO4NaOH��
A���٢�
B���ۢ�
C���٢�
D���ڢ�
�ο��𰸣�����������֮������û�����Ե������ܼ��𣬹ʢٴ���
��FeCl3��ҺΪ��ɫ������NaOH��Һ�����ɺ��ɫ������������NaOH�ɼ���MgCl2��ʣ��һ��ΪNaNO3���ɼ��𣬹ʢ���ȷ��
��HCl��Na2CO3��μӿɼ��𣬵����ܼ���Na2SO4��NaOH���ʢ۴���
��CuSO4��ҺΪ��ɫ���ֱ���뵽BaCl2��NaOH��Һ�пɷֱ������ɫ��������ɫ������ʣ��һ��ΪNa2SO4�����Լ��𣬹ʢ���ȷ��
��ѡD��
���������
�����Ѷȣ���
4��ʵ���� ʵ��������ϩʱ�������¶ȹ��߶���������Ӧ��ʹ�����Ҵ���Ũ���ᷴӦ���ɶ�����������̼��ˮ������̼�ڡ�
(1)������ͼ���Ϊ�٢ڢۢܵ�װ�����һ��ʵ�飬����֤������Ӧ��������к���CO2��SO2��ˮ������ ��װ�õı�ű�ʾװ�õ�����˳������������ ���ҵ�˳��___��____��___ ��____
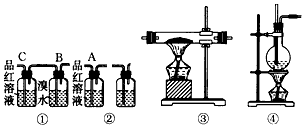
(2)ʵ��ʱ��װ�â���Cƿ��������____________��ԭ����____________��Bƿ�е�������____________��Bƿ��Һ��������____________�� ��Aƿ��Ʒ����Һ����ɫ��˵��_______________��
(3)װ�â��мӵĹ���ҩƷ��____________������֤�����������________________��װ�â���ʢ�ŵ���Һ��________________������֤��������е�________________��
(4)װ�â�������װ��������λ�õ�������____________________��
�ο��𰸣�(1)�ܣ��ۣ��٣���
(2)Ʒ����ɫ��SO2��ʹƷ����ɫ����ˮ��ɫ����ȥ�����SO2��SO2�Ѿ�����
(3)CuSO4��ĩ��H2O������ʯ��ˮ��CO2
(4)�ȳ�ȥSO2������Ӱ��ʵ������
���������
�����Ѷȣ�һ��
5������� �����������壨FeSO4?7H2O����ҽҩ������Ѫ����ij����С��ⶨ�ò�Ѫ������Ԫ�صĺ�����ʵ�鲽�����£�
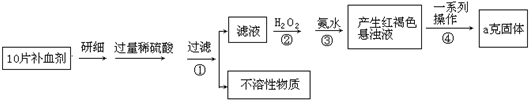
��ش��������⣺
��1��֤���������Һ�к���Fe2+�ķ�����______��
��2��д�����е����ӷ�Ӧ����ʽ��______��
��3��������з�Ӧ�����ӷ���ʽ��______��
��4���������һϵ�д����IJ������裺���ˡ�______�����ա���ȴ��������
��5����С����Щͬѧ��Ϊ��KMnO4��Һ�ζ�Ҳ�ܽ�����Ԫ�غ����IJⶨ����5Fe2++MnO4-+8H+��5Fe3++Mn2++4H2O��
��ʵ��ǰ������Ҫ��ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ��������ҩ�ס���ƽ�������룩���������ձ�����ͷ�ι��⣬����______��
�ڵζ����յ�ʱ����ɫΪ______ɫ��
��6��������ÿ��Ӧ����16.8mg���ҵ��������о���������ʳ����ȫ��ͨ�����ú�FeSO4?7H2O��Ƭ����������������������ÿ������ú�______mgFeSO4?7H2OƬ����
�ο��𰸣���1��Fe3+��KSCN��Һ�Ժ�ɫ�����������ڼ���Fe3+���ڣ����Լ�����������Fe2+����ΪFe3+������Fe2+�����ȵμ�KSCN��Һ����Һ����ɫ���ٵμ���ˮ��˫��ˮ����Һ��ΪѪ��ɫ��˵������Fe2+��
�ʴ�Ϊ��ȡ������Һ�����Թ��У��ȵμ�KSCN��Һ����Һ����ɫ���ٵμ���ˮ����˫��ˮ��ϡ���ᣩ����Һ��ΪѪ��ɫ��
��2��˫��ˮ���������ԣ������������ܽ�Fe2+ȫ������ΪFe3+��ͬʱ����ˮ����Ӧ���ӷ���ʽΪ2Fe2++H2O2+2H+�T2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+�T2Fe3++2H2O��
��3��������ǽ�Fe3+ת��Ϊ����������������Ӧ���ӷ���ʽΪFe3++3NH3?H2O=Fe��OH��3��+3NH4+��
�ʴ�Ϊ��Fe3++3NH3?H2O=Fe��OH��3��+3NH4+��
��4���������һϵ�д�������������������Һ����ת��Ϊ����������Ҫ���ˡ�ϴ�ӵ�����������Ȼ��������������������ȴ�������������������
�ʴ�Ϊ��ϴ�ӣ���ȴ��
��5���پ�ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ���������ձ�����ͷ�ιܣ�250mL����ƿ��
�ʴ�Ϊ��250mL����ƿ��
�ڸ������Ϊ��ɫ�����ζ����յ�ʱ��Fe2+����ȫ��������������һ�θ�����ز���Ӧ����Һ����ɫΪ��ɫ���ʴ�Ϊ���ϣ�
��6��16.8mg����ΪFeSO4?7H2OƬ��������������������ҪFeSO4?7H2OƬ������Ϊ16.8mg��56278=83.4mg��
�ʴ�Ϊ��83.4mg��
���������
�����Ѷȣ�һ��