微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 9、下列溶液中含Cl-浓度最小的是
A、10ml 0.1mol/L AlCl3的溶液 B、20ml 0.2mol/LCaCl2的溶液
C、30ml 0.2mol/LKCl的溶液 D、100ml 0.25mol/LNaCl的溶液
参考答案:C
本题解析:A项中Cl-浓度为0.3mol/L;B项中Cl-浓度为0.4mol/L;C项中Cl-浓度为0.2mol/L。
考点:浓度大小的比较
点评:本题的关键是要注意本题中的计算与所给体积无关。
本题难度:一般
2、计算题 (4分)将标准状况下44.8 L NH3与足量的盐酸充分反应。试计算:
(1)生成NH4Cl的物质的量为多少?
(2)生成NH4Cl的质量为多少?
参考答案:(1) 2mol? (2) 107g
本题解析:略
本题难度:简单
3、选择题 高岭土中[Al2(Si2O5)(OH)4]中SiO2的质量分数为( )
A.46.5%
B.23.3%
C.21.7%
D.35.7%
参考答案:Al2(Si2O5)(OH)4改写为氧化性形式为Al2O3?2SiO2?2H2O,
SiO2的质量分数=2×(28+32)102+120+36×100%=46.5%,
故选A.
本题解析:
本题难度:一般
4、选择题 设NA表示阿伏加德罗常数的值,下列说法中正确的是
A.1 mol NH4+所含质子数为10NA
B.10克氖气所含原子数约为6.02×1023
C.22.4 L SO2所含的分子数为NA
D.2.3克Na变为Na+时失去的电子数是0.1NA
参考答案:D
本题解析:A错,1 mol NH4+所含质子数为11NA;B错,10克氖气所含原子数约为3.01×1023;C错,应在标准状况下;D正确;
本题难度:一般
5、实验题 (18分)(1)写出下图中序号①~④仪器的名称:
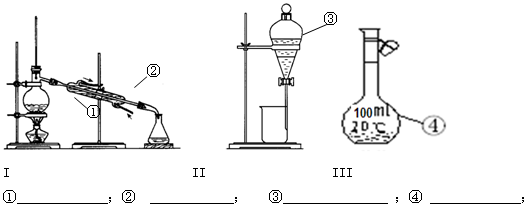
(2)仪器①~④中,使用时必须检查是否漏水的有??。(填仪器序号)
(3)分离碘水中的碘应先选择装置?(填装置序号)进行操作A,再选装置进行??操作。进行操作A时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:?(填序号)。
①常温下为液态?②I2在其中溶解程度大?③与水互溶程度小?④密度要比水大
(4)右图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol/L的稀硫酸。

可供选用的仪器有:
①胶头滴管;②烧瓶;③烧杯;④?药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
a.盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的?

b.配制稀硫酸时,还缺少的仪器有?、?(写仪器名称);
c.经计算,配制480 mL 1 mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为______?mL,量取硫酸时应选用??mL规格的量筒;
A.10 mL? B.50 mL? C.100 mL? D.200mL
d.对所配制的稀硫酸进行测定,发现其浓度大于1 mol/L,配制过程中下列各项操作可能引起该误差的原因有 (? )?。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.定容时,俯视容量瓶刻度线进行定容
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
参考答案:(1)①蒸馏烧瓶?②冷凝管?③分液漏斗?④容量瓶
(2) ③④? (3)Ⅱ?蒸馏?①②③?
(4)(a)D? (b)玻璃棒、500mL容量瓶(各1分)? (c)27.2(2分)? B? (d)ABC
本题解析:(1)根据仪器的结构可知,四种仪器分别是①蒸馏烧瓶、②冷凝管、③分液漏斗、④容量瓶。
(2)使用时必须检查是否漏水的有容量瓶和分液漏斗,所以答案选③④。
(3)分离碘水中的碘应先萃取,然后在蒸馏。即先在装置Ⅱ中进行。选用的萃取剂的原则:?①和原溶液中的溶剂互不相溶;?②对溶质的溶解度要远大于原溶剂,所以答案选①②③。
(4)(a)浓硫酸具有很强的腐蚀性,所以答案选D。
(b)由于没有480ml的容量瓶,所以应该配制500ml,因此需要500ml容量瓶。另外稀释和转移时还需要玻璃棒。
(c)需要硫酸的物质的量是0.5L×1mol/L=0.5mol,因此需要浓硫酸的体积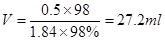 ,因此选择50ml量筒,即答案选B。
,因此选择50ml量筒,即答案选B。
(d)根据c=n/V可知,用量筒量取浓硫酸时,仰视刻度线取浓硫酸,则溶质增加,浓度偏高;定容时,俯视容量瓶刻度线进行定容,则容量瓶中溶液体积减少,浓度偏高;将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作,则冷却后,溶液体积减少,浓度偏高;转移溶液时,不慎有少量溶液洒到容量瓶外面,则溶质减少,浓度偏小;容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水,不影响实验结果;定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,则容量瓶中溶液体积增加,浓度偏小,实验答案选ABC。
本题难度:一般