��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ�У�Ũ����ȱ���ǿ�������ֱ������Ե��ǣ�������
A��Ũ��������������Ӧ
B��Ũ����������������Ӧ
C��Ũ������ͭ��Ӧ
D��Ũ������ľ̿�۷�Ӧ
�ο��𰸣�A��Ũ��������������Ӧ������������ˮ��Ũ������ֳ����ԣ�û�з���������ԭ��Ӧ����A����
B��Ũ����������������Ӧ��������������ˮ��Ũ������ֳ����ԣ�û�з���������ԭ��Ӧ����B����
C��Ũ������ͭ��Ӧ��������ͭ�����������ˮ������������ԭ��Ӧ����������ͭ�����ֳ����ԣ���C��ȷ��
D��Ũ������ľ̿�۷�Ӧ�����ɶ�����������̼��ˮ��û�������ɣ�Ũ����ֻ���ֳ������ԣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
2������� Ϊ̽������п��18.4mol?L-1Ũ����ķ�Ӧ��ij�о�С���������ʵ�飮
[ʵ��I]��Ӧ������ɷֵĶ���̽��
ȡ65.0gп����98%��ŨH2SO4����=1.84g?mL-1��110m��ַ�Ӧ��пȫ���ܽ⣬�����Ƶõ����壬��ͬѧ��Ϊ���ܻ������ʣ�
��1���о�С�����Ƶõ������л��е���Ҫ������������ǣ�______�������ʽ�����������ֽ������Ҫԭ���ǣ�______���û�ѧ����ʽ�ͱ�Ҫ�����ּ���˵����
��2��Ϊ֤ʵ��ط������û�ѧС���ͬѧ���ʵ�飬��װ��ͼ1װ�ã��������˵��������̽����
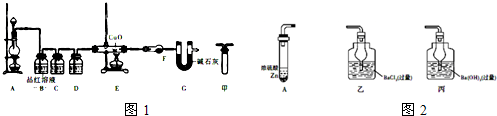
��װ��C�м�����Լ��ǣ�______��װ��D�м�����Լ��ǣ�______��
��װ��F�м�����Լ��ǣ�______��U��G������Ϊ��______��
����ͬѧ��ΪA��B��Ӧ����ͼ�еļ�װ�ã���װ�õ�����Ϊ��______��
[ʵ��II]����Ũ������������ɷֵĶ���̽��
Ϊ�˶����ⶨŨ�������ǿ�����Ե����Ũ�ȣ���Ƶ�ʵ�鷽��Ϊ��ȡ18.4mol?L-1Ũ����aml��������п��A�з�Ӧ�������ɵ�����ͨ��ij��Һ���ⶨ���ɳ�����������
��1��A�в���������Ӧͨ��ͼ2�е�______����ҡ�������װ�ã�
��2����ͬѧ��ΪҪ��Сʵ������Ҫ����һ������Ӧ���ɵ�SO2ȫ���ų��IJ�������Ҳ��ͬѧ��Ϊû�б�Ҫ���������ǣ�______��
�ο��𰸣�ʵ��I����1����������Ũ�Ƚ��ͣ�п��ϡ���ᷴӦ�������������Ի�ѧС�����Ƶõ������л��е���Ҫ�������������������
�ʴ�Ϊ��H2�����ŷ�Ӧ�Ľ��У�����Ũ�Ƚ��ͣ���ʹп��ϡ���ᷴӦ����H2��Zn+H2SO4�TZnSO4+H2����
��2����Cװ���dz�ȥ�������������������ƣ���KMnO4���ȼ�Һ���գ�Dװ����Ũ���ᣬ��ˮ�������ã�
�ʴ�Ϊ��NaOH��Һ����ȥ��������е�SO2��Ũ���
��Fװ����ˮ����ͭ�������Ƿ���ˮ���ɣ�G�Ƿ�ֹ������H2O�������ܶ�Ӱ����������ļ��飬
�ʴ�Ϊ����ˮ����ͭ����ֹ������H2O�������ܶ�Ӱ����������ļ��飻
��A��B��Ӧ����ͼ�еļ�װ���ǰ�ȫװ�÷�ֹ���������ã��ʴ�Ϊ����ֹ������
ʵ���Ϊ�˶����ⶨŨ�������ǿ�����Ե����Ũ�ȣ���Ƶ�ʵ�鷽��Ϊ��ȡ18.4mol?L-1Ũ����aml��������п��A�з�Ӧ�������ɵ�����ͨ��ij��Һ���ⶨ���ɳ�����������
��1��A����������Ϊ���������������ͨ��ij��Һ���� �����ɳ�������������Ҫ�Ͷ�����̼��Ӧ���ɳ������Ҳ����������Ӧ�����Ͷ�������Ӧ���������ᱵ������
�ʴ�Ϊ������
��2��п�������淴Ӧ���У�Ũ����Ũ�ȼ�С��Ϊϡ������п��Ӧ���ɵ�����Ϊ�������������������Ѷ�������ȫ���ų�������Ҫ����װ�ý���Ӧ���ɵ�SO2ȫ���ų��IJ�����
�ʴ�Ϊ��������������Ὣ���������ȫ��������У�
���������
�����Ѷȣ�һ��
3��ѡ���� ij�л���ķ���ʽΪC4H8O2���й���ͬ���칹����Ŀ��˵���������
A�������������4��
B�������������2��
C���Ⱥ����ǻ��ֺ���ȩ������3��
D�����ڷ����к�����Ԫ����ͬ���칹��
�ο��𰸣�C
������������⿼����ͬ���칹�����д֪ʶ�����ڿ��鿼�������֪ʶ���������������ʽΪC4H8O2���л�����������ͬ���칹���м����������������������������������������4�֣�Aѡ����ȷ�����������ͬ���칹���ж����2?�����ᣬ��2�֣�Bѡ����ȷ���Ⱥ����ǻ��ֺ���ȩ����ͬ���칹����CH2OHCH2CH2CHO��CH3CHOHCH2CHO��CH3CH2CHOHCHO��CH2OHCH(CH3)CHO��(CH3)2COHCHO����5�֣�Cѡ������ڷ����к���4��̼ԭ�Ӻ�2����ԭ����ɵ���Ԫ��״�������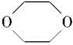 ��Dѡ����ȷ��
��Dѡ����ȷ��
�����Ѷȣ�һ��
4�������&n bsp; Ϊ����Ũ������ľ̿�ڼ��������·�Ӧ������SO2��CO2���壬�������ͼ��ʾʵ��װ�ã�a��b��cΪֹˮ�У�B�����ڴ��������ң�D�з�����I2�͵��۵���ɫ��Һ��ʪ����֬�ޣ�����I2�͵��۵���ɫ��Һ����֬�ޣ�
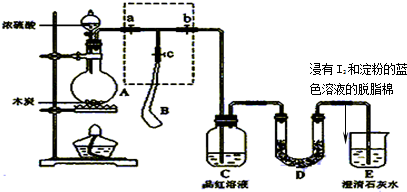
��ش��������⣺
��1��װ��A��D�з�����Ӧ�Ļ�ѧ����ʽΪ______��______��
��2��ʵ��ǰ�����װ��A�������ԣ����Բ�ȡ�IJ�����______��
��3����ʵ��ɰܵĹؼ����ڿ��Ʒ�Ӧ������������ʲ��ܹ��죬����������ֵ�װ�ã�����ȷ�IJ���˳����______���ò��������д��
����Aװ���м���Ũ���ᣬ���ȣ�ʹA�в����������������B���������г���һ��������ʱ��ֹͣ���ȣ�
�ڴ�װ��A��ȴ��������B��������ٱ仯�ر�ֹˮ��a����ֹˮ��b��������ѹ���ң�ʹ����B��������������װ��C�У����ﵽʵ��Ŀ�ĺر�ֹˮ��b��
�۴�ֹˮ��a��c���ر�ֹˮ��b��
��4��ʵ��ʱ��װ��C�е�����Ϊ______��
��5����D�в���______����ʱ������˵��ʹE�г���ʯ��ˮ����ǵ���CO2��������SO2��
��6��װ��D������Ϊ______��
�ο��𰸣���1��װ��A��Ũ������ǿ�����ԣ��ܽ�C����Ϊ������̼��D�еⵥ���ܽ�������������Ϊ���ᣬ�ʴ�Ϊ��C+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��I2+SO2+2H2O=H2SO4+2HI��
��2���跨ʹװ�������γ���ѹ��ʴ�Ϊ���رշ�Һ©���Ļ�������ֹˮ��a��b���ر�ֹˮ��c���������ȣ����ȣ�Բ����ƿA����C��������ð�����ƿ����ƣ�����Դ����C����������ˮ��������֤��Aװ�õ����������ã�
��3����ʹ�������B����B������������飬�ʴ�Ϊ���ۢ٢ڣ�
��4������������ʹƷ����Һ��ɫ���ʴ�Ϊ��Ʒ����Һ��ɫ��
��5��������һ����֬����ɫ��dz��������һ����֬����ɫ����ʱ�����ڳ����Ƕ�����̼���ʴ�Ϊ��������һ����֬����ɫ��dz��������һ����֬����ɫ���䣻
��6��װ��D������Ϊ��ȥSO2������SO2�ѱ��������ʴ�Ϊ����ȥSO2������SO2�ѱ�������
���������
�����Ѷȣ�һ��
5������� ������C��H��O���л���3��0gװ��Ԫ�ط���װ�ã�ͨ��������O2ʹ֮��ȫȼ�գ������ɵ���������ͨ��װ��CaCl2(A)�ͼ�ʯ��(B)�ĸ���ܣ����A������������1��8 g��B������������4��4 g����֪���л������Է�������Ϊ60����1��ȼ�մ��л���3��0 g������O2����״����?L����2������л���ķ���ʽ?��
�ο��𰸣���1��2��24L?��2��C2H4O2
�����������1�����������غ㶨�ɿ�֪ȼ�մ��л���3��0 g������O2������Ϊ1��8 g ��4��4 g ��3��0g =3��2g��n(O2)=3��2g��32g/mol=0��1mol�������ڱ�״���������Ϊ2��24L����2��n(H2O)= 1��8 g�� 18g/mol= 0��1mol;n(CO2)= 4��4 g��44g/mol=0��1mol��������3��0g���л����У�����H��0��2mol;C:0��1mol��O��(3��0g��0��2mol��1g/mol��0��1mol��12g/mol)��16g/mol=0��1mol�����Ըû���������ʽ��CH2O����ʽ��Ϊ30�� ��Ϊ���л������Է�������Ϊ60�����Ըû�����ķ���ʽΪC2H4O2��
�����Ѷȣ�һ��