微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 据报道,N5是破坏力极强的炸药之一,18O2是比黄金还贵重的物质。下列说法正确的是
[? ]
A.18O2中含18个中子
B.原子半径:N<18O
C.N5和N2互为同位素
D.2N5=5N2是化学变化
参考答案:D
本题解析:
本题难度:简单
2、填空题 下表是元素周期表的一部分,针对表中的①~⑧中元素,用元素符号或化学式填空回答以下问题:
 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0
2
①
②
3
③
④
⑤
⑥
⑦
⑧
|
(1)在这些元素中,金属性最强的元素是______,最活泼的非金属元素是______;
(2)化学性质最不活泼的元素是______,其原子的原子结构示意图为______;
(3)元素的最高价氧化物对应的水化物中酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______;
(4)在③~⑦元素中,原子半径最大的是______,原子半径最小的是______;
(5)在⑥与⑦的单质中,化学性质较活泼的是______,设计一个实验方案比较其氧化性的强弱(用反应的化学方程式表示):______.
参考答案:由元素在周期表中的位置可知,①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为S、⑦为Cl、⑧为Ar,
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,在这些元素中,金属性最强的元素是Na,最活泼的非金属元素是F,
故答案为:Na;F;
(2)稀有气体Ar最外层为稳定结构,化学性质最不活泼,其原子结构示意图为: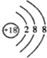 ,故答案为:Ar;
,故答案为:Ar; ;
;
(3)F元素没有最高价含氧酸,元素的最高价氧化物对应的水化物中酸性最强的是HClO4;Na的金属性最强,NaOH的碱性最强,Al(OH)3是两性氢氧化物,
故答案为:HClO4;NaOH;Al(OH)3;
(4)同周期自左而右原子半径减小,故在③~⑦元素中,原子半径最大的是Na,原子半径最小的是Cl,故答案为:Na;Cl;
(5)同周期自左而非金属性增强,单质的活泼性最强,故Cl2较硫活泼,Cl2+H2S=S↓+2HCl等可以说明单质的氧化性强弱,
故答案为:Cl2;Cl2+H2S=S↓+2HCl.
本题解析:
本题难度:一般
3、推断题 A、B、C、D、E、F、G均是原子序数小于36的元素。A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道;?C元素的基态原子最外层有3个未成对电子,次外层有2个电子;?D?的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2。
根据信息回答下列问题:?
(1)C的外围电子排布图为___________?。C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为__________;分子的VSEPR模型名称为___________;阴离子的立体构型为______________。
(2)G的价电子排布式为___________。用电子式表示化合物AE2的形成过程________。
(3)F与BD易形成配合物F(BD)5,在F(BD)5中F的化合价为_______;与BD分子互为等电子体的分子和离子分别为____________和____________(填化学式)。
(4)E有多种含氧酸根①EO-?②EO2-?③EO3-?④EO4-,其中空间构型为四面体型的是__________。(填序号)
(5)B、C、D、E原子相互化合形成的分子有多种,请列举两种分子内所有原子都满足最外层8电子稳定结构的分子:______________________(写分子式)?
参考答案:(1)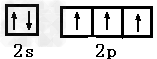 ?;?sp3?;正四面体?;?角型
?;?sp3?;正四面体?;?角型
(2)3d84s2?;“略”
(3)0?;N2?;CN-?
(4)④
(5)CO2、NCl3、CCl4、COCl2、N≡C-C≡N等中的任意2个
本题解析:
本题难度:一般
4、简答题 在第三周期元素中,除稀有气体元素外:
(1)原子半径最小的元素是______;(填元素符号)
(2)金属性最强的元素是______;(填元素符号)
(3)最高价氧化物对应水化物酸性最强的是______,(用化学式回答,下同):它对应的酸酐为______;
(4)最不稳定的气态氢化物是______;
(5)最高价氧化物对应水化物碱性最强的是______;
(6)氧化物中具有两性的是______.
参考答案:(1)同周期元素的原子,从左到右原子半径逐渐减小,所以半径最小的是Cl,故答案为:Cl;
(2)同周期元素的原子,从左到右金属性逐渐减弱,所以金属性最强的是Na,故答案为:Na;
(3)同周期元素的原子,从左到右最高价氧化物对应的水化物的酸性逐渐增强,所以酸性最强的是HClO4,它的酸酐是Cl2O7,故答案为:HClO4;Cl2O7;
(4)同周期元素的原子,从左到右氢化物越来越稳定,最不稳定的是:SiH4,故答案为:SiH4;
(5)同周期元素的原子,从左到右最高价氧化物对应的水化物的碱性逐渐减弱,所以碱性最强的是NaOH,故答案为:NaOH;
(6)具有两是性的氧化物Al2O3,故答案为:Al2O3.
本题解析:
本题难度:一般
5、选择题 某元素的原子结构示意图为 ,该元素位于元素周期表中
,该元素位于元素周期表中
[? ]
A.第三周期、ⅢA族
B.第三周期、ⅡA族
C.第二周期、ⅢA族
D.第二周期、ⅡA族
参考答案:B
本题解析:
本题难度:简单