| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《水的电离平衡》高频考点预测(2017年最新版)(二)
参考答案:D 本题解析:各离子浓度大小为c(Na+)> c(HCO3-)> c(OH-)> c(H+)> c(CO32-) 本题难度:一般 3、选择题 常温下,在0.1 mol/LHF溶液中,水的离子积是 参考答案:A 本题解析:常温下,水的离子积是1.0×10-14. 本题难度:一般 4、选择题 下列各物质投入水中,因促进水的电离而使溶液呈碱性的是 |
参考答案:C
本题解析:酸碱抑制水的电离,能水解的盐促进水的电离,CH3COONa属于强碱弱酸盐,水解显碱性,NH4Cl属于强酸弱碱盐,水解显酸性,选C。
考点:考查影响水电离的因素。
本题难度:一般
5、选择题 已知某温度下纯水中的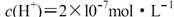 ,对此下列说法正确的是
,对此下列说法正确的是
A.据此无法求算水中c(OH-)
B.该温度低于25℃
C.此温度下水的离子积为常温下的两倍
D.若向水中加入少量盐酸,则水的电离度减小
参考答案:D
本题解析:纯水中的c(H+)=2×10-7mol/L,说明水的电离受到了促进。水电离出来的c(H+) 和c(OH-)是相等的,故c(OH-)= 2×10-7mol/L,A错;水的电离是吸热反应,电离受到了促进,所以是升高了温度,故温度高于25℃,B错;此温度下水的离子积为4×10-7mol/L,是常温下的4倍,C错;若向水中加入少量盐酸,水的电离受到抑制,则水的电离度减小,D对。
考点:水电离平衡的移动和水的离子积。
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点总结《二氧化硫》.. | ||