��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1����֪��25��ʱ��
��2CO(s)+ O2(g)==2CO2(g) ��H1����566KJ/mol
��C(s)+O2(g)==CO2(g) ��H2����394KJ/mol��
��̼��������Ӧ����һ����̼���Ȼ�ѧ����ʽΪ��_____________________________��
��2�������Ϊ2 L���ܱ������У�A��B��һ�������·�Ӧ����C��A(g)��2B(s)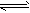 2C (g)����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� ____________ ���ڲ�ͬ�¶��´ﵽƽ��ʱ������C�����ʵ�������ͼ��ʾ����÷�Ӧ��____________��Ӧ������ȡ������ȡ� ������500�棬�ӷ�Ӧ��ʼ��ƽ�⣬C��ƽ����Ӧ����v(C) ��___________________��
2C (g)����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� ____________ ���ڲ�ͬ�¶��´ﵽƽ��ʱ������C�����ʵ�������ͼ��ʾ����÷�Ӧ��____________��Ӧ������ȡ������ȡ� ������500�棬�ӷ�Ӧ��ʼ��ƽ�⣬C��ƽ����Ӧ����v(C) ��___________________��

�ο��𰸣���1��2C (s)+O2(g)==2CO(g) ��H1����222kJ/mol
��2��K= �����ȣ�0��05mol/(L��min)
�����ȣ�0��05mol/(L��min)
���������
�����Ѷȣ�һ��
2������� ̼��̼�Ļ����������������������е�Ӧ�÷dz��㷺����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�
��1����ѧ���Խ��ܼ���Ϊ�����ĵ�̼����������أ���������Υ����չ��̼���õ���______������ţ�
A�����ԭ�������ʣ���չ��ɫ��ѧ
B��������չ������ҵ�������������������
C���ƹ�ú��������Һ���������ṩ����Чȼ��
D����������̫���ܡ����ܡ����ܡ����ܵ���Դ
��2�������˺���������̬ϵͳ�У�����Ҫ������ȥCO2����Ҫ���ṩ�����O2��ij�ֵ绯ѧװ�ÿ�ʵ������ת����2CO2�T2CO+O2��CO������ȼ�ϣ���֪�÷�Ӧ��������ӦʽΪ��4OH--4e-��O2��+2H2O����������ӦʽΪ______��
��3��CO2��ת�����л���ʵ��̼ѭ���������ΪlL���ܱ������У�����1mol?CO2��3mol?H2��һ�������·�����Ӧ��
CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ?mol-1��
���CO2��CH2OH��g����Ũ����ʱ��仯��ͼ��ʾ��
�ٴ�3min��8min��v��H2��=______��
����˵��������Ӧ�ﵽƽ��״̬����______�����ţ���
A����Ӧ��CO2��CH2OH�����ʵ���Ũ��֮��Ϊ1��1����ͼ�н���㣩
B�����������ܶȲ���ʱ�ŵı仯���仯
C����λʱ����ÿ����3mol?H2��ͬʱ����1mol?H2O
D��CO2����������ڻ�������б��ֲ���
��4����֪��
��C��s��+O2��g���TCO2��g������H1=-437.3kJ?mol-1
��2H2��g��+O2��g���T2H2O��g������H2=-571.6kJ?mol-1
��2CO��g��+O2��g���T2CO2��g������H3=-566.0kJ?mol-1
��C��s��+H2O��g���TCO��g��+H2��g������H=______��
��5��ij���ױ�������30�桢30MPa�����£���Fe��COCl2��������CO2��H2��Ӧ���ɶ�������飮�ٶ���һ�����г���һ������CO2��H2�������������CO2��H2��ת���ʾ�Ϊ100%������ֻ�ж�������飬
=a����a��ȡֵ��ΧΪ______��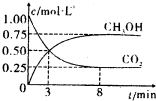
�ο��𰸣���1��A�����ԭ�������ʣ���չ��ɫ��ѧ�����Լ�����Ⱦ�����ϵ�̼���õ������A��ȷ��
B��������չ������ҵ������������������������ŷŴ�����β�����������̼�ȣ������ϵ�̼���õ������B����
C���ƹ�ú��������Һ���������ṩ����Чȼ�ϣ����Լ�����Ⱦ�����ϵ�̼���õ������C��ȷ��
D����������̫���ܡ����ܡ����ܡ����ܵ���Դ�����Լ�����Ⱦ�����ϵ�̼���õ������D��ȷ��
��ѡ��B��
��2���ܷ�ӦʽΪ2CO2=2CO+O2��������ӦΪ4OH--4e-=O2��+2H2O���ܷ�Ӧʽ��ȥ������Ӧʽ��������Ӧʽ��2CO2+4e-+2H2O=2CO+4OH-��
�ʴ�Ϊ��2CO2+4e-+2H2O=2CO+4OH-��
��3����v��CH3OH��=0.75mol/L-0.50mol/L5min=0.05mol/��L?min����v��H2��=3v��CH3OH��=0.15mol/��L?min�����ʴ�Ϊ��0.15mol/��L?min����
��A����ͼ��֪��Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1��1ʱ����δ�ﵽƽ��״̬����A����
B����������������䣬������������䣬�������Ƿ�ﵽƽ��״̬�������ڻ��������ܶȲ���ʱ��ı仯���仯�������ж��Ƿ�ﵽƽ��״̬����B����
C�������Ƿ�ﵽƽ��״̬�������ڵ�λʱ����ÿ����3molH2��ͬʱ����1molH2O����C����
D��CO2����������ڻ�������б��ֲ��䣬˵���ﵽƽ��״̬����D��ȷ��
��ѡ��D��
��4����C��s��+O2��g���TCO2��g������H1=-437.3kJ?mol-1
��2H2��g��+O2��g���T2H2O��g������H2=-571.6kJ?mol-1
��2CO��g��+O2��g���T2CO2��g������H3=-566.0kJ?mol-1
�ɸ�˹���ɣ���+�ڡ�12-�ۡ�12����C��s��+H2O��g���TCO��g��+H2��g������H=+131.5kJ?mol-1��
�ʴ�Ϊ��+131.5kJ?mol-1��
��5��CO2��H2ת��Ϊ���飬4CO2+13H2һ������
���������
�����Ѷȣ�һ��
3������� ��ú��Ϊȼ�Ͽ�ͨ����������;����
;����C(s)+O2(g)  CO2(g) (1mol̼���ʷ�Ӧ����Q1 kJ)
CO2(g) (1mol̼���ʷ�Ӧ����Q1 kJ)
;��������ˮú�� C(s)+H2O(g) CO(g)+H2(g) (1mol̼���ʷ�Ӧ����Q2 kJ)
CO(g)+H2(g) (1mol̼���ʷ�Ӧ����Q2 kJ)
��ȼ��ˮú�� 2CO(g)+O2(g)  2CO2(g)
2CO2(g)
2H2(g)+O2(g) 2H2O(g) (1molCO��1molH2��Ӧ������Q3 kJ)
2H2O(g) (1molCO��1molH2��Ӧ������Q3 kJ)
�Իش��������⣺
��1���������ʵ����ĵ���̼��Ӧʱ��;����ų�������_________(����ڡ��������ڡ���С�ڡ�);����ų���������
��2��Q1 ��Q2 ��Q3 ����ѧ��ϵʽ��__________________��
��3��������ȡˮú����Ӧ�����ȷ�Ӧ�����Է�Ӧ�������е�������________(����ڡ��������ڡ���С�ڡ�)�����������е���������
��4������úͨ��;������Ϊȼ�ϵ����壺_____________��
�ο��𰸣���1������
��2��Q1 = Q3- Q2
��3����
��4��ȼ�ճ�֣���Լ��Դ����Ⱦ��
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪H2��g����C2H4��g����C2H5OH��l����ȼ���ȷֱ���285.8kJ?mol-1��1411.0kJ?mol-1��1366.8kJ?mol-1������C2H4��g����H2O��l����Ӧ����C2H5OH��l���ġ�HΪ��������
A��-44.2?kJ?mol-1
B��+44.2?kJ?mol-1
C��-330?kJ?mol-1
D��+330?kJ?mol-1
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� ��������ʱ������(N2H4)Ϊȼ�ϣ��ö�������Ϊ�����������������ʷ�Ӧ���ɵ�����ˮ��������֪��
N2(g)+2O2(g)=2NO2(g) ��H1=+67.7 kJ��mol-1; ��
N2H4(g)+O2(g)=N2(g)+2H2O(g) ��H2= - 534 kJ��mol-1�� ��
�Լ���1mol�ºͶ���������ȫ��Ӧʱ�ų�������Ϊ_______________kJ��д���������������Ӧ���Ȼ�ѧ����ʽ��________________��
�ο��𰸣�567.85 ��2N2H4(g)+2NO2(g)=3N2(g)+ 4H2O(g) ��H=-11317kJ��mol-1
���������
�����Ѷȣ�һ��