微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 7.8g过氧化钠投入足量水中生成的气体在标准状况下的体积是多少升?若把生成的溶液用2mol/L的硫酸来完全中和,需硫酸溶液的体积是多少?
参考答案:n(Na2O2)=7.8g78g/mol=0.1mol,
2Na2O2+2H2O=4NaOH+O2↑
2mol? 4mol? 22.4L
0.1mol?n? V
n(NaOH)=0.2mol,V(O2)=1.12L,
H2SO4+2NaOH=Na2SO4+2H2O
1? ?2
n(H2SO4)? 0.2mol
n(H2SO4)=0.1mol,
V(H2SO4)=0.1mol2mol/L=0.05L.
答:生成的气体在标准状况下的体积是1.12L,需硫酸溶液的体积是0.05L.
本题解析:
本题难度:一般
2、填空题 向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式 。
(2)整个过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为 色;继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为20~50 mg・kg-1。制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
参考答案:(1)I2+5Cl2+6H2O=2HIO3+10HCl
(2)KI、I2 (3)红棕 HBrO3>Cl2>HIO3 (4)10.58
本题解析:(1)CCl4层变成紫色说明有I2生成,继续滴加氯水变成无色,说明I2又被氧化生成HIO3,同时生成HCl。(2)首先KI被氧化生成I2,后来I2又被氧化生成KIO3,所以整个过程中的还原剂是KI、I2。(3)Br2的CCl4溶液显红棕色;继续滴加氯水,CCl4层颜色没有变化,说明氯水能氧化I2但不能氧化Br2,结合第(1)问可得氧化性HBrO3>Cl2>HIO3。(4)KI被Cl2氧化成KIO3,对应关系式为
I- ~ KIO3 ~ 3Cl2
1 mol 3 mol
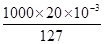 mol n(Cl2)
mol n(Cl2)
则n(Cl2)=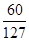 mol,V(Cl2)=
mol,V(Cl2)=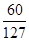 mol×22.4 L・mol-1≈10.58 L。
mol×22.4 L・mol-1≈10.58 L。
本题难度:一般
3、选择题 二氧化硫是造成酸雨的主要成分之一,二氧化硫排放到空气中溶于水生成亚硫酸(H2SO3),其中亚硫酸中硫元素(S)的化合价为(? )
A.+2
B.-2
C.+4
D.+6
参考答案:C
本题解析:根据化合物中正负价代数和为0可知,亚硫酸中氢和氧化合价分别是+1价和-2价,所以硫的化合价是+4价。答案选C。
本题难度:简单
4、选择题 某CuO粉末与适量的硫酸(ρ=1.7g?cm-3)在微热下充分反应,冷却后恰好全部形成CuSO4?5H2O(设反应过程中无水份损失).则此硫酸溶液的物质的量浓度为( )
A.8.5mol?L-1
B.10.0mol?L-1
C.17.0mol?L-1
D.18.4mol?L-1
参考答案:CuO粉末与适量的硫酸微热下充分反应,冷却后恰好全部形成CuSO4?5H2O,可以改写呈成CuO?H2SO4?4H2O,故原硫酸溶液中m(H2SO4):m(H2O)=98:4×18=98:72,故该硫酸的质量分数为9898+72=98170,该硫酸的密度ρ=1.7g?cm-3,故该硫酸的物质的量浓度c=1000×1.7×9817098mol/L=10mol/L,
故选B.
本题解析:
本题难度:简单
5、填空题 (16分) 以电解法生产金属锰产生的阳极泥中,其锰含量高达40%~50%,主要成分为MnO2的水合物,且含有显著量的Pb2+、Sn2+等重金属杂质。本工艺采用的木屑富含的纤维素在较浓硫酸的作用下膨胀、水解生成还原糖,酸性条件下,可与二氧化锰反应生成可溶性的硫酸锰。

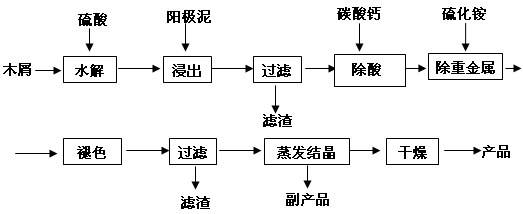
(1)工业上电解硫酸锰的水溶液生产金属锰,阳极的电极反应式为 。
(2)写出木屑水解反应的化学方程式: 。配平浸出步骤反应方程式C6H12O6 + MnO2 + H2SO4→ MnSO4 + CO2 + H2O
(3)若取消除酸操作步骤,将会产生 气体(填化学式)而污染环境;
(4)本工艺的一种副产品是重要的农业生产资料,写出其化学式 ;
(5)取一定量的阳极泥进行实验分析,得到如下图像。硫酸的最合适用量为 mL,若再增加硫酸的用量,将会导致 (填化学式)的消耗量增大。

(6)某阳极泥中MnO2(相对分子质量为87)的质量分数为50.0%,将174g该阳极泥与320g36.5%的浓盐酸混合加热,则产生的氯气在标准状况下应少于 L。(假设阳极泥中的其它成分不参与反应)
参考答案:(1)4OH- -4e-=O2 + 2H2O 或2H2O
本题解析:
本题难度:困难