��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��16�֣�ij�о���ѧϰС��Ϊ�о�������Ũ���ᷴӦ����������ijɷݲ��ⶨ������ĺ���������������ʵ�飺
��ʵ���Ʋ⡿������������Ũ���ᷴӦ������SO2��H2�������塣
(1)��С���������Ʋ�������ǣ�?��
��ʵ������a����ѡ���ҩƷ�����ۡ�Ũ���ᡢ����ͭ��ĩ��0.2 mol/L��H2C2O4����Һ��0.1 mol/L������KMnO4����Һ�����ָʾ����
b��ʵ��װ����Ƽ���װ(���ȼ��г�װ�þ�����ȥ)
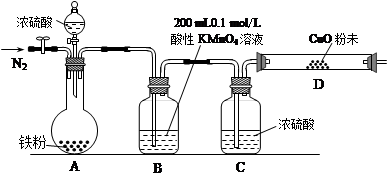
��ʵ����̼����ݴ�����
(2)B�з�����Ӧ�����ӷ���ʽΪ��?��
(3)ʵ��ǰ��ͨ��һ��ʱ���N2����Ŀ����?��
(4)B��C��D����ʢ�Լ�����������֤ʵ���ɵ�������ͬʱ����SO2��H2��������?
?��
(5)A�з�Ӧ��������ͨN2ʹA�����ɵ�����ȫ���ϳ�����B��D�з�Ӧ��ȫ���Ⱥ�����ȡ��B�з�Ӧ�����Һ����ƿ�У�ÿ��ȡ��25 mL����H2C2O4����Һ���еζ���
��H2C2O4����Һ������KMnO4��Һ��Ӧ�����ӷ���ʽ���£��뽫�÷���ʽ��ɲ���ƽ��
(? )H2C2O4+(? )MnO4- +(? )H+ ��(? )Mn2+ +(? ) H2O+(? ) (? )
�ڵζ��ﵽ�յ�ʱ��������?��
���ظ��ζ����Σ�ƽ��ÿ�κ���H2C2O4����Һ15.63 mL��������Ũ���ᷴӦ������SO2��������ʵ���Ϊ?����������ʵ��ǰ��װ��D����������0.9 g���������������SO2���������Ϊ?��
�ο��𰸣���16�֣�(1)�ڼ��ȵ�������Ũ������Fe��Ӧ����SO2�����ŷ�Ӧ�Ľ��У�����Ũ�ȱ�ϡ����Fe��Ӧ����H2
(2) 5SO2+2MnO4-+2H2O��5SO42-+2Mn2++4H+
(3) �ų�װ���еĿ�������ֹH2�����������ȷ�����ը��
(4) Bƿ����Һ�Ϻ�ɫ��dz˵��������SO2��D�к�ɫ��ĩ���˵��������H2��(���һ�ֵ�1��)
(5) ��5��2��6��2��8��10CO2?
�ڵ������һ��H2C2O4��ҺʱKMnO4��Һ���Ϻ�ɫ��ȥ�Ұ����֮�ڲ��ָ���
��0.025 mol�� 33.3%
�����������1�������ڼ��ȵ�������Ũ������Fe��Ӧ����SO2�����ŷ�Ӧ�Ľ��У�����Ũ�ȱ�ϡ��
��Fe��Ӧ����H2��
��2�����Ը��������Һ���������ԣ�������SO2�����Է���ʽΪ5SO2+2MnO4-+2H2O��5SO42-+2Mn2++4H+��
��3�����ڿ����к����������ڼ��ȵ���������������������ը������ͨ�뵪����Ϊ���ų�װ���еĿ�������ֹH2�����������ȷ�����ը��
��4��SO2���л�ԭ�ԣ���ʹ���Ը��������Һ��ɫ���������л�ԭ�ԣ���ʹ��ɫ����ͭ��ԭ�ɺ�ɫ��ͭ��
��5�����ڷ�Ӧ��1mol������صõ�5mol���ӣ�������̼�Ļ��ϼ��ǣ�3�ۣ�����������CO2������1mol������ʧȥ2mol���ӣ�����������ͻ�ԭ�������ʵ���֮����2�U5�����Է���ʽΪ5H2C2O4+2MnO4- +6H+ ��2Mn2+ +8H2O+10CO2��
���������Ը��������Һ���Ϻ�ɫ�������յ�ʱ�������ǵ������һ��H2C2O4��ҺʱKMnO4��Һ���Ϻ�ɫ��ȥ�Ұ����֮�ڲ��ָ���
�����IJ�������ʵ�����0.01563L��0.2 mol/L=0.003126mol���������ĸ��������
0.0012504mol������ʣ����������0.0012504mol��8��0.01mol������SO2��Ӧ�ĸ������
��0.02mol��0.01mol��0.01mol������SO2��0.025mol��D����������0.9 g������ݷ�Ӧʽ
CuO��H2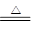 Cu��H2O��֪��������0.8��19��0.05mol������SO2�����������
Cu��H2O��֪��������0.8��19��0.05mol������SO2�����������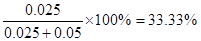
�����Ѷȣ�һ��
2��ѡ���� ���Ȼ�����Һ��ͨ��SO2����Һ�Գ��壬�����Ȼ�����Һ��װ�����Թ��У�һ֧ͨ��������һ֧���ռ���Һ��Ȼ����ͨ��SO2��������Թܶ����а�ɫ�������ɴ˵ó������н��ۺ������ǣ�?��
A���Ȼ�����������
B��SO2�л�ԭ�Ժ�����
C����֧�Թ��ڰ�ɫ�������������ᱵ
D���Ȼ�����Һ��ͨ��SO2����Һ�Գ����ԭ��������SO2�������������������Ⱶ
�ο��𰸣�B
�����������
�����Ѷȣ���
3��ʵ���� ��8�֣�ij�о���ѧϰС���˫��ˮ��չ�����о���
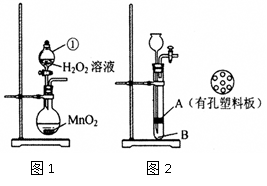
��1��ͼ1�������ٵ�����?����װ���з����Ļ�ѧ����ʽΪ?
?��ͼ1װ��Ҳ��������ʵ������?���壨ֻ��һ�ּ��ɣ�
��2��С��ͬѧ��MnO2��ˮ�ఴһ��������ˮ��ϡ����̣�������С��״���壬����ͼ2װ�������������Է���ʵ��������ն������̡�ʵ��ǰ����װ�������Եķ����ǣ�
���������ӳ���©����עˮ��?���ر�����������עˮ��ʹ©����Һ���Ը����Թ���Һ�棬һ��ʱ��߶Ȳ�䣬˵�����������á����п�״����Ӧ������?�����A����B����
��3������ͼ2װ�÷�Ӧһ��ʱ�����ֹͣ��Ӧ���������?��
��4��Cu��ϡ�����ֱ�ӷ�Ӧ�����μ�H2O2��Һ�����ȣ�������ˮ��һ����ɫ��Һ����÷�Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1����Һ©����2H2O2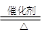 2H2O+O2����H2��CO2
2H2O+O2����H2��CO2
��2����û©���¶ˣ����γ�Һ�⣩��A����3���ر���������ÿ��1�֣�
��4��Cu+H2SO4+H2O2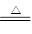 CuSO4+2H2O��2�֣�
CuSO4+2H2O��2�֣�
�����������1�����������Ĺ����֪�����Ƿ�Һ©������װ������ȡ�����ģ�����ʽ��2H2O2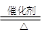 2H2O+O2��������װ�õ��ص��֪����������ȡ������CO2��
2H2O+O2��������װ�õ��ص��֪����������ȡ������CO2��
��2�������Ƿ�Һ©����������Ҫ��û©���¶ˣ����γ�Һ�⣩��Ϊ����ʹ���ư�����ֹͣ�Ϳ�ʼ����״����Ӧ�÷���A����
��3����ֹͣ��Ӧ���ر���������ѹ���������£��������Һ���룬��Ӧ��ֹͣ��
��4�����ݷ�Ӧ����������״����Ӧ�ķ���ʽӦ����Cu+H2SO4+H2O2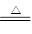 CuSO4+2H2O��
CuSO4+2H2O��
�����Ѷȣ�һ��
4��ѡ���� ��֪ijԪ�ص���������ϼ�Ϊ+ 6�ۣ��ɴ˵ó��Ľ�����ȷ����
A����Ԫ����Ԫ�����ڱ���һ�����ڢ�A��
B����Ԫ�ؿ�������Ԫ��
C����Ԫ�ؿ���������Se��Ԫ��
D����Ԫ��ԭ�������һ����6������
�ο��𰸣�C
����������������Ϊ+6�۵�Ԫ�س��ˢ�A��(������)���������Ǣ�B��Ԫ���磺��(Cr)�ȣ��������ֻ��һ�����ӡ���A��B��D��˵�����Ǵ���ġ�
�����Ѷȣ�һ��
5��ʵ���� ��ҵ�ϳ�����������ʢװ��Ũ���ᡣij��ȤС���ͬѧ���֣���һ������������Ũ�������ʱ���۲쵽������ȫ�ܽ⣬�������������塣ʵ�������������Լ���?0.01 mol/L ����KMnO4��Һ��0.10 mol/L KI��Һ��������ˮ��������Һ������ˮ������Э������̽��������Һ������ijɷ֡�
��������롿
��������Һ�еĽ������ӿ��ܺ���Fe2����Fe3���е�һ�ֻ����֣�
�����������п϶�����?���塣
��ʵ��̽����
?
| ʵ�����
| Ԥ������
| ��?��
|
��֤�����
| ����٣�ȡ����0.01 mol/L ����KMnO4��Һ������������Һ��
| ?
| ?
|
����ڣ�?
| ?
| ����Fe3��
|
��֤�����
| ����������ͨ������װ��
| ?
| �������ֻ���������
|
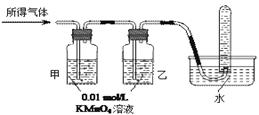
���������ۡ�
��1����ͬѧ�����������ѡ��KSCN��Һ���������KSCN��������ˮ������Һ������ɲ���������̽���������Ƿ���У���˵��ԭ��?��
��2����ͬѧ������Թ������������H2��Q���壬Ϊ�����������ʵ��װ������ͼ��ͼ�мг�����ʡ�ԣ���
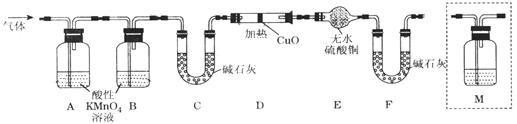
��Q������ԭ����?���û�ѧ����ʽ��ʾ����
��Ϊȷ��Q�Ĵ��ڣ���M��ʢ�ŵ��Լ�Ϊ?������װ��M������?��ѡ����ţ���
a��A֮ǰ? b��A-B��? c��B-C��? d��C-D��
��װ��ͼ��D��E��F��ϵ�������?��
�ο��𰸣�SO2?
��ʵ��̽����
�������Һ�Ϻ�ɫ��ȥ������Fe2��
�������ȡ����������Һ���μ�KI�͵�����Һ����Һ��Ϊ��ɫ��������ȡ������Һ���μ�����KSCN��Һ����Һ���Ѫ��ɫ����
��������KMnO4��Һ��ɫ������KMnO4��Һ��ɫ���䣬�Թ����ռ�������
���������ۡ�
��1������ȷ��1�֣�������Һ�к���Fe3������������Һ���Ƿ���Fe2��
��2����C+2H2SO4(Ũ)=CO2��+2SO2��+2H2O
�ڳ���ʯ��ˮ��c?��ȷ���Ƿ���H2
�����������������롿Ũ��������ڼ��������·�Ӧ���ɶ��������������������п϶�����SO2����Ϊ��SO2��
��ʵ��̽������֤�����������Һ�еĽ������ӿ��ܺ���Fe2����Fe3���е�һ�ֻ����֣�
���Ը��������Һ���Ϻ�ɫ����ǿ�����ԣ������������л�ԭ�ԣ����Ը�������ܱ����������ӻ�ԭ��ʹ�Ϻ�ɫ��ȥ������������Һ�Ϻ�ɫ��ȥ��˵�����ж��������ӣ�����û�У��⻯���л�ԭ�ԣ������������������ԣ��������ܱ������������������ɵ��ʵ⣬�������۱���ɫ�����Բ������ȡ����������Һ���μ�KI��Һ�͵�����Һ�������Һ��Ϊ��ɫ��˵���������������ӣ�����û�У���Ϊ����Һ�Ϻ�ɫ��ȥ������Fe2+����ȡ����������Һ���μ�KI��Һ�͵�����Һ����Һ��Ϊ��ɫ��
��������������п϶�����SO2���壻
���������л�ԭ�ԣ���ʹ���Ը��������Һ��ɫ����������ʹ���Ը��������Һ��ɫ����������������ˮ�������������KMnO4��Һ��ɫ��˵�����ж�����������KMnO4��Һ��ɫ���䣬˵������������ȫ�����գ�����Թ����ռ����壬ֻ������������Ϊ������KMnO4��Һ��ɫ������KMnO4��Һ��ɫ���䣬�Թ����ռ������壻
���������ۡ�
��1����ˮ���������ԣ������������л�ԭ�ԣ���ˮ�ܽ����������������������������ӣ�KSCNֻ�ܼ������������Ӳ��ܼ�����������ӣ���������Һ�к���Fe3+����������Һ���Ƿ���Fe2+�����Ըù۵㲻��ȷ����Ϊ������ȷ������Һ�к���Fe3+����������Һ���Ƿ���Fe2+��
��2�����ڼ���ʱ�������в�������Ũ���ᷴӦ��̼Ҳ��Ũ���ᷴӦ�������ɶ�����������̼��ˮ����Ӧ����ʽΪC+2H2SO4(Ũ)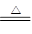 CO2��+2SO2��+2H2O����QΪ������̼��������̼�Ͷ���������ʹ����ʯ��ˮ����ǣ�ѡ��a��b�ܶ��������Ӱ�����ж϶�����̼�Ĵ��ڣ�ѡdʱ������̼����ʯ�����գ���Ϊ�������ʯ��ˮ��C���۸������������ʷ������������л�ԭ�ԣ��ܻ�ԭ��ɫ������ͭ������ˮ��ˮ��ʹ��ɫ����ˮ����ͭ��������Ϊ��ȷ���Ƿ���H2��
CO2��+2SO2��+2H2O����QΪ������̼��������̼�Ͷ���������ʹ����ʯ��ˮ����ǣ�ѡ��a��b�ܶ��������Ӱ�����ж϶�����̼�Ĵ��ڣ�ѡdʱ������̼����ʯ�����գ���Ϊ�������ʯ��ˮ��C���۸������������ʷ������������л�ԭ�ԣ��ܻ�ԭ��ɫ������ͭ������ˮ��ˮ��ʹ��ɫ����ˮ����ͭ��������Ϊ��ȷ���Ƿ���H2��
�����Ѷȣ�һ��