微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法中不正确的是
[? ]
A.“暖冰”也是水分子间通过氢键结合而成的固体
B.水凝固形成20℃时的“暖冰”所发生的变化是化学变化
C.水凝固形成20℃时的“暖冰”所发生的变化是物理变化
D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
2、填空题 化学键的键能是指气态原子间形成1mol化学键时释放的能量。如:H(g)+I(g)→H-I(g)+297KJ 即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297KJ的热量。化学反应的发生可以看成旧化学键的破坏和新化学键的形成。下表是一些键能数据。(单位:kJ/mol)
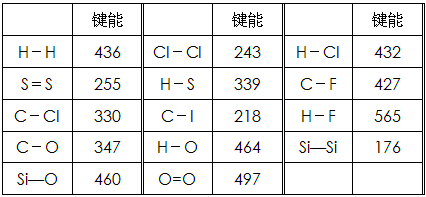
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性_________(填“大于”或“小于”)CF4的稳定性。试预测C-Br键的键能范围_________<C-Br键能<_________
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)=2HCl(g) ΔH=-QKJ/ mol;通过计算确定热化学方程式中Q的值为______________
(3)有人认为:H-O键的键能大于H-S键的键能,所以H2O的熔沸点高于H2S的熔沸点。你是否赞同这种观点?如不赞同,请说出你的解释。________________________________________
(4)①Si-Si键能小于Si-O键能的理由是:________________________________
②请写出晶体硅与氧气反应生成二氧化硅的热化学方程式:______________________________
3、填空题 镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有____________________。
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如下图所示,请改正图中错误:_____________________。
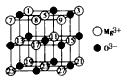
(3)用镁粉、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:_____________________________。
(4) Mg是第三周期元素,该周期部分元素氟化物的熔点见下表。氟化物的熔点

解释表中氟化物熔点差异的原因:________________________。
(5)人工模拟酶是当前研究的热点。有研究表明,化合物X可用于研究模拟酶,当其结合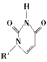 或Cu(I) (I表示化合价为+1)时,分别形成a和b:?
或Cu(I) (I表示化合价为+1)时,分别形成a和b:?
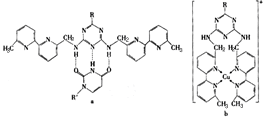
①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有_________键的特性。
②粒子间作用力包括化学键和分子问作用力,比较a和b中粒子间作用力的差异______________。
4、选择题 下列有关HF、HCl、HBr、HI的说法错误的是
[? ]
A.均为直线形极性分子
B.熔、沸点依次增大
C.稳定性依次减弱
D.还原性依次增强
5、选择题 以下说法正确的是( )
A.C60与金刚石一样属于原子晶体
B.干冰升华破坏了共价键
C.正丁烷、异丁烷互为同分异构体
D.由于水分子之间存在氢键,所以水分子比较稳定