微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
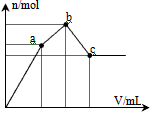
1、选择题 向100 mL 0.1 mol・L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol・L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
[? ]
A.a点对应的沉淀只有BaSO4
B.c点溶液呈碱性
C.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-==Al(OH)3↓+2BaSO4↓
D.c点加入Ba(OH)2溶液的体积为200 mL
参考答案:B
本题解析:
本题难度:一般
2、选择题 实验室中,要使AlCl3溶液中的Al3+全部沉淀出来,适宜用的试剂是
[? ]
A.NaOH溶液
B.Ba(OH)2溶液
C.盐酸
D.氨水
参考答案:D
本题解析:
本题难度:简单
3、填空题 国务院强调“南水北调”工程必须坚持“三先三后”的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、
Cu2+、Ag+.试分析回答下列问题:
(1)该废液中可能大量存在的一种阴离子是________(选填序号).
A.SO42-?B.NO3-?C.Cl-?D.CO32-
(2)检验废液中铝元素的含量,需将其从废水样品中分离出来,所用的试剂可以是________,铝元素发生变化的离子方程式是______________________.
(3)为了回收废液中的金属银,某同学设计了如下方案
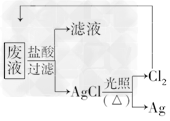
若依该方案获得银108?g,为保证不污染环境和氯气的循环利用,理论上应提供标准状况下的氢气________L.
参考答案:(1)B
(2)NaOH溶液;Al3++4OH-===AlO2-+2H2O
(3)11.2
本题解析:
本题难度:一般
4、选择题 在实验室里,要想使AlCl3溶液中的Al3+全部沉淀出来 ,应选用下列试剂中的
[? ]
A.Ba(OH)2溶液
B.NaOH溶液
C.氨水
D.硫酸
参考答案:C
本题解析:
本题难度:一般
5、填空题 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为_______________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式 ____________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是____________________。(填序号)
① 硫酸铝和氢氧化钠 ② 硫酸铝和氨水③ 硫酸锌和氢氧化钠④ 硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式 __________________________。试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因_______________________
参考答案:(1)AlO2-(或Al(OH)4-)
(2)Zn+2NaOH==Na2ZnO2+H2↑ (或Zn+2NaOH+2H2O==Na2Zn(OH)4+H2↑)
(3)①③④
(4)Al3++3NH3・H2O==Al(OH)3↓+3NH4+;可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成Zn(NH3)42+,氨水的用量不易控制
本题解析:
本题难度:一般