微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A是一种来自石油的重要的有机化工原料,E是一种具有果香味的有机物,F是一种高聚物,可制成多种包装材料.(过程中的水或其他物质已省略)
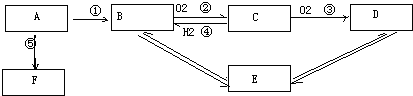
(1)写出下列物质的结构简式:A、______?C、______F、______
(2)写出反应化学方程式
①反应______?②反应______
B和D生成E______
E与NaOH溶液共热______
(3)丙烯(CH2=CHCH3)与A的结构相似,写出丙烯生成高聚物的方程式
______.
参考答案:A是一种来自石油的重要的有机化工原料,可以知道A是乙烯,根据B氧气
本题解析:
本题难度:一般
2、选择题 一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为
A.3.0 mol
B.1.5 mol
C.1.0 mol
D.0.75 mol
参考答案:B
本题解析:PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,发生的的氧化还原反应。由于在氧化还原反应中氧化剂得到的电子与还原剂失去的电子的物质的量相等。所以化合价升高与降低的总数相等。Cr3+→Cr2O72-,化合价从+3→+6,1 mol Cr3+反应失去电子3mol,但是PbO2→Pb2+,化合价从+4→+2,1 mol PbO2反应得到电子2mol,因此所需PbO2的物质的量为3÷2="1.5" mol。故正确选项为B。
本题难度:一般
3、选择题 下列说法中正确的是
A.金属单质在化学反应中只能做还原剂
B.非金属单质在化学反应中只能做氧化剂
C.金属原子在化学反应中失去的电子越多,其还原性就越强
D.分解反应一定是氧化还原反应
参考答案:A
本题解析:略
本题难度:一般
4、简答题 0.4g氢氧化钠恰好与10ml的盐酸完全反应,试求这种盐酸的物质的量浓度是多少?
参考答案:NaOH的物质的量为0.4g40g/mol=0.01mol,
由NaOH+HCl=NaCl+H2O
? 1? 1
则HCl的物质的量为0.01mol,
盐酸10mL,则盐酸的浓度为0.01mol0.01L=1mol/L,
答:这种盐酸的物质的量浓度为1mol/L.
本题解析:
本题难度:一般
5、选择题 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是
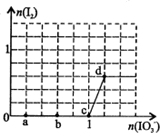
A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3-+ 2IO3- =I2+5SO42-+3H++H2O