微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.NA个H2SO4分子的总质量就是H2SO4的摩尔质量
B.将40 g烧碱溶于水得溶液甲,再向甲中通入1 mol HCl得溶液乙(假设过程中溶液体积不变),则在相同温度下,甲和乙的导电能力一样
C.1 L 0.1 mol/L HF溶液中含有的离子总数约为0.2 NA
D.标况下22.4 L SO3溶解于水并稀释为1 L后,溶液中c(H+)=2 mol/L
2、选择题 溴乙烷中含有少量乙醇杂质,下列方法中可以除去该杂质的是( ? )
A.加入浓硫酸并加热到170℃,使乙醇变成乙烯而逸出
B.加入氢溴酸并加热,使乙醇转化为溴乙烷
C.加入金属钠,使乙醇发生反应而除去
D.加水振荡,静置分层后,用分液漏斗分离去水层
3、选择题 可以用分液漏斗分离的一组液体混合物是(?)
A.溴和四氯化碳
B.苯和溴苯
C.汽油和苯
D.硝基苯和水
4、填空题 过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
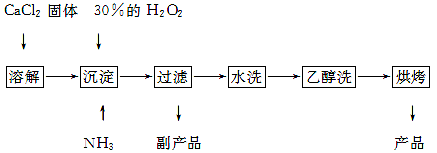
已知CaO2・8H2O呈白色,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)用上述方法制取CaO2・8H2O的化学方程式是?;
(2)检验“水洗”是否合格的方法是?;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是(写出两种):
①?;
②?。
(4)测定产品中CaO2的含量的实验步骤:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol・L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol・L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
【已知:I2+2S2O32-=2I-+S4O62-】
①CaO2的质量分数为?(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能?(填“不受影响”、“偏低”或“偏高”),原因是?。
5、选择题 下列实验可以获得预期效果的是
[? ]
A.用金属钠检验乙醇中是否含有少量水?
B.用溴水除去苯中的少量苯酚
C.用质谱法测定有机物相对分子质量?
D.用湿润的pH试纸测定溶液的pH