��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���ǵ�ѭ���е���Ҫ���ʣ����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
(1)��֪��H��H����Ϊ436 kJ��mol��1��N��N����Ϊ946 kJ��mol��1��N��H����Ϊ391 kJ��mol��1��д���ϳɰ���Ӧ���Ȼ�ѧ����ʽ��?
(2)�����£���һ��4L���ܱ������г���5.2molH2��2molN2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±���ʾ��
ʱ��/min
| 5
| 10
| 15
| 20
| 25
| 30
|
c(NH3)/mol��L��1
| 0.08
| 0.14
| 0.18
| 0.20
| 0.20
| 0.20
|
��5min�ڣ�����H2��ƽ����Ӧ����Ϊ___________________________________?
��N2��ƽ��ת����?
�۴������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=__________________________����Ӧ�ﵽƽ�����ά������������䣬�¶Ȳ��䣬��ƽ����ϵ�м���H2��N2��NH3��8mol����ѧƽ�⽫��_______�����ƶ�(�����Ӧ�����淴Ӧ��)��
����ά������������䣬ֻ�����¶Ȼ�ѧƽ�ⳣ��ֵ?������С�����䣩������Ӧ����?������С�����䣩��
�����¶�ά�ֲ��䣬ֻ�����������4L��Ϊ2L������ƽ��ʱN2��ƽ��Ũ��?0.4 mol��L��1������ڡ�С�롢���ڣ�
�ο��𰸣�(1)N2(g)? +? 3H2(g)  2NH3 (g)?��H=��92kJ�� mol-1(3��)
2NH3 (g)?��H=��92kJ�� mol-1(3��)
(2)��0.024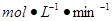 ? (2��)?��20%(2��)
? (2��)?��20%(2��)
�� O.1[��0.1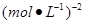 ] (2��)?����Ӧ? (2��)
] (2��)?����Ӧ? (2��)
�� ��С(2��)�����(2��)
�ݴ���(2��)
�����������
�����Ѷȣ�һ��
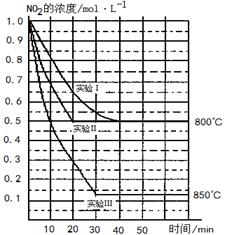
2������� ��12�֣�ij�����£���2L�ܱ������з������·�Ӧ��2NO2(g)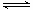 2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
2NO(g)��O2(g) ��H>0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ0 mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
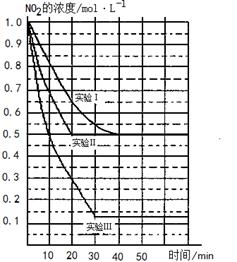
��ش��������⣺
��1������ͼ�б��϶�Ӧ�ķ�Ӧ�¶ȣ�800���850�棩��ʵ��������ķ�Ӧ������_______________________��
��2��д���÷�Ӧ��ƽ�ⳣ������ʽ��K=______________��
��3����ʵ����д�ƽ��������ܱ�������ͨ��1mol NO2��1mol NO������壨�����¶Ȳ��䣩����ƽ�⽫_________��������ƶ����������ƶ������ƶ�����
��4��һ��������NO2��SO2�ɷ�����Ӧ���䷽��ʽΪ��
NO2(g)��SO2(g)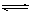 SO3(g)��NO(g) ��H>0����NO2��SO2�������
SO3(g)��NO(g) ��H>0����NO2��SO2�������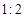 �����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����?����?��
�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����?����?��
A����ϵѹǿ���ֲ���? B�����������ɫ���ֲ���
C��SO3��NO������ȱ��ֲ���? D����������ƽ����Է����������ֲ���
��5�����ı�������ʹƽ�ⳣ����÷�Ӧ?����?��
A��һ��������Ӧ�����ƶ�? B����ƽ���ƶ�ʱ������Ӧ������������С
C��һ�����淴Ӧ�����ƶ�? D����ƽ���ƶ�ʱ���淴Ӧ������������С
�ο��𰸣���12�֣�ÿ��2�֣�
������
 ?ʹ���˴���
?ʹ���˴���
��������2 (NO) c(O2)/��2 (NO2)?���������ƶ�?������B?��5��A B
�����������1���¶�Խ�ߣ���Ӧ����Խ�죬�ﵽƽ���ʱ���Խ�̡���������Ӧʱ���ȷ�Ӧ�����������¶ȣ�ƽ��������Ӧ�����ƶ���NO2��Ũ�Ƚ��ͣ����ͼ��Ϊ�����𰸣���ʵ����ʵ��I��ƽ��״̬��ͬ�����ﵽƽ���ʱ���١�����Ϊ��Ӧ���������ĵģ����������ķ�Ӧ������ʹ���˴�����
��2����ѧ��������һ�������µĿ��淴Ӧ�У������淴Ӧ��Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ��ƽ�ⳣ����K����2 (NO) c(O2)/��2 (NO2)��
��3������ͼ���֪��ʵ��I��ƽ��ʱNO2��NO��������Ũ�ȷֱ���0.5mol/L��0.5mol/L��0.25mol/L������ʱͨ���NO2��NO��Ũ�ȶ���0.5mol/L�������¶Ȳ��䣬ƽ�ⳣ�����䣬ʵ��ƽ���Dz��ƶ��ġ�
��4����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬����ɫ��dz��Ũ���й�ϵ������B��ȷ�����ݷ���ʽ��֪����Ӧǰ����������Dz���ģ����ѹǿҲ�Dz���ģ�����A����˵����ͬ�����ݷ���ʽ��֪��SO3��NO�������ʼ����1�U1�ģ����ֲ��䣬C����˵�����������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����������ʵ������Dz���ģ�����DҲ����˵������ѡB��
��5����������Ӧ�����ȷ�Ӧ��ƽ�ⳣ�����˵���¶�һ�������ߵģ�ƽ��������Ӧ�����ƶ�������ѡ��A��B��ȷ��C����D�Ǵ���ģ��淴Ӧ����������Ȼ����������ѡAB��
������ƽ�ⳣ��ֻ���¶Ⱥͻ�ѧ�������й�ϵ��ƽ�ⳣ���ı䣬ֻ����ͨ���ı��¶�ʵ�֣�����ƽ���ƶ���������ϵ�ġ�
�����Ѷȣ�����
3��ѡ���� ���и������ݲ��ܷ�ӳ���淴Ӧ2A B+3C����ƽ��״̬����(? )
B+3C����ƽ��״̬����(? )
A��va(��)="2" mol��(L��min)-1��va(��)="2" mol��(L��min)-1
B��va(��)="2" mol��(L��min)-1��vb(��)="1" mol��(L��min)-1
C��vc(��)="1" mol��(L��min)-1��vb(��)="1.5" mol��(L��min)-1
D��va(��)="1" mol��(L��min)-1��vc(��)="1.5" mol��(L��min)-1
�ο��𰸣�C
����������жϿ��淴Ӧ�ﵽƽ��״̬�ı�־��v(��)=v(��)���ò�ͬ���ʱ�ʾ�������淴Ӧ���ʣ�Ҫͨ����ѧ����ʽ����������Ϊͬһ�����ʱ�ʾ��C���vb(��)�����vc(��)="4.5" mol��(L��min)-1��vc(��)��vc(��)���ʴ�ΪC�
�����Ѷȣ�һ��
4��ѡ���� ������ʵ����������������ԭ�����͵���
A������ˮ�д�������ƽ�⣺Br2+H2O  HBr+HBrO������NaOH��Һ����ɫ��dz
HBr+HBrO������NaOH��Һ����ɫ��dz
B����2HI H2��I2(g)ƽ����ϵ����ѹǿʹ��ɫ����
H2��I2(g)ƽ����ϵ����ѹǿʹ��ɫ����
C����ӦCO��NO2 CO2+NO ��H��0�����¶�ʹƽ�����淽���ƶ�
CO2+NO ��H��0�����¶�ʹƽ�����淽���ƶ�
D���ϳɰ���Ӧ��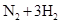

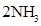 ����H��0 Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ
����H��0 Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ
�ο��𰸣�B
�������������ı�Ӱ��ƽ���һ����������ƽ������ܹ��������ָı�ķ�����У��������������ԭ������ԭ�����������е�ƽ����ϵ��ѡ��B�еķ�Ӧ�ڷ�Ӧǰ������Dz���ģ���������Խǿ��ƽ�ⲻ�ƶ�����ɫ��������Ϊ���ʵ��Ũ����������ģ������������������ԭ�������ͣ���ѡB��
�����Ѷȣ���
5������� ��֪ij��Ӧ�ĸ�����Ũ���������£�aA��g��+bB��g��

2C��g��
��ʼŨ�ȣ�mol/L����1.5?1.0?0
2sĩŨ�ȣ�mol/L����0.9?0.8?0.4
���a=______��b______����2S��B�ķ�Ӧ����=______��
�ο��𰸣�aA��g��+bB��g��

2C��g��
��ʼŨ�ȣ�mol/L����1.5? ? 1.0?0
�仯Ũ�ȣ�mol/L����0.6? ? 0.2? 0.4
2sĩŨ�ȣ�mol/L����0.9? ?0.8? ?0.4
��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ�����0.6��0.2��0.4=a��b��2�����a=3b=1��
�ʴ�Ϊ��a=3��B=1
��2S��B�ķ�Ӧ���ʣ�B��=��c(B)��t=0.2mol/L2s=0.1mol/��L?s����
�ʴ�Ϊ��0.1mol/��L?s��
���������
�����Ѷȣ�һ��