��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��8�֣�һ�����������ۺ�������������ɵ����ȼ����ڸ������������������գ�ʹ֮��ַ�Ӧ�������û������ϸ���ֳ����ȷݣ��ֱ�Ͷ��������ռ���Һ�������У���ַ�Ӧ��ǰ������m mol NaOH���ų�0.336 L���壻��������n mol HCl���ų�V L���塣�������������������ȼ���������������ϡ���ᷴӦ���ɵõ�3.36 L���壨����������ڱ�״���²ⶨ������
��1�������ȼ���ɳɷֵ�����������
��2��m��n��V��ֵ��
�ο��𰸣�(1)��(Al)="27.95%?" ��(Fe3O4)=72.05%
(2)m="0.05" mol? n="0.24" mol
V="1.344" L
����������������⣬�������ȷ�Ӧ��Ļ����Ͷ���ռ���Һ�У��������壬˵�����۹�����Fe3O4��ȫ��Ӧ�����ڵ������������ᡢ�Ӧ���ų�H2������ȣ���2Al��3H2��֪��
ԭ���ȼ�������������m1(Al)=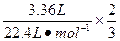 ��27 g��mol-1="2.7" g
��27 g��mol-1="2.7" g
�������ȷ�Ӧ��ʣ����������m2(Al)=  ��2��27 g��mol-1="0.54" g
��2��27 g��mol-1="0.54" g
���ȷ�Ӧ������������m3(Al)="2.7" g-0.54 g="2.16" g
(1)��8Al+3Fe3O4 9Fe+4Al2O3,��
9Fe+4Al2O3,��
m(Fe3O4)= ="6.96" g
="6.96" g
m(Fe)=  ="5.04" g
="5.04" g
m(Al2O3)= ="4.08" g
="4.08" g
�ʦ�(Al)=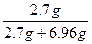 ��100%=27.95%
��100%=27.95%
��(Fe3O4)=1-27.95%=72.05%
(2)����ԭ���غ�Al��NaAlO2��NaOH
m="n(NaOH)="  ="0.05" mol
="0.05" mol
��2Al��6HCl��3H2? Al2O3��6HCl? Fe��2HCl��H2
n=n(HCl)= ��3+
��3+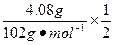 ��6+
��6+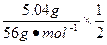 ��2="0.24" mol
��2="0.24" mol
V=V(H2)="("  )��22.4 L��mol-1="1.344" L
)��22.4 L��mol-1="1.344" L
�����Ѷȣ���
2��ѡ���� ȷ��ȡ6.0g��������Ʒ����SiO2��Fe2O3��������100mLϡ�����У���ַ�Ӧ������Һ�м���10mol?L����NaOH��Һ����������������/g�������꣩�ͼ���NaOH��Һ���/mL(������)֮��Ĺ�ϵ����ͼ��ʾ���������������ʵ���Ũ��Ϊ��mol?L������
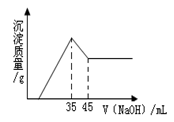
A��1.75
B��3.50
C��0.85
D����ȷ��
�ο��𰸣�A
�����������
�����Ѷȣ���
3������� ��Ҫ�ش��������⣮
��1�������£�Ũ����������������������ԭ���ǣ�______��
��2��ҽ���ϡ�θ��ƽ������Ҫ�ɷ�ΪAl��OH��3��������θ�ᣨ�����ᣩ�����ԭ����______��
��3������̼�����Ϊ�µ�ʱ������ȫ����C02�ŷ���Ҫ�����������������һ�֡���̼����ľٴ�______��
�ο��𰸣���1�������£�Ũ������ʹ������ۻ�����������һ�����ܵ�����Ĥ����������Ĥ������Ũ���ᣬ��ֹ�ڲ�����Ũ�����һ����Ӧ������Ũ��������������������棬
�ʴ�Ϊ������������Ũ�����л�ۻ���
��2��θ��ƽ[��Ҫ�ɷ�Al��OH��3]���Ժ�θ��ijɷ�����֮�䷢���кͷ�Ӧ����Al��OH��3+3HCl�TAlCl3+3H2O��
�ʴ�Ϊ��Al��OH��3������ᷢ������кͷ�Ӧ��
��3������̼���Ӧ����C02�ŷţ������еľٴ��磺��Լ��ֽ���õ磬��ʹ��һ���Կ��ӣ�ֲ�����֡����û�ʯȼ�ϵȣ�
�ʴ�Ϊ�����û�ʯȼ�ϣ�
���������
�����Ѷȣ�һ��
4��ѡ���� ���и������ʵ�ϡ��Һ���Ӧ��������ǰ�ߵ�����ߣ����Ǻ��ߵ���ǰ�ߣ���Ӧ������ͬ����
[? ]
A��NaHSO4��Ba(OH)2?
B��AlCl3��NaOH
C��NaAlO2��H2SO4?
D��Na2CO3��H2SO4
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� ijѧ����ʵ��������5��ʵ�飺
(1)��������Һ����μ���ϡ��ˮֱ��������
(2)��������Һ�м���NaOH��Һֱ��������
(3)��ǿ������Һ����μ���������Һֱ��������
(4)��ƫ��������Һ��ͨ ��CO2ֱ��������
(5)��ǿ����Һ����μ���ƫ��������Һֱ��������
����������ʵ�黭������5��ͼ��������Ϊ�������ʵ�����������Ϊ��Һ�м��� ���ʵ�����ʵ����ͼ�������ϵ��ȷ����?
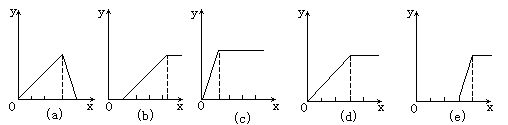
? [? ]
A��(1)��(a)
B��(3)��(e)
C��(2)��(b)
D��(4)��(d)
�ο��𰸣�B
���������
�����Ѷȣ�һ��