微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某反应体系中的物质有NaOH、Au2O3,Na2S4O6,Au2O,H2O,Na2S2O3.Au2O3为反应物,则下列有关说法正确的是( )
A.该反应体系中有三种元素的价态发生了变化
B.Au2O在反应中作还原剂
C.Na2S2O3发生还原反应
D.1molAu2O3发生反应,转移电子4mol
参考答案:因为Au2O3为反应物,则Au2O必定为生成物,在Au2O3中Au的化合价为+3,Au2O中Au的化合价为+1,即Au在反应中化合价降低,则另一种元素的化合价必定升高,在Na2S2O3中S的化合价为+2,Na2S4O6中S的化合价为2.5价,所以Na2S2O3为反应物,Na2S4O6为生成物,根据化合价的升降总数相等,以及Na+守恒,则生成物中必定为NaOH,则反应的化学方程式为:
Au2O3+4Na2S2O3+2H2O=Au2O+2Na2S4O6+4NaOH.则
A.反应中只有Au和S两种元素的化合价发生变化,故A错误;
B.Au2O为生成物,为还原产物,故B错误;
C.Na2S2O3中S的化合价为+2,Na2S4O6中S的化合价为2.5价,Na2S2O3发生氧化反应,故C错误;
D.1molAu2O3发生反应,转移电子2×(3-1)mol=4mol,故D正确.
故选D.
本题解析:
本题难度:一般
2、选择题 属于氧化还原反应的离子反应是( )
A.氢气通过灼热的氧化铜
B.稀盐酸和碳酸钠溶液
C.铜片与硝酸汞溶液
D.氧化铝与氢氧化钠溶液混合
参考答案:A.为氧化还原反应,但不是离子反应,故A错误;
B.为离子反应,但不是氧化还原反应,故B错误;
C.为离子反应,Cu和Hg元素的化合价发生变化,属于氧化还原反应,故C正确;
D.为离子反应,但不是氧化还原反应,故D错误.
故选C.
本题解析:
本题难度:一般
3、填空题 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).

(1)若A是一种黄色单质固体,则B→C的化学方程式为______.
(2)若A是一种活泼金属,C是淡黄色固体,则C中阳离子与阴离子数之比为______.试写出C与水反应的化学方程式______(用双线桥表示电子转移).
(3)若C是红棕色气体,则A的化学式可能为______.
参考答案:(1)A是一种黄色单质固体,应为S,则B为SO2,C为SO3,SO2在催化剂条件下生成SO3,
反应的方程式为2SO2+O2?催化剂
本题解析:
本题难度:一般
4、简答题 A、B、C、D、E五种短周期元素的原子序数依次增大,且已知:①其原子半径的大小关系是:D>E>B>C>A;②A、D同主族,可形成离子化合物;③B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;④B、E两元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和.请填写下列空白:
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg?B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
参考答案:由题干条件可知,A、B、E是在三个不同周期的短周期主族元素,B、C在同一周期(第二周期),D、E在同一周期(第三周期),A为H元素,A、D同主族,可形成离子化合物,可形成NaH,D为Na元素,B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,则一定有Al元素,因D为Na,则E为Al,可形成含氧酸盐,则所得盐中均含C元素,C应为O元素,B为N元素,则
(1)B、D的最高价氧化物对应的水化物分别为HNO3、NaOH,都为强电解质,浓度相同时,对水的电离的抑制程度相同,则水电离出的c(H+)的相对大小关系X等于Y,化合物NH5所属晶体类型为离子晶体,应为NH4H,为离子化合物,电子式为
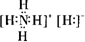
,
故答案为:等于;
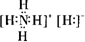
;
(2)使气态NH3变成液态后从混合气体中分离出去,应采用液化的方法,有利于平衡向正反应方向移动,
故答案为:冷却;
(3)Al与NaOH反应的离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,在反应3NO2+H2O=2HNO3+NO中,被氧化与被还原的物质的量之比2:1,
故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;2:1;
(4)n(N2H4)=132mol,则1molN2H4气体燃烧放出的热量为32×16.7kJ=534.4kJ,
所以该燃烧反应的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.4kJ/mol,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.4kJ/mol;
(5)X、Y分别是B、C与A形成的10电子微粒,则X为NH3,Y为H2O,NH3可与H3O+反应生成NH4+,
发生NH3+H3O+=NH4++H2O,说明NH3结合H+能力较H2O强,故答案为:NH3+H3O+=NH4++H2O.
本题解析:
本题难度:一般
5、选择题 P4剧毒,不小心沾到皮肤上可以用CuSO4溶液解毒,反应为11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4,下列说法正确的是( )
A.P4是还原剂,CuSO4是氧化剂
B.1molP4可还原
mol的P4
C.被氧化的P4和被还原的P4的质量比为5:6
D.0.6molCuSO4可氧化0.11mol的P4
参考答案:A、反应11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4中,化合价降低元素是Cu和P,所在的反应物P4和CuSO4是氧化剂,化合价升高元素是P,所在的反应物P4还原剂,故A错误;
B、在反应中,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,11molP4参与反应,其中5mol的P4做氧化剂,60mol硫酸铜做氧化剂,只有6mol的P4做还原剂,反应共转移120mol电子,1molP4做氧化剂时会得到12mol电子,只可还原112mol的P4,故B正确;
C、氧化还原反应中化合价升高的磷元素有11mol,即6mol的P4被氧化,的P4和化合价降低的磷元素有20 mol,即5mol的P4被还原,被氧化的P4和被还原的P4的质量比为6:5,故C错误;
D、该氧化还原反应中参加反应的硫酸铜是60mol,做氧化剂被还原的P4是5mol,所以0.6mol的CuSO4可氧化0.5mol的P4,故D错误.
故选B.
本题解析:
本题难度:简单