微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知S、Cr两元素的最高价均为+6,则下列粒子中,从化合价分析,可能存在过氧键(―O―O―)的是(? )
A.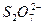
B.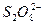
C.
D.
参考答案:B
本题解析:―O―O―中O元素的化合价为-1,因此有-1价氧元素的粒子中就应有过氧键。分析四种粒子中各元素的化合价,只有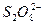 中有部分氧元素为-1价。
中有部分氧元素为-1价。
本题难度:简单
2、选择题 为研究CO2和SO2的有关性质,某学生做如下实验:如图,烧瓶中分别收集的是两种气体,烧瓶内导管口系着瘪气球,向瓶中滴加品红试液,反应一段时间后,对实验现象的描述正确的是( )

A.甲烧瓶中试液变无色,气球均胀大,且甲大于乙
B.两试液均变无色,气球均胀大,且甲小于乙
C.分别取出瓶中溶液,向其中滴加BaCl2溶液,均能产生白色沉淀
D.分别取出瓶中溶液,向其中滴加BaCl2溶液,甲中的溶液产生白色沉淀,乙不能
参考答案:A
本题解析:本题考查了两种气体的物理性质和化学性质。物理性质方面,因SO2溶解度大于CO2,烧瓶甲内气体压强明显减小,气球鼓胀的程度甲大于乙;化学性质方面,SO2有漂白性,甲烧瓶中因充有SO2,品红试液褪色,而乙烧瓶中无此现象;滴加BaCl2溶液中,均不能产生白色沉淀。答案为A。
本题难度:一般
3、实验题 某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告。
物质
| 类别
| 化学性
质预测
| 实验验证
|
实验操作
| 实验现象
| 实质(用离子
方程式表示)
|
二氧
化硫
| 酸性
氧化物
| 与水
反应
| 将盛满SO2气体的试管倒立在水中,并测定试管中溶液的pH
| ①?
| SO2+H2O
 H2SO3 H2SO3
|
与碱
反应
| ②?
| 出现白
色沉淀
| ③?
|
?
(2)该探究小组还根据SO2中S元素的化合价,预测并通过实验探究SO2的其他性质。探究过程中选用的实验药品有:浓硫酸、亚硫酸钠固体、Na2S溶液、酸性高锰酸钾溶液、品红溶液等。探究过程的实验装置图如图所示,请回答下列问题。
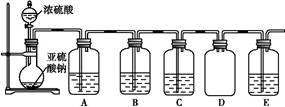
①请你完成下列表格。
装置
| 药品
| 作用
|
A
| ?
| 验证二氧化硫的还原性
|
B
| ?
| ?
|
C
| 品红溶液
| ?
|
?
②A中发生反应的离子方程式为?。
③实验时C中的实验现象是?。
④D装置的作用是?。E是尾气处理装置,有人认为E装置中可以加入足量的Ba(NO3)2溶液,你认为是否合理,请结合离子方程式加以说明:?。
参考答案:(1)①试管中液面上升,溶液pH<7
②将二氧化硫气体通入足量澄清石灰水[或Ba(OH)2溶液]中
③SO2+Ca2++2OH-=CaSO3↓+H2O(或SO2+Ba2++2OH-=BaSO3↓+H2O)
(2)①
装置
药品
作用
A
酸性高锰酸钾溶液
?
B
Na2S溶液
验证二氧化硫的氧化性
C
?
验证二氧化硫的漂白性
?
②5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
③品红溶液褪色
④防倒吸?不合理,因为发生的反应为3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO↑+4H+,生成的NO仍然对环境有污染
本题解析:(1)二氧化硫在水中的溶解度较大,将盛满SO2气体的试管倒立在水中,由于二氧化硫的溶解造成试管内压强减小,导致液面上升。同时,二氧化硫的水溶液即亚硫酸呈酸性,所以溶液的pH<7。验证二氧化硫与碱反应时,由于题目要求“出现白色沉淀”,因此不能用NaOH、KOH等碱溶液,必须用Ba(OH)2或Ca(OH)2等碱溶液。(2)根据所提供的药品,验证二氧化硫的还原性,可选择具有强氧化性的酸性高锰酸钾溶液。品红溶液显然是验证二氧化硫的漂白性,现象是品红溶液褪色。具有还原性的Na2S判断SO2具有氧化性。二氧化硫的水溶液呈酸性,在酸性环境中2NO3-可将溶液中+4价的S氧化为SO42-并生成BaSO4沉淀,同时2NO3-被还原为NO,带来新的污染。
本题难度:一般
4、选择题 下列关于SO2性质的说法中,不正确的是
A.能使品红溶液褪色
B.能与水反应生成硫酸
C.能与NaOH溶液反应
D.能使酸性KMnO4溶液褪色
参考答案:B
本题解析:A.SO2有漂白性,能使品红溶液褪色。正确但不符合题意。B .SO2与水发生反应产生亚硫酸。错误,符合题意。C. SO2是酸性氧化物,与碱发生反应SO2+2NaOH=Na2SO3+H2O. 正确但不符合题意.D.SO2有还原性,能被高锰酸钾溶液氧化: 2KMnO4+5SO2+2H2O= K2SO4+ 2MnSO4 + 2H2SO4。能使酸性KMnO4溶液褪色.正确但不符合题意。选项为B.2的性质。
本题难度:一般
5、选择题 将浸湿了溴水的棕红色滤纸,挂在含二氧化硫的容器里,滤纸褪色了,这是因为( )
A.二氧化硫具有漂白性
B.溴挥发而褪色
C.二氧化硫具有还原性
D.溴被还原成Br―
参考答案:CD
本题解析:溴水和二氧化硫发生了氧化还原反应,Br2+SO2+2H2O=2HBr+H2SO4,滤纸褪色。故选CD。
点评:本题考查的是常见无机化合物的性质和氧化还原反应,难度不大,掌握好基础知识很容易解得本题。
本题难度:一般